Coniférine
La coniférine est un composé phytochimique présent notamment dans de nombreuses espèces de conifères. C'est en fait le glucoside de l'alcool coniférylique, l'un des trois principaux monolignols. C'est un métabolite des conifères servant entre autres d'intermédiaire dans la lignification de la paroi cellulaire.
| Coniférine | |
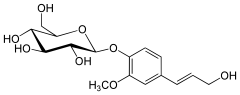
| |
| Identification | |
|---|---|
| Nom systématique | (2R,3S,4S,5R,6S)-2-(hydroxyméthyl)-6-[4-[(E)-3-hydroxyprop-1-ényl]-2-méthoxyphénoxy]oxane-3,4,5-triol |
| Synonymes |
4-(3-hydroxyprop-1-én-1-yl)-2-méthoxyphényl β-D-glucopyranoside, alcool coniférylique β-D-glucoside, coniférol β-D-glucoside, coniféroside |
| No CAS | |
| No ECHA | 100.230.647 |
| PubChem | 5280372 |
| ChEBI | 16220 |
| SMILES | |
| InChI | |
| Apparence | aiguilles incolores au goût légèrement amer[1] - [2] |
| Propriétés chimiques | |
| Formule | C16H22O8 |
| Masse molaire[3] | 342,341 1 ± 0,016 7 g/mol C 56,13 %, H 6,48 %, O 37,39 %, |
| Propriétés physiques | |
| T° fusion | 186 °C[2] |
| Solubilité | faiblement soluble dans l'eau froide (5 g·l−1), bonne dans l'eau bouillante, insoluble dans l'éther[4] |
| Précautions | |
| SGH | |
 |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Occurrence naturelle

L'agronome allemand Theodor Hartig est le premier à l'isoler en 1861 de la sève cambiale du mélèze. Wilhelm Kubel (de), un pharmacien de Holzminden, l'a identifié pour la première fois comme glucoside de l'alcool coniférilique en 1866[5]. La coniférine est le principal glycoside des conifères et a été isolée par exemple du mélèze Larix decidua, de l'épicéa commun (Picea abies), des pins Pinus cembra et Pinus strobus ainsi que du frêne Fraxinus quadrangulata. Elle est également présente dans les extraits de racine de l'angélique officinale (Angelica archangelica subsp. litoralis)[6]. On la trouve enfin dans les asperges, le salsifis noir, la betterave sucrière et d'autres plantes[1] - [2].
Propriétés
Dans la coniférine, le D-glucose est β1-lié glycosidiquement à l'alcool coniférylique. Sous forme de dihydrate, il se présente sous la forme d'aiguilles incolores, solubles dans l'eau et l'alcool, mais pas dans l'éther. La coniférine a un goût légèrement amer, est inodore et s'altère à l'air libre[1].
La coniférine se divise en D-glucose et en alcool coniférylique après avoir été chauffée avec des acides dilués ou par l'enzyme émulsine (une β-glucosidase)[1] - [7]. La coniférine, en solution avec du phénol et de l'acide chlorhydrique concentré, prend une couleur bleue intense. Cette réaction de détection peut également être utilisée pour trouver de la coniférine dans les différents bois de conifères[1].
Extraction
La coniférine est obtenue par écorçage des grumes de conifères fraîchement coupées au moment de la formation du bois (au printemps et au début de l'été). On racle le cambium du bois en formation pour en recueillir la sève qui est bouillie, filtrée et séparée par évaporation. Les cristaux obtenus ont alors purifiés par recristallisation[1].
Utilisations
La coniférine peut être oxydée en vanilline avec du dichromate de potassium et de l'acide sulfurique[1]. C'est la méthode qu'ont utilisé les chimistes Ferdinand Tiemann et Wilhelm Haarmann pour la première synthèse de la vanilline. Si la coniférine a été un temps utilisée pour la production de vanilline, il est plus efficace de le faire à partir de l'eugénol.
Notes et références
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Coniferin » (voir la liste des auteurs).
- Tiemann, F. & Haarmann, W., « Ueber das Coniferin und seine Umwandlung in das aromatische Princip der Vanille. », Berichte der deutschen chemischen Gesellschaft, vol. 7, , p. 608–623 (DOI 10.1002/cber.187400701193)
- (de) « Coniferin », sur Römpp Online, Georg Thieme Verlag (consulté le )
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals, Whitehouse Station (N.J.), Merck, , 14e éd., 2564 p. (ISBN 978-0-911910-00-1), p. 420
- (de) Wilhelm Kubel, « Coniferin - ein Glucosid aus dem Cambialsafte der Nadelhölzer », Journal für Praktische Chemie, vol. 97, , p. 243–246 (lire en ligne)
- John Lemmich, Svend Havelund and Ole Thastrup, « Dihydrofurocoumarin glucosides from Angelica archangelica and Angelica silvestris », Phytochemistry, vol. 22, no 2, , p. 553–555 (DOI 10.1016/0031-9422(83)83044-1)
- (de) Hermann Ammon, Hunnius pharmazeutisches Wörterbuch, de Gruyter, , 8e éd., 1528 p. (ISBN 978-3-11-015792-5 et 3-11-015792-6)