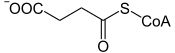
Succinate-CoA ligase (formant de l'ADP)
La succinyl-CoA synthétase formant de l'ADP (A-SCS), également appelée succinate thiokinase et succinate-CoA ligase, est une ligase qui catalyse la réaction :
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
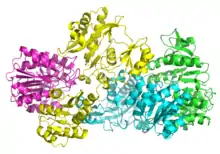
Cette enzyme de la matrice mitochondriale des eucaryotes catalyse la seule phosphorylation au niveau du substrat du cycle de Krebs. Elle réalise le couplage d'une réaction exergonique, l'hydrolyse de la Succinyl-CoA en succinate, avec la phosphorylation de l'ADP en ATP, qui est une réaction endergonique. La variation d'enthalpie libre standard résultante de cette réaction vaut ΔG°’ = −3,4 kJ·mol-1.
Il existe une autre isoforme de la succinyl-CoA synthétase, fonctionnant avec le GDP plutôt qu'avec l'ADP : la succinate-CoA ligase formant du GDP (G-SCS, EC ). On a pu montrer que, chez les mammifères, les tissus intervenant essentiellement dans l'anabolisme, tels que le foie et les reins, tendent plutôt à exprimer la G-SCS, tandis que les tissus intervenant essentiellement dans le catabolisme, tels que le cerveau, le cœur et les muscles, tendent plutôt à exprimer l'A-SCS[2].
Notes et références
- (en) Marie E. Fraser, Michael N.G. James, William A. Bridger3 et William T. Wolodko, « A detailed structural description of Escherichia coli succinyl-CoA synthetase », Journal of Molecular Biology, vol. 285, no 4, , p. 1633-1653 (PMID 9917402, DOI 10.1006/jmbi.1998.2324, lire en ligne)
- (en) David O. Lambeth, Kristin N. Tews, Steven Adkins, Dean Frohlich et Barry I. Milavetz, « Expression of Two Succinyl-CoA Synthetases with Different Nucleotide Specificities in Mammalian Tissues », Journal of Biological Chemistry, vol. 279, no 35, , p. 36621-36624 (PMID 15234968, DOI 10.1074/jbc.M406884200, lire en ligne)
- (en) Kaufman S, « Studies on the mechanism of the reaction catalyzed by the phosphorylating enzyme », J. Biol. Chem., vol. 216, , p. 153-164 (PMID 13252015)
- (en) Kaufman S and Alivasatos SGA, « Purification and properties of the phosphorylating enzyme from spinach », J. Biol. Chem., vol. 216, , p. 141-152 (PMID 13252014)