Pyridazine
La pyridazine (ou 1,2-diazine) est une molécule di-azotée hétérocyclique de formule chimique C4H4N2. Entre les années 1966-1970, Henri Laborit fait une étude de cette famille chimique et introduit en thérapeutique l'AGR 1240 minaprine commercialisée sous le nom de Cantor.
| Pyridazine[1] | |
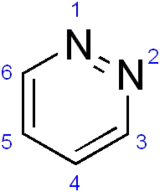
| |
| Structure de la Pyridazine. | |
| Identification | |
|---|---|
| Nom UICPA | Pyridazine |
| Synonymes |
1,2-diazine |
| No CAS | |
| No ECHA | 100.005.478 |
| No CE | 206-025-5 |
| PubChem | |
| SMILES | |
| InChI | |
| Apparence | Liquide incolore |
| Propriétés chimiques | |
| Formule | C4H4N2 [Isomères] |
| Masse molaire[2] | 80,088 ± 0,003 9 g/mol C 59,99 %, H 5,03 %, N 34,98 %, |
| pKa | 2,24 à 20 °C[1] |
| Moment dipolaire | 4,22 ± 0,02 D [3] |
| Propriétés physiques | |
| T° fusion | −8 °C[1] |
| T° ébullition | 208 °C[1] |
| Solubilité | Soluble dans l'eau[1]. |
| Masse volumique | 1,107 |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 8,67 ± 0,03 eV (gaz)[4] |
| Précautions | |
| Directive 67/548/EEC | |
 Xi |
|
| Écotoxicologie | |
| DL50 | 2 650 mg·kg-1 (souris)[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
Structure
La pyridazine possède 2 atomes d'azote compris dans un cycle aromatique à 6 chaînons. Elle est l'isomère de position de la pyrimidine (1,3-diazine) et de la pyrazine (1,4-diazine).
De nombreux composés contiennent le noyau pyridazine, par exemple :
- herbicides comme la credazine, le pyridafol et le pyridate ;
- médicaments comme le cefozopran, la cadralazine, la minaprine, l'hydralazine et le cilazapril.
Propriétés physiques
Son poids moléculaire est de 80,09 g·mol-1. À température supérieure à −8 °C, c'est un liquide incolore qui passe à l'état gazeux vers les 208 °C.
Utilisation
Elle est principalement utilisée en recherche et dans l'industrie chimique comme produit de départ ou d'addition pour la synthèse de composés plus complexes. Très peu de composés naturels contenant cette structure sont connus, avec pour exception les monoamycines (antibactérien).
Notes et références
- (en) ChemIDplus, « Pyridazine - RN: 289-80-5 », sur chem.sis.nlm.nih.gov, U.S. National Library of Medicine (consulté le )
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1 et 1-4200-6679-X), p. 9-50
- (en) David R. Lide, Handbook of chemistry and physics, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205