NCK2
La protéine cytoplasmique NCK2, également connue sous le nom NCK-beta et Grb4, est une protéine qui, chez l'homme, est codée par le gène NCK2[5] - [6] - [7] - [8].
| Protéine cytoplamique NCK2 | ||
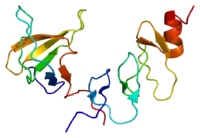 Modélisation en 3D de la protéine NCK2 | ||
| Caractéristiques générales | ||
|---|---|---|
| Nom approuvé | Protéine cytoplasmique NCK2 Protéine adaptatrice NCK 2 Growth Factor Receptor-Bound Protein 4 Protéine adaptatrice SH2/SH3 NCK-Beta[1] | |
| Symbole | O43639-NCK2_HUMAN | |
| Synonymes | Grb4 | |
| Fonction | Adaptateur | |
| Humain | ||
| Locus | 2q12.2105,894,274 | |
| Localisation | 105,744,648 | |
| Point isoélectrique | 6.49[2] | |
| Masse moléculaire | 42 915[3] Da[4] | |
| Nombre de résidus | 380[3] acides aminés[4] | |
Description et fonction
NCK appartient à la famille des protéines adaptatrices, il existe deux gènes NCK chez les mammifères, NCK1 et NCK2[8]. Au sein de l'espèce humaine, NCK1 est localisé sur le chromosome 3 et NCK2 est situé dans le chromosome 2[8]. La protéine est composée de trois domaines SH3 (en) et un domaine SH2 (en)[8]. La protéine n'a pas de fonction catalytique connue[8]. Néanmoins, il été a démontré qu'elle s'associe et qu'elle recrute diverses protéines impliquées dans la régulation de la protéine tyrosine kinases réceptrice[8]. C'est grâce à ces actions régulatrices que cette protéine est censée être impliquée dans la réorganisation du cytosquelette[8]. En outre, des variants d'épissage, de transcription alternatives et codant différentes protéines de type isoformes, ont été identifiés sur cet adaptateur cytoplasmique[8].
Implications et interactions
Il a été déterminé que NCK2 peut notamment interagir avec :
- Le Récepteur du facteur de croissance épidermique (EGF)[5] ;
- LIMS1 (en)[9] - [10] ;
- PDGFRB (en)[11] ;
- PTK2[12] ;
- La Glycoprotéine de surface cellulaire TCD3 à chaîne d'epsilon (en)[13] ;
- TrkB (en)[14] ;
- Enfin, au cours d'une transmission synaptique, cette protéine adaptatrice de type cytoplasmique peut également entrer en interaction avec la famille d'enzymes PAK[15], dont en particulier la PAK3 (en)[16].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « NCK2 » (voir la liste des auteurs).
Notes
Références
- (en) « UniProtKB - O43639 (NCK2_HUMAN) », sur le site "Uniprot" (consulté le ).
- (en) « NCK2 (human) », sur le site "Phosphosite" (consulté le ).
- (en) « UCSC Genome Browser on Human Dec. 2013 (GRCh38/hg38) Assembly », sur le site GenomeUcscEdu (consulté le ).
- Les valeurs de la masse et du nombre de résidus indiquées ici sont celles du précurseur protéique issu de la traduction du gène, avant modifications post-traductionnelles, et peuvent différer significativement des valeurs correspondantes pour la protéine fonctionnelle.
- M. Chen, H. She, E. M. Davis, C. M. Spicer et al., « Identification of Nck family genes, chromosomal localization, expression, and signaling specificity », The Journal of Biological Chemistry, vol. 273, no 39, , p. 25171–8 (PMID 9737977, DOI 10.1074/jbc.273.39.25171).
- (en) L.E. Braverman et L.A. Quilliam, « Identification of Grb4/Nckbeta, a src homology 2 and 3 domain-containing adapter protein having similar binding and biological properties to Nck », The Journal of Biological Chemistry, vol. 274, no 9, , p. 5542–9 (PMID 10026169, DOI 10.1074/jbc.274.9.5542)
- (en) Liu J., Li M., Ran X., Fan J.S. et Song J., « Structural insight into the binding diversity between the human Nck2 SH3 domains and proline-rich proteins », Biochemistry, vol. 45, no 23, , p. 7171–84 (PMID 16752908, DOI 10.1021/bi060091y).
- (en) « Code Gène : NCK2 NCK adaptor protein 2 », sur le site Ncbi (consulté le ).
- (en) Y. Tu, F. Li, S. Goicoechea et C. Wu, « The LIM-only protein PINCH directly interacts with integrin-linked kinase and is recruited to integrin-rich sites in spreading cells », Molecular and Cellular Biology, vol. 19, no 3, , p. 2425–34 (PMID 10022929, PMCID 84035, DOI 10.1128/mcb.19.3.2425).
- (en) Y. Tu, F. Li et C. Wu, « Nck-2, a novel Src homology2/3-containing adaptor protein that interacts with the LIM-only protein PINCH and components of growth factor receptor kinase-signaling pathways », Molecular Biology of the Cell, vol. 9, no 12, , p. 3367–82 (PMID 9843575, PMCID 25640, DOI 10.1091/mbc.9.12.3367).
- (en) Chen M., She H., A. Kim et al., « Nckbeta adapter regulates actin polymerization in NIH 3T3 fibroblasts in response to platelet-derived growth factor bb », Molecular and Cellular Biology, vol. 20, no 21, , p. 7867–80 (PMID 11027258, PMCID 86398, DOI 10.1128/mcb.20.21.7867-7880.2000).
- (en) S. M. Goicoechea, Y. Tu, Y. Hua et al., « Nck-2 interacts with focal adhesion kinase and modulates cell motility », The International Journal of Biochemistry & Cell Biology, vol. 34, no 7, , p. 791–805 (PMID 11950595, DOI 10.1016/s1357-2725(02)00002-x).
- (en) D. Gil, W. W. Schamel, M. Montoya, F. Sánchez-Madrid et B. Alarcon, « Recruitment of Nck by CD3 epsilon reveals a ligand-induced conformational change essential for T cell receptor signaling and synapse formation », Cell, vol. 109, no 7, , p. 901–12 (PMID 12110186, DOI 10.1016/S0092-8674(02)00799-7).
- (en) S. Suzuki, M. Mizutani, Suzuki K., M. Yamada et al., « Brain-derived neurotrophic factor promotes interaction of the Nck2 adaptor protein with the TrkB tyrosine kinase receptor », Biochemical and Biophysical Research Communications, vol. 294, no 5, , p. 1087–92 (PMID 12074588, DOI 10.1016/S0006-291X(02)00606-X).
- (en) Dominique Bagnard, Axon Growth and Guidance, Springer Science & Business Media, , 170 p. (lire en ligne), pages 32 à 40.
- Alexandre Moreau, « III. Rôle de l’interaction Nck2/PAK3 dans la modulation de la transmission synaptique excitatrice : contrôle sérotoninergique de la balance excitation-inhibition dans le cortex visuel. », dans Alexandre Moreau, Neuromodulation des réseaux neuronaux, Université Paris-Sud, (lire en ligne [PDF]), pages 157 à 180.
Pour approfondir
Bibliographie
- (en) Dominique Bagnard, Axon Growth and Guidance, Springer Science & Business Media, , 170 p. (lire en ligne), pages 32 à 40.
- Alexandre Moreau, « III. Rôle de l’interaction Nck2/PAK3 dans la modulation de la transmission synaptique excitatrice : contrôle sérotoninergique de la balance excitation-inhibition dans le cortex visuel. », dans Alexandre Moreau, Neuromodulation des réseaux neuronaux, Université Paris-Sud, (lire en ligne [PDF]), pages 157 à 180.
- (en) N. Xu et M. Henkemeyer, « Ephrin-B3 reverse signaling through Grb4 and cytoskeletal regulators mediates axon pruning », Nature Neuroscience, vol. 12, , p. 268–276 (PMID 19182796, PMCID 2661084, DOI 10.1038/nn.2254).
- (en) Lei Shi, « Dock protein family in brain development and neurological disease », Communicative & Integrative Biology, vol. 6, no 6, (DOI 10.4161/cib.26839, lire en ligne, consulté le ).
- (en) Li W, Hu P, Skolnik EY et al., « The SH2 and SH3 domain-containing Nck protein is oncogenic and a common target for phosphorylation by different surface receptors », Molecular and Cellular Biology, vol. 12, no 12, , p. 5824–33 (PMID 1333047, PMCID 360522, DOI 10.1128/MCB.12.12.5824).
- (en) Tu Y, Li F et Wu C, « Nck-2, a novel Src homology2/3-containing adaptor protein that interacts with the LIM-only protein PINCH and components of growth factor receptor kinase-signaling pathways », Molecular Biology of the Cell, vol. 9, no 12, , p. 3367–82 (PMID 9843575, PMCID 25640, DOI 10.1091/mbc.9.12.3367).
- (en) Tu Y, Li F, Goicoechea S et Wu C, « The LIM-only protein PINCH directly interacts with integrin-linked kinase and is recruited to integrin-rich sites in spreading cells », Molecular and Cellular Biology, vol. 19, no 3, , p. 2425–34 (PMID 10022929, PMCID 84035, DOI 10.1128/mcb.19.3.2425).
- (en) Braverman LE et Quilliam LA, « Identification of Grb4/Nckbeta, a src homology 2 and 3 domain-containing adapter protein having similar binding and biological properties to Nck », The Journal of Biological Chemistry, vol. 274, no 9, , p. 5542–9 (PMID 10026169, DOI 10.1074/jbc.274.9.5542).
- (en) Coutinho S, Jahn T, Lewitzky M et al., « Characterization of Ggrb4, an adapter protein interacting with Bcr-Abl », Blood, vol. 96, no 2, , p. 618–24 (PMID 10887126).
- (en) Chen M, She H, Kim A, Woodley DT et Li W, « Nckbeta adapter regulates actin polymerization in NIH 3T3 fibroblasts in response to platelet-derived growth factor bb », Molecular and Cellular Biology, vol. 20, no 21, , p. 7867–80 (PMID 11027258, PMCID 86398, DOI 10.1128/MCB.20.21.7867-7880.2000).
- (en) Tu Y, Kucik DF et Wu C, « Identification and kinetic analysis of the interaction between Nck-2 and DOCK180 », FEBS Letters, vol. 491, no 3, , p. 193–9 (PMID 11240126, DOI 10.1016/S0014-5793(01)02195-0).
- (en) Jahn T, Seipel P, Coutinho S, Miething C et al., « Grb4/Nckbeta acts as a nuclear repressor of v-Abl-induced transcription from c-jun/c-fos promoter elements », The Journal of Biological Chemistry, vol. 276, no 46, , p. 43419–27 (PMID 11514578, DOI 10.1074/jbc.M107030200).
- (en) Cowan CA et Henkemeyer M, « The SH2/SH3 adaptor Grb4 transduces B-ephrin reverse signals », Nature, vol. 413, no 6852, , p. 174–9 (PMID 11557983, DOI 10.1038/35093123).
- (en) Goicoechea SM, Tu Y, Hua Y et al., « Nck-2 interacts with focal adhesion kinase and modulates cell motility », The International Journal of Biochemistry & Cell Biology, vol. 34, no 7, , p. 791–805 (PMID 11950595, DOI 10.1016/S1357-2725(02)00002-X).
- (en) Suzuki S, Mizutani M, Suzuki K et al., « Brain-derived neurotrophic factor promotes interaction of the Nck2 adaptor protein with the TrkB tyrosine kinase receptor », Biochemical and Biophysical Research Communications, vol. 294, no 5, , p. 1087–92 (PMID 12074588, DOI 10.1016/S0006-291X(02)00606-X).
- (en) Gil D, Schamel WW, Montoya M et al., « Recruitment of Nck by CD3 epsilon reveals a ligand-induced conformational change essential for T cell receptor signaling and synapse formation », Cell, vol. 109, no 7, , p. 901–12 (PMID 12110186, DOI 10.1016/S0092-8674(02)00799-7).
- (en) Song J, Vranken W, Xu P et al., « Solution structure and backbone dynamics of the functional cytoplasmic subdomain of human ephrin B2, a cell-surface ligand with bidirectional signaling properties », Biochemistry, vol. 41, no 36, , p. 10942–9 (PMID 12206665, DOI 10.1021/bi025815u).
- (en) Aspenström P, « The WASP-binding protein WIRE has a role in the regulation of the actin filament system downstream of the platelet-derived growth factor receptor », Experimental Cell Research, vol. 279, no 1, , p. 21–33 (PMID 12213210, DOI 10.1006/excr.2002.5576).
- (en) S. Hafizi, F. Alindri, R. Karlsson et B. Dahlbäck, « Interaction of Axl receptor tyrosine kinase with C1-TEN, a novel C1 domain-containing protein with homology to tensin », Biochemical and Biophysical Research Communications, vol. 299, no 5, , p. 793–800 (PMID 12470648, DOI 10.1016/S0006-291X(02)02718-3)
- (en) Velyvis A, Vaynberg J, Yang Y et al., « Structural and functional insights into PINCH LIM4 domain-mediated integrin signaling », Nature Structural Biology, vol. 10, no 7, , p. 558–64 (PMID 12794636, DOI 10.1038/nsb938).
- (en) Ran X et Song J, « Structural insight into the binding diversity between the Tyr-phosphorylated human ephrinBs and Nck2 SH2 domain », The Journal of Biological Chemistry, vol. 280, no 19, , p. 19205–12 (PMID 15764601, DOI 10.1074/jbc.M500330200).
- (en) Song J, « Tyrosine phosphorylation of the well packed ephrinB cytoplasmic beta-hairpin for reverse signaling : Structural consequences and binding properties », The Journal of Biological Chemistry, vol. 278, no 27, , p. 24714–20 (PMID 12606549, DOI 10.1074/jbc.M210625200).
Liens externes
- (en) « NCK2 NCK adaptor protein 2 [Homo sapiens (human)] », sur le site NCBI, (consulté le ).
- (en) « NCK2 Gene (Protein Coding) : NCK Adaptor Protein 2 », sur le site GENCARDS Human gene database, Weizmann Institute of Science (consulté le ).