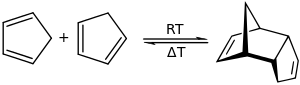
Dicyclopentadiène
Le dicyclopentadiène (DCPD) est un composé organique tricyclique de formule C10H12. À température ambiante, très pur c'est un solide incolore à jaunâtre avec une odeur proche du camphre (moins pur c'est un liquide). Sa densité d'énergie est de 10,975 Wh·L-1. Il est coproduit en larges quantités lors du vapocraquage du naphta et du fioul pour produire de l'éthylène. Son usage principal est sous forme de résines, en particulier des résines de polyesters insaturés. Il est aussi utilisé pour la fabrication des encres, adhésifs et peintures.
| Dicyclopentadiène | ||
| ||
 | ||
| Identification | ||
|---|---|---|
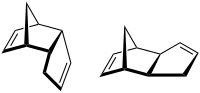
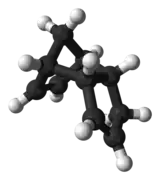
| Nom UICPA | tricyclo[5.2.1.02,6]deca-3,8-diène | |
| Synonymes |
1,3-dicyclopentadiène |
|
| No CAS | ||
| No ECHA | 100.000.958 | |
| No CE | 247-724-5 | |
| No RTECS | PC1050000 | |
| PubChem | 6492 6428576 (6R) 10396885 (1S,7R) |
|
| InChI | ||
| Apparence | cristal ou poudre (très pur) ou liquide incolore à jaunâtre, odeur gênante de camphre même faible concentration[1] | |
| Propriétés chimiques | ||
| Formule | C10H12 [Isomères] |
|
| Masse molaire[2] | 132,202 3 ± 0,008 8 g/mol C 90,85 %, H 9,15 %, |
|
| Propriétés physiques | ||
| T° fusion | 33 °C[1] | |
| T° ébullition | 166 °C[1] | |
| Solubilité | 0,04 g·l-1 (eau, 20 °C)[3] | |
| Masse volumique | 0,94 g·cm-3 (20 °C)[1] | |
| T° d'auto-inflammation | 500 °C[1] | |
| Point d’éclair | 39 °C (coupelle fermée)[1] | |
| Limites d’explosivité dans l’air | 0,8-6,3 vol. %[1] | |
| Pression de vapeur saturante | 2,98 mbar (20 °C)[1] 5,30 mbar (30 °C)[1] 9,09 mbar (40 °C)[1] 15,1 mbar (50 °C)[1] |
|
| Précautions | ||
| SGH[3] | ||
  |
||
| NFPA 704[3] | ||
| Transport[1] | ||
| Inhalation | Toxique si inhalé. Cause une irritation des voies respiratoires[3]. | |
| Peau | Nocif si absorbé à travers la peau. Cause une de la peau[3]. | |
| Yeux | Cause une des yeux[3]. | |
| Ingestion | Nocif en cas d'ingestion[3]. | |
| Écotoxicologie | ||
| DL50 | 1010 mg/kg (oiseau domestique, oral)[4] 1200 mg/kg (bétail, oral)[4] |
|
| CL50 | 660ppm/4H (rat, inhalation)[8] 771ppm/4H (lapin, inhalation)[7] 145ppm/4H (souris, inhalation)[7] 770ppm/4H (cochon d'inde, inhalation)[7] |
|
| LogP | 2,89 (20 °C)[3] | |
| Unités du SI et CNTP, sauf indication contraire. | ||
Réactivité
Lorsqu'il est chauffé au-dessus de 150 °C, il subit une rétro-réaction de Diels-Alder pour former le cyclopentadiène, un ligand commun en chimie organométallique. Cette réaction peut être catalysée par de la poudre de fer. Cette réaction est réversible, et à température ambiante, le cyclopentadiène se dimérise lentement pour reformer le dicyclopentadiène.
Utilisations
Le dicyclopentadiène peut être utilisé comme monomère pour des réactions de polymérisation, soit par polymérisation d'alcène, soit par polymérisation par ouverture de cycle par métathèse. Par exemple, dans le cas d'une polymérisation d'alcène, des copolymères peuvent être formés avec l'éthylène ou le styrène, uniquement en polymérisant à partir de la liaison double du cycle de norbornène[9]. Dans le cas d'une polymérisation par ouverture de cycle par métathèse, on forme l'homopolymère polydicyclopentadiène.
L'hydrogénation du dicyclopentadiène donne l'endo-tétrahydrodicyclopentadiène qui par réaction à haute température avec le chlorure d'aluminium se réarrange en adamantane[10].
Le tétrahydrodicyclopentadiène est utilisé comme carburant en aviation, le JP-10.
Notes et références
- Entrée « 3a,4,7,7a-Tetrahydro-4,7-methanoindene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 25 septembre 2012 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé Dicyclopentadiene, consultée le 25 septembre 201.
- National Technical Information Service. Vol. AD-A087-257,
- Progress Report for Contract No. PH-43-64-886, Submitted to the National Cancer Institute by The Institute of Chemical Biology, University of San Francisco. Vol. PH43-64-886
- "Proceedings of the International Congress on Toxicology, Toxicology as a Predictive Science, 1st, Toronto, 1977," Plaa, G.L., and W.A. Duncan, eds., New York, Academic Press, Inc., 1978Vol. -, Pg. 448, 1978.
- Toxicology and Applied Pharmacology. Vol. 20, Pg. 552, 1971 Pubmed
- National Technical Information Service. Vol. OTS0557739,
- (en) Xiaofang Li et Zhaomin Hou, « Scandium-Catalyzed Copolymerization of Ethylene with Dicyclopentadiene and Terpolymerization of Ethylene, Dicyclopentadiene, and Styrene », Macromolecules, vol. 38, no 16, , p. 6767 (DOI 10.1021/ma051323o)
- Paul von R. Schleyer, M. M. Donaldson, R. D. Nicholas, and C. Cupas, Adamantane, Org. Synth., coll. « vol. 5 », , p. 16
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Dicyclopentadiene » (voir la liste des auteurs).