Champignon pathogène
Un champignon pathogène est un mycète responsable d'infections fongiques. Les agents pathogènes fongiques, essentiellement des espèces de microchampignons, sont des parasites obligatoires ou facultatifs (parasite primaire ou parasite secondaire de faiblesse ou de blessure) qui peuvent causer des maladies chez les animaux (champignons zoopathogènes notamment chez les humains), chez les plantes (champignons phytopathogènes) ou chez d'autres organismes. L'intensification de l'élevage et des pratiques agricoles, la capacité microbienne à se propager via le commerce international et les mouvements accrus de population (à des fins touristiques ou migratoires), et le réchauffement climatique favorisent la dissémination de ces pathogènes et de leurs vecteurs. L'impact de ces facteurs biotiques et abiotiques dans le développement de maladies fongiques est largement sous-estimé alors qu'il contribue sensiblement depuis la fin du XXe siècle à la propagation des maladies infectieuses émergentes ou résurgentes qui constituent une menace pour les plantes, les animaux et la santé des écosystèmes[1].
| Sous-classe de | Fungi, agent infectieux |
|---|---|
| Cause immédiate de | mycose |
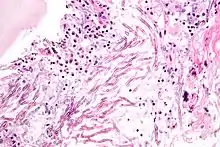



Chez les animaux
Les insectes sont attaqués par des milliers d'espèces de champignons entomopathogènes[2], les poissons par des agents ichtyopathogènes. Les champignons zoopathogènes menacent de nombreuses espèces animales en danger d'extinction : les chauves-souris (infectées notamment par Geomyces destructans), les amphibiens (Batrachochytrium dendrobatidis, Batrachochytrium salamandrivorans (en) responsables de la chytridiomycose) et les reptiles (Ophidiomyces ophiodiicola (en) responsable de l'ophidiomycose, maladie fongique du serpent)[3]…
Les champignons du genre Nematocida sont des parasites des nématodes, et notamment, Nematocida parisii est un pathogène du ver rond et animal modèle Caenorhabditis elegans.
Succès évolutif des mammifères ?
L'extinction Crétacé-Paléogène à l'origine de la disparition de nombreux animaux (dont les dinosaures non aviens et les grands reptiles) et de 65 % des espèces végétales, a entraîné de grandes accumulations de nécromasse qui a, comme les autres extinctions et radiations évolutives, favorisé la prolifération de champignons décomposeurs. À la suite de cette extinction massive, le développement de champignons pathogènes aurait entravé l'émergence d'un deuxième âge reptilien et contribué au succès évolutif des mammifères, vertébrés endothermes[4] et au système immunitaire complexe les rendant plus résistants aux infections fongiques[5].
Chez l'homme
Les pathologies fongiques chez l'homme (souvent subdivisées en infections appelées mycoses superficielles, mycoses sous-cutanées et mycoses systémiques) sont étudiées par la mycologie médicale et combattues par les antimycosiques. « Le traitement des infections fongiques a été généralement moins efficace que celui des infections bactériennes, essentiellement parce que les champignons, sont des eucaryotes, et sont beaucoup plus semblables aux cellules humaines que ne le sont les bactéries. De nombreuses substances inhibant ou tuant les champignons sont de ce fait assez toxiques pour les êtres humains et ont donc un faible indice thérapeutique. En outre, la plupart des champignons ont un système de détoxication qui modifie de nombreux agents antifongiques, et en limitent l'efficacité. La plupart des antifongiques n'ont qu'une activité fongistatique tant que des applications répétées maintiennent de hauts niveaux d'antibiotiques non modifiés. Néanmoins, quelques substances sont utiles dans le traitement de nombreuses mycoses sévères[6] ».
Près de 300 espèces fongiques connues sont impliquées dans les mycoses humaines[7]. Les maladies opportunistes systémiques dues à ces agents infectieux sont rarement contagieuses, contrairement aux maladies virales et bactériennes. Elles sont à l'origine de 1,6 million de morts par an à l'échelle mondiale[8], soit plus que celles dues aux animaux les plus mortels pour l'homme et « presque autant que la tuberculose (1,7 million), la maladie infectieuse la plus meurtrière au monde[9] ». Les principales infections fongiques sont les cryptococcoses avec une mortalité associée de 20 à 70 %, suivies par les candidoses (mortalité associée de 46 à 75 %), les pneumocystoses (20 à 80 %), les aspergilloses (30 à 95 %) et les histoplasmoses (28 à 50 %)[10].
Chez les plantes
L'étude des champignons phytopathogènes relève de la phytopathologie ou pathologie végétale. Des antifongiques à action fongicide ou fongistatique sont utilisés contre ces organismes nuisibles aux végétaux. 10 000 espèces fongiques sont considérées comme phytopathogènes[11]. Principale cause de maladies chez les plantes, ces bioagresseurs sont responsables d'environ 70 % des maladies des plantes cultivées et réduisent les rendements agricoles de plus de 20 %[12].
Chez les autres organismes
Les mycoparasites infectent une autre espèce fongique.
Notes et références
- (en) Matthew C Fisher, Daniel A Henk, Cheryl J Briggs, John S Brownstein, Lawrence C Madoff, Sarah L McCraw, Sarah J Gurr, « Emerging fungal threats to animal, plant and ecosystem health », Nature, vol. 484, no 7393, , p. 186 (DOI 10.1038/nature10947).
- (en) Robert L. Metcalf et William H. Luckmann, Introduction to Insect Pest Management, John Wiley & Sons, , p. 217
- (en) Arturo Casadevall, « Don't Forget the Fungi When Considering Global Catastrophic Biorisks », Health Security, vol. 15, no 4, , p. 341-342 (DOI 10.1089/hs.2017.0048).
- (en) Vincent A Robert, Arturo Casadevall, « Vertebrate endothermy restricts most fungi as potential pathogens », J Infect Dis, vol. 200, no 10, , p. 1623-1626 (DOI 10.1086/644642).
- (en) Arturo Casadevall, « Fungi and the Rise of Mammals », PLoS Pathog., vol. 8, no 8, (DOI 10.1371/journal.ppat.1002808)
- Lansing M Prescott, Joanne M Willey, Linda M Sherwood, Christopher J Woolverton, Microbiologie, De Boeck Superieur, (lire en ligne), p. 200
- (en) « Stop neglecting fungi », Nature Microbiology, vol. 2, no 17120, (DOI 10.1038/nmicrobiol.2017.120).
- (en) Gordon D. Brown, David W. Denning, Neil A. R. Gow1, Stuart M. Levitz, Mihai G. Netea and Theodore C. White, « Hidden Killers: Human Fungal Infections », Science Translational Medicine, vol. 4, no 165, (DOI 10.1126/scitranslmed.3004404).
- Nathaniel Herzberg, « Les champignons : menace silencieuse », Le Monde : supplément "Cahier du Monde", no 22919, , p. 1.
- (en) Tulasi Satyanarayana et Gotthard Kunze, Yeast Diversity in Human Welfare2017, Springer, p. 140
- Paysage, biodiversité fonctionnelle et santé des plantes, Editions Quae, , p. 95
- (en) Jim Deacon, « Chapter 14: Fungi as plant pathogens », Blackwell Publishing, (consulté le ).
Voir aussi
Bibliographie
- (en) Hermann H. Prell et Peter Day, Plant-Fungal Pathogen Interaction : A Classical and Molecular View, Springer Science & Business Media, , 214 p. (ISBN 978-3-540-66727-8, lire en ligne).
- (en) Charles R. Lane, Paul Bealeset Kelvin et J.D. Hughes, Fungal Plant Pathogens, CAB International, , 324 p. (ISBN 978-1-84593-778-2, lire en ligne), p. 307.
- (en) Oliver Kurzai, Human Fungal Pathogens, Springer Science & Business Media, , 307 p. (ISBN 978-1-84593-778-2, lire en ligne), p. 298
Articles connexes
Liens externes
- (en) « Global Action Fund for Fungal Infections: Gaffi (le Fonds global d’action contre les infections fongiques) », sur gaffi.org (consulté en )
- Carte montrant l'évolution des MIE dans le monde entre 1995 et 2010 : explosion des maladies infectieuses émergentes (MIE) chez les plantes et les animaux (tirée de la revue Nature, « Fear of fungi », Vol. 484, n° 7393, 12 avril 2012)


