Caryophyllène
Le caryophyllène, parfois appelé β-caryophyllène (BCP) pour le distinguer de l'humulène, un isomère jadis appelé α-caryophyllène, est un sesquiterpène naturel bicyclique composé d'un macrocycle à neuf atomes de carbone fusionné avec un noyau cyclobutane, ce qui est exceptionnel pour un composé naturel. C'est un constituant de nombreuses huiles essentielles, notamment l'huile produite par le giroflier[3], le chanvre cultivé[4], le romarin[5], le houblon et le papeda de Mélanésie (Citrus macroptera).
| Caryophyllène | |
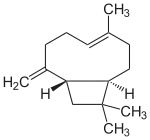 Structure du caryophyllène. |
|
| Identification | |
|---|---|
| Nom UICPA | (1R,4E,9S)-4,11,11-triméthyl-8-méthylidènebicyclo[7.2.0]undéc-4-ène |
| Synonymes |
β-caryophyllène, |
| No CAS | |
| No ECHA | 100.001.588 |
| No CE | 201-746-1 |
| No RTECS | DT8400000 |
| PubChem | 5281515 |
| ChEBI | 10357 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C15H24 [Isomères] |
| Masse molaire[1] | 204,351 1 ± 0,013 7 g/mol C 88,16 %, H 11,84 %, |
| Propriétés physiques | |
| T° ébullition | 262 à 264 °C[2] |
| Masse volumique | 0,902 g cm−3[2] à 20 °C |
| Point d’éclair | 96 °C[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
Il est également largement présent dans le poivre noir et la lavande.
Il est généralement mélangé à l'isocaryophyllène, son isomère cis, et à l'humulène, isomère comportant un macrocycle unique.
Il fait partie des composés qui contribuent à la nature épicée du poivre.
Fonctions biologiques en laboratoire
Le β-caryophyllène agit comme agoniste sélectif du récepteur cannabinoïde de type 2 (CB2) et possède un effet anti-inflammatoire cannabimimétique significatif chez la souris[4].
Il ne se lie cependant pas au récepteur cannabinoïde de type 1 (CB1) exprimé centralement et ne provoque donc pas d'effets psychomimétiques.
Il possède des activités anticancéreuses, affectant la croissance et la prolifération de nombreuses lignées de cellules cancéreuses[6].
Diverses autres activités pharmacologiques du β-caryophyllène comprennent : actions cardioprotectrices[7] - [8] - [9] - [10], hépatoprotectrices[11] - [12] - [13], gastroprotectrices[14] - [15], neuroprotectrices[16], néphroprotectrices[17], anti-convulsives[18], anti-inflammatoires[19] et immunomodulatrices[16] - [20].
Il participe à la protection des cellules dopaminergiques[21], à l'inhibition de l'activation de la microglie[22] et des astrocytes[23] et à la neuroprotection et module la nociception[24], la dépendance et la consommation d'alcool[25], prévenant également les dommages induits par l'alcool[26].
Il présente un potentiel multicible pour le traitement de la sclérose en plaques, de la maladie de Parkinson et d'autres affections neuroinflammatoires[27] - [28] - [29].
Il inhibe les comportements addictifs envers la nicotine, la cocaïne et la méthamphétamine, chez les souris[30] - [31] - [32].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé (−)-trans-Caryophyllene ≥98.5% (sum of enantiomers, GC), consultée le 21 avril 2014.
- (en) C. Ghelardini, N. Galeotti, L. Di Cesare Mannelli, G. Mazzanti et A. Bartolini, « Local anaesthetic activity of β-caryophyllene », Il Farmaco, vol. 56, nos 6-7, , p. 387-389 (PMID 11482764, DOI 10.1016/S0014-827X(01)01092-8, lire en ligne).
- (en) Jürg Gertsch, Marco Leonti, Stefan Raduner, Ildiko Racz, Jian-Zhong Chen, Xiang-Qun Xie, Karl-Heinz Altmann, Meliha Karsak et Andreas Zimmer, « Beta-caryophyllene is a dietary cannabinoid », Proceedings of the National Academy of Sciences of the United States of America, vol. 105, no 26, , p. 9099-9104 (PMID 18574142, PMCID 2449371, DOI 10.1073/pnas.0803601105, lire en ligne).
- (en) Elena Ormeño, Virginie Baldy, Christine Ballini et Catherine Fernandez, « Production and Diversity of Volatile Terpenes from Plants on Calcareous and Siliceous Soils: Effect of Soil Nutrients », Journal of Chemical Ecology, vol. 34, no 9, , p. 1219-1229 (PMID 18670820, DOI 10.1007/s10886-008-9515-2, lire en ligne).
- Klaudyna Fidyt, Anna Fiedorowicz, Leon Strządała et Antoni Szumny, « β-caryophyllene and β-caryophyllene oxide-natural compounds of anticancer and analgesic properties », Cancer Medicine, vol. 5, no 10, , p. 3007–3017 (ISSN 2045-7634, PMID 27696789, PMCID 5083753, DOI 10.1002/cam4.816, lire en ligne, consulté le )
- Nancy S. Younis, « β-Caryophyllene Ameliorates Cyclophosphamide Induced Cardiac Injury: The Association of TLR4/NFκB and Nrf2/HO1/NQO1 Pathways », Journal of Cardiovascular Development and Disease, vol. 9, no 5, , p. 133 (ISSN 2308-3425, PMID 35621844, PMCID 9145742, DOI 10.3390/jcdd9050133, lire en ligne, consulté le )
- Chunmei Bai, Qianqian Ma, Qi Li et Lijun Yu, « Combination of 1,8-cineole and beta-caryophyllene synergistically reverses cardiac hypertrophy in isoprenaline-induced mice and H9c2 cells », Bioorganic Chemistry, vol. 124, , p. 105823 (ISSN 1090-2120, PMID 35489272, DOI 10.1016/j.bioorg.2022.105823, lire en ligne, consulté le )
- Vivek S. Kumawat et Ginpreet Kaur, « Cannabinoid 2 receptor agonist and L-arginine combination attenuates diabetic cardiomyopathy in rats via NF-ĸβ inhibition », Canadian Journal of Physiology and Pharmacology, vol. 100, no 3, , p. 259–271 (ISSN 1205-7541, PMID 34860602, DOI 10.1139/cjpp-2021-0046, lire en ligne, consulté le )
- Anita Yovas et Stanely Mainzen Prince Ponnian, « β-Caryophyllene inhibits Fas- receptor and caspase-mediated apoptosis signaling pathway and endothelial dysfunction in experimental myocardial infarction », Journal of Biochemical and Molecular Toxicology, vol. 35, no 12, , e22907 (ISSN 1099-0461, PMID 34816538, DOI 10.1002/jbt.22907, lire en ligne, consulté le )
- Naoya Arizuka, Tomoaki Murakami et Kazuhiko Suzuki, « The effect of β-caryophyllene on nonalcoholic steatohepatitis », Journal of Toxicologic Pathology, vol. 30, no 4, , p. 263–273 (ISSN 0914-9198, PMID 29097836, PMCID 5660948, DOI 10.1293/tox.2017-0018, lire en ligne, consulté le )
- M. E. Mohamed, R. M. Abdelnaby et N. S. Younis, « β-caryophyllene ameliorates hepatic ischemia reperfusion-induced injury: the involvement of Keap1/Nrf2/HO 1/NQO 1 and TLR4/NF-κB/NLRP3 signaling pathways », European Review for Medical and Pharmacological Sciences, vol. 26, no 22, , p. 8551–8566 (ISSN 2284-0729, PMID 36459036, DOI 10.26355/eurrev_202211_30391, lire en ligne, consulté le )
- Hong-Ik Cho, Jeong-Min Hong, Joo-Wan Choi et Hyo-Sun Choi, « β-Caryophyllene alleviates D-galactosamine and lipopolysaccharide-induced hepatic injury through suppression of the TLR4 and RAGE signaling pathways », European Journal of Pharmacology, vol. 764, , p. 613–621 (ISSN 1879-0712, PMID 26254779, DOI 10.1016/j.ejphar.2015.08.001, lire en ligne, consulté le )
- Y. Tambe, H. Tsujiuchi, G. Honda et Y. Ikeshiro, « Gastric cytoprotection of the non-steroidal anti-inflammatory sesquiterpene, beta-caryophyllene », Planta Medica, vol. 62, no 5, , p. 469–470 (ISSN 0032-0943, PMID 9005452, DOI 10.1055/s-2006-957942, lire en ligne, consulté le )
- Da Hyun Jung, Mi Hee Park, Chul Jin Kim et Jin Young Lee, « Effect of β-caryophyllene from Cloves Extract on Helicobacter pylori Eradication in Mouse Model », Nutrients, vol. 12, no 4, , p. 1000 (ISSN 2072-6643, PMID 32260414, PMCID 7230661, DOI 10.3390/nu12041000, lire en ligne, consulté le )
- Keylla da Conceição Machado, Muhammad Torequl Islam, Eunüs S. Ali et Razina Rouf, « A systematic review on the neuroprotective perspectives of beta-caryophyllene », Phytotherapy research: PTR, vol. 32, no 12, , p. 2376–2388 (ISSN 1099-1573, PMID 30281175, DOI 10.1002/ptr.6199, lire en ligne, consulté le )
- Heng Li, Defen Wang, Yujie Chen et Minsheng Yang, « β-Caryophyllene inhibits high glucose-induced oxidative stress, inflammation and extracellular matrix accumulation in mesangial cells », International Immunopharmacology, vol. 84, , p. 106556 (ISSN 1878-1705, PMID 32416450, DOI 10.1016/j.intimp.2020.106556, lire en ligne, consulté le )
- Diogo Vilar da Fonsêca, Carlos da Silva Maia Bezerra Filho, Tamires Cardoso Lima et Reinaldo Nóbrega de Almeida, « Anticonvulsant Essential Oils and Their Relationship with Oxidative Stress in Epilepsy », Biomolecules, vol. 9, no 12, , p. 835 (ISSN 2218-273X, PMID 31817682, PMCID 6995584, DOI 10.3390/biom9120835, lire en ligne, consulté le )
- Vafa Baradaran Rahimi et Vahid Reza Askari, « A mechanistic review on immunomodulatory effects of selective type two cannabinoid receptor β-caryophyllene », BioFactors (Oxford, England), vol. 48, no 4, , p. 857–882 (ISSN 1872-8081, PMID 35648433, DOI 10.1002/biof.1869, lire en ligne, consulté le )
- Charu Sharma, Juma M. Al Kaabi, Syed M. Nurulain et Sameer N. Goyal, « Polypharmacological Properties and Therapeutic Potential of β-Caryophyllene: A Dietary Phytocannabinoid of Pharmaceutical Promise », Current Pharmaceutical Design, vol. 22, no 21, , p. 3237–3264 (ISSN 1873-4286, PMID 26965491, DOI 10.2174/1381612822666160311115226, lire en ligne, consulté le )
- Guifang Wang, Weibin Ma et Jingwei Du, « β-Caryophyllene (BCP) ameliorates MPP+ induced cytotoxicity », Biomedicine & Pharmacotherapy = Biomedecine & Pharmacotherapie, vol. 103, , p. 1086–1091 (ISSN 1950-6007, PMID 29710667, DOI 10.1016/j.biopha.2018.03.168, lire en ligne, consulté le )
- Vahid Reza Askari et Reza Shafiee-Nick, « The protective effects of β-caryophyllene on LPS-induced primary microglia M1/M2 imbalance: A mechanistic evaluation », Life Sciences, vol. 219, , p. 40–73 (ISSN 1879-0631, PMID 30620895, DOI 10.1016/j.lfs.2018.12.059, lire en ligne, consulté le )
- L. C. Assis, M. R. Straliotto, D. Engel et M. A. Hort, « β-Caryophyllene protects the C6 glioma cells against glutamate-induced excitotoxicity through the Nrf2 pathway », Neuroscience, vol. 279, , p. 220–231 (ISSN 1873-7544, PMID 25194788, DOI 10.1016/j.neuroscience.2014.08.043, lire en ligne, consulté le )
- Armenuhi Moghrovyan, Lilya Parseghyan, Gohar Sevoyan et Anna Darbinyan, « Antinociceptive, anti-inflammatory, and cytotoxic properties of Origanum vulgare essential oil, rich with β-caryophyllene and β-caryophyllene oxide », The Korean Journal of Pain, vol. 35, no 2, , p. 140–151 (ISSN 2005-9159, PMID 35354677, PMCID 8977206, DOI 10.3344/kjp.2022.35.2.140, lire en ligne, consulté le )
- Shamma Al Mansouri, Shreesh Ojha, Elyazia Al Maamari et Mouza Al Ameri, « The cannabinoid receptor 2 agonist, β-caryophyllene, reduced voluntary alcohol intake and attenuated ethanol-induced place preference and sensitivity in mice », Pharmacology, Biochemistry, and Behavior, vol. 124, , p. 260–268 (ISSN 1873-5177, PMID 24999220, DOI 10.1016/j.pbb.2014.06.025, lire en ligne, consulté le )
- Zoltan V. Varga, Csaba Matyas, Katalin Erdelyi et Resat Cinar, « β-Caryophyllene protects against alcoholic steatohepatitis by attenuating inflammation and metabolic dysregulation in mice », British Journal of Pharmacology, vol. 175, no 2, , p. 320–334 (ISSN 1476-5381, PMID 28107775, PMCID 5758392, DOI 10.1111/bph.13722, lire en ligne, consulté le )
- M. E. Flores-Soto, J. A. Corona-Angeles, A. R. Tejeda-Martinez et P. A. Flores-Guzman, « β-Caryophyllene exerts protective antioxidant effects through the activation of NQO1 in the MPTP model of Parkinson's disease », Neuroscience Letters, vol. 742, , p. 135534 (ISSN 1872-7972, PMID 33271195, DOI 10.1016/j.neulet.2020.135534, lire en ligne, consulté le )
- Lívia B. A. Fontes, Débora Dos S. Dias, Beatriz J. V. Aarestrup et Fernando M. Aarestrup, « β-Caryophyllene ameliorates the development of experimental autoimmune encephalomyelitis in C57BL/6 mice », Biomedicine & Pharmacotherapy = Biomedecine & Pharmacotherapie, vol. 91, , p. 257–264 (ISSN 1950-6007, PMID 28463791, DOI 10.1016/j.biopha.2017.04.092, lire en ligne, consulté le )
- Vahid Reza Askari, Vafa Baradaran Rahimi, Seyed Abbas Tabatabaee et Reza Shafiee-Nick, « Combination of Imipramine, a sphingomyelinase inhibitor, and β-caryophyllene improve their therapeutic effects on experimental autoimmune encephalomyelitis (EAE) », International Immunopharmacology, vol. 77, , p. 105923 (ISSN 1878-1705, PMID 31711937, DOI 10.1016/j.intimp.2019.105923, lire en ligne, consulté le )
- Ewa Galaj, Guo-Hua Bi, Allamar Moore et Kai Chen, « Beta-caryophyllene inhibits cocaine addiction-related behavior by activation of PPARα and PPARγ: repurposing a FDA-approved food additive for cocaine use disorder », Neuropsychopharmacology: Official Publication of the American College of Neuropsychopharmacology, vol. 46, no 4, , p. 860–870 (ISSN 1740-634X, PMID 33069159, PMCID 8026612, DOI 10.1038/s41386-020-00885-4, lire en ligne, consulté le )
- Xiang-Hu He, Ewa Galaj, Guo-Hua Bi et Yi He, « β-caryophyllene, an FDA-Approved Food Additive, Inhibits Methamphetamine-Taking and Methamphetamine-Seeking Behaviors Possibly via CB2 and Non-CB2 Receptor Mechanisms », Frontiers in Pharmacology, vol. 12, , p. 722476 (ISSN 1663-9812, PMID 34566647, PMCID 8458938, DOI 10.3389/fphar.2021.722476, lire en ligne, consulté le )
- Yi He, Ewa Galaj, Guo-Hua Bi et Xiao-Fei Wang, « β-Caryophyllene, a dietary terpenoid, inhibits nicotine taking and nicotine seeking in rodents », British Journal of Pharmacology, vol. 177, no 9, , p. 2058–2072 (ISSN 1476-5381, PMID 31883107, PMCID 7161544, DOI 10.1111/bph.14969, lire en ligne, consulté le )