Borazane
Le borazane est un composé chimique de formule BH3NH3. Il s'agit d'un solide incolore d'aspect cireux utilisé principalement pour stocker efficacement l'hydrogène pour les applications alternatives aux hydrocarbures.
| Borazane | |
| |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.170.890 |
| Propriétés chimiques | |
| Formule | BH3NH3 |
| Masse molaire[1] | 30,865 ± 0,008 g/mol H 19,59 %, B 35,03 %, N 45,38 %, |
| Propriétés physiques | |
| T° fusion | décomposition thermique dès 68 °C jusqu'à 97,61 °C |
| Masse volumique | 0,780 kg/m3 |
| Précautions | |
| Directive 67/548/EEC | |
 E |
|
| Unités du SI et CNTP, sauf indication contraire. | |
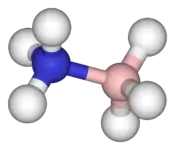
Propriétés et structure
Le borazane adopte une configuration moléculaire semblable à celle de l'éthane CH3-CH3, mais la comparaison ne va pas loin puisque l'éthane est gazeux à température ambiante tandis que le borazane est solide : le borazane est en effet une molécule très polaire. La longueur de la liaison B–N est de 158 pm, tandis que celles des liaisons B–H et N–H sont respectivement de 115 pm et 96 pm.
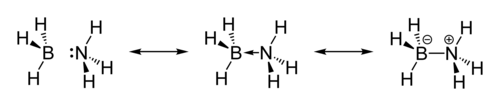
La structure du borazane a été élucidée par diffraction de neutrons. Elle indique une association étroite entre les centres NH et BH[2] - [3].
Préparation du borazane
La réaction du diborane avec l'ammoniac donne principalement le sel [(NH3)2BH2]+, (BH4)−, mais le borazane est le produit majoritaire à l'aide, par exemple, de tétrahydrofurane :
Réactions et utilisations
Le borazane a été proposé comme source d'hydrogène pour la propulsion automobile sans hydrocarbures car il libère de l'hydrogène H2 en polymérisant, sous l'effet de la chaleur, successivement en (BH2NH2)n et en (BHNH)n, et permet de libérer davantage d'hydrogène à température ambiante et par unité de volume que l'hydrogène liquéfié.
Il peut également servir de réactif lors de synthèses organiques en tant qu'alternative stable au diborane B2H6.
Un mélange de borazane et de lanthane, chauffé au laser sous haute pression, produit du décahydrure de lanthane LaH10, qui à 188 GPa est supraconducteur au-dessous de −13,5 °C[4] - [5].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) W.T. Klooster, T. F. Koetzle, P. E. M. Siegbahn, T. B. Richardson et R. H. Crabtree, « Study of the N-H...H-B Dihydrogen Bond Including the Crystal Structure of BH3NH3 by Neutron Diffraction », Journal of the American Chemical Society, vol. 121, , p. 6337-6343 (DOI 10.1021/ja9825332)
- (en) R. Boese, N. Niederprüm et D. Bläser, Molecules in Natural Science and Medicine, Chichester, England, E. Horwood, (ISBN 978-0135615980).
- Sean Bailly, « De la supraconductivité à température quasi ambiante », Pour la science, no 496, , p. 8.
- (en) Maddury Somayazulu, Muhtar Ahart, Ajay K. Mishra, Zachary M. Geballe, Maria Baldini et al., « Evidence for Superconductivity above 260 K in Lanthanum Superhydride at Megabar Pressures », Physical Review Letters, vol. 122, , article no 027001 (DOI 10.1103/PhysRevLett.122.027001).