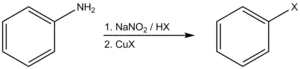Réaction de Sandmeyer
La réaction de Sandmeyer est une réaction chimique utilisée pour synthétiser des halogénures d'aryle à partir de sels d'aryldiazonium, en utilisant des sels de cuivre comme réactifs ou catalyseurs[1] - [2] - [3]. Cette réaction est un exemple de substitution aromatique radicalaire-nucléophile. Elle fournit une méthode par laquelle on peut effectuer des transformations uniques sur le benzène, telles que l'halogénation, la cyanation, la trifluorométhylation et l'hydroxylation.
La réaction a été découverte en 1884 par le chimiste suisse Traugott Sandmeyer, qui essayait alors de synthétiser le phénylacétylène à partir du chlorure de benzènediazonium et de l'acétylure de cuivre(I). Au lieu de cela, le principal produit qu'il isola fut le chlorobenzène[4].
De nos jours, on appelle « réaction de Sandmeyer » toute méthode de substitution d'un groupe amine aromatique via la préparation de son sel de diazonium suivie par son remplacement par un nucléophile en présence catalytique[note 1] de sels de cuivre(I).
Les réactions de Sandmeyer les plus communément utilisées sont la chloration, la bromation, la cyanation, et l'hydroxylation, utilisant respectivement CuCl, CuBr, CuCN, et Cu2O, comme réactif. Plus récemment a été développée la trifluorométhylation de sels de diazonium, une réaction qualifiée de « type Sandmeyer ». Les sels de diazonium réagissent aussi notamment avec les boronates, les iodures, les thiols, l'eau et l'acide hypophosphoreux[5], et la fluoration peut être conduite en utilisant des anions tétrafluoroborate (dans ce dernier cas, la réaction est alors appelée réaction de Balz-Schiemann). Cependant, comme ces réactions n'ont pas besoin de catalyseur métallique, on ne les qualifie pas en général de « réaction de Sandmeyer ». De multiples variantes utilisant d'autres sels et d'autres métaux de transition – notamment sels de cuivre(II), fer(III) et cobalt(III) – ont été développées[6].
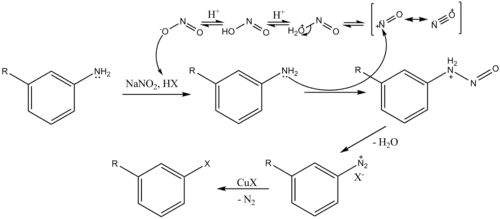
Mécanisme réactionnel
Dans le mécanisme ci-dessous, l'amine aromatique est diazotée par l'acide nitreux formé in situ par l'action du nitrite de sodium en présence d'un excès d'acide pour former le sel de diazonium, qui sera décomposé pour donner, en fonction des réactifs présents, l'halogénure d'aryle ou le nitrile voulu[7] - [8].
Variantes
Cette réaction est une substitution nucléophile aromatique (SNAr), elle se fait par la dégradation d'un sel de diazonium. Les produits de la réaction sont[9] :
- en présence de chlorure de cuivre(I) (CuCl) et d'acide chlorhydrique, la formation d'un chlorobenzène ;
- en présence de bromure de cuivre(I) (CuBr) et d'acide bromhydrique, la formation d'un bromobenzène ;
- en présence d'iodure de sodium ou de potassium sans catalyseur, la formation d'un iodobenzène [10].
- en présence de cyanure de cuivre(I) (CuCN), la formation d'un benzonitrile [11].
Quel que soit l'homologue, il y aura toujours un dégagement de diazote gazeux.
Il existe toute une série de réactions apparentées à celle de Sandmeyer qui permettent de substituer un groupe amino par un autre sur un noyau aromatique via un diazonium. Certaines nécessitent un catalyseur à base de cuivre, d'autres non. Quelques exemples de groupes:
- Nitro, le tétrafluoroborate du diazonium est traité par un nitrite en présence de poudre de cuivre comme catalyseur [12]
- Acide sulfinique, par l'action du dioxyde de soufre sur le diazonium en présence de sulfate de fer (II) et de poudre de cuivre [13]
- Azide, par l'action de l'azoture de sodium sur le diazonium sans catalyseur [14].
- Acide phénylarsonique, le diazonium est ajouté à une solution d'arsénite de sodium en présence de sulfate de cuivre [15]
- Mercaptan. Il existe différentes variantes où le diazonium est traité par un xanthate, un sulfure, un disulfure suivi d'une réduction [16].
- Hydrogène. Cette réaction est appelée désamination de Griess, le diazonium est réduit par de l'éthanol [17] ou de l'acide hypophosphoreux.
- Hydroxyde (phénol). Le diazonium est ajouté à de l'eau chaude en présence d'acide sulfurique [18].
La réaction de Gomberg-Bachmann [19] est également un cas de figure analogue, où l'électrophile est un autre cycle aromatique, formant un biphényle. La réaction de Schiemann permet d'introduire un fluor et se distingue de par la particularité de la procédure de synthèse.
Réaction de Schiemann
Pour l'homologue fluor, la réaction utilisée sera la réaction de Balz-Schiemann[20], qui est également une décomposition de sel de diazonium, avec la particularité de passer par le tétrafluoroborate du diazonium, un sel peu soluble et relativement stable, qui se laisse décomposer thermiquement pour donner un fluorobenzène, avec dégagement gazeux simultané d'azote et de trifluorure de bore.
Notes
- Du fait du faible coût des sels de cuivre, une quantité stœchiométrique est souvent employée pour une meilleure réactivité, même lorsque la catalyse est possible.
2.↑ cette réaction est une étape clé de la synthèse de la lévothyroxine (Chalmers et Hems, 1949) qui est le principe actif des médicaments contre l'hypothyroïdie comme le lévothyrox"
Références
- (de) T. Sandmeyer, « Ueber die Ersetzung der Amidgruppe durch Chlor in den aromatischen Substanzen », Ber. Dtsch. Chem. Ges., vol. 17, no 2, , p. 1633–1635 (ISSN 0365-9496, DOI 10.1002/cber.18840170219, lire en ligne).
- (de) T. Sandmeyer, « Ueber die Ersetzung der Amid-gruppe durch Chlor, Brom und Cyan in den aromatischen Substanzen », Ber. Dtsch. Chem. Ges., vol. 17, no 2, , p. 2650–2653 (ISSN 0365-9496, DOI 10.1002/cber.188401702202, lire en ligne).
- Ludwig Gattermann, « Untersuchungen über Diazoverbindungen », Berichte der Deutschen Chemischen Gesellschaft, vol. 23, no 1, , p. 1218–1228 (DOI 10.1002/cber.189002301199, lire en ligne)
- Herbert H. Hodgson, « The Sandmeyer Reaction », Chemical Reviews, vol. 40, no 2, , p. 251–277 (ISSN 0009-2665, PMID 20291034, DOI 10.1021/cr60126a003)
- (en) Zerong Wang, Comprehensive Organic Name Reactions and Reagents, John Wiley & Sons, Inc., , 2471–2475 p. (ISBN 9780470638859), « Sandmeyer Reaction »
- M. P. Doyle, B. Siegfried and J. F. Dellaria, « Alkyl nitrite-metal halide deamination reactions. 2. Substitutive deamination of arylamines by alkyl nitrites and copper(II) halides. A direct and remarkably efficient conversion of arylamines to aryl halides », J. Org. Chem., vol. 42, no 14, , p. 2426–2431 (DOI 10.1021/jo00434a017)
- (en) J. K. Kochi, « The Mechanism of the Sandmeyer and Meerwein Reactions », J. Am. Chem. Soc., vol. 79, no 11, , p. 2942–2948 (ISSN 0002-7863, DOI 10.1021/ja01568a066).
- (en) H. H. Hodgson, « The Sandmeyer Reaction », Chem. Rev., vol. 40, no 2, , p. 251–277 (ISSN 0009-2665, DOI 10.1021/cr60126a003).
- « Quelques réactions de base - Sandmeyer », sur le site Abécédaire de Chimie Organique (consulté le ).
- Org. Syn. CV2 p351, 1943, http://www.orgsyn.org/Content/pdfs/procedures/CV2P0351.pdf
- Org. Syn. CV1 p514, 1925, http://www.orgsyn.org/Content/pdfs/procedures/CV1P0514.pdf
- E.B. Starkey "p-Dinitrobenzene" Org. Syn. CV2 p225, 1925, http://www.orgsyn.org/Content/pdfs/procedures/CV2P0225.pdf
- G. Wittig, R.W. Hoffmann "1,2,3-Benzothiadiazole-1,1-dioxyde" Org. Syn. CV5 p60, 1973, http://www.orgsyn.org/Content/pdfs/procedures/CV5P0060.pdf
- G. David Mendenhall, Peter A.S. Smith "2-Nitrocarbazole" Org. Syn. CV5 p829, 1973, http://www.orgsyn.org/Content/pdfs/procedures/CV5P0829.pdf
- R.H. Bullard, J.B. Dickey "Phenylarsonic acid" Org. Syn. CV2 p494, 1941, http://www.orgsyn.org/Content/pdfs/procedures/CV2P0494.pdf
- C.F.H Allen, D.D. MacKay "Thiosalycilic acid" Org. Syn. CV2 p580, 1943, http://www.orgsyn.org/Content/pdfs/procedures/CV2P0580.pdf
- L.A. Bigelow, J.R. Johnson, L.T. Sandborn "m-Bromotoluene" Org. Syn. CV1 p133, 1926, http://www.orgsyn.org/Content/pdfs/procedures/CV1P0133.pdf
- H.E. Ungnade, E.F. Orwoll "3-Bromo-4-hydroxytoluene" Org. Syn. CV3 p130, 1955, http://www.orgsyn.org/Content/pdfs/procedures/CV3P0130.pdf
- (en)Gomberg–Bachmann reaction
- (de) G. Balz et G. Schiemann, « Über aromatische Fluorverbindungen, I.: Ein neues Verfahren zu ihrer Darstellung », Ber. Dtsch. Chem. Ges., vol. 60, no 5, , p. 1186–1190 (ISSN 0365-947X, DOI 10.1002/cber.19270600539).
Liens externes
- (en) « Sandmeyer Reaction », sur le site Organic Chemistry Portal (consulté le ).
- (en) « Balz-Schiemann Reaction », sur le site Organic Chemistry Portal (consulté le ).