Pirfénidone
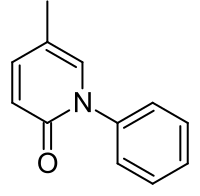
La pirfénidone (5-méthyl-1-phényl-2-(1H)-pyridone) est un principe actif de type immunosuppresseur avec des propriétés antifibrotiques et anti-inflammatoires utilisé pour le traitement de la fibrose pulmonaire idiopathique (FPI).
| Pirfénidone | |
| |
| Pirfénidone. | |
| Identification | |
|---|---|
| Nom UICPA | 5-méthyl-1-phénylpyridine-2-one |
| Synonymes |
Esbriet, Pirespa, Etuary |
| No CAS | |
| No ECHA | 100.150.129 |
| Code ATC | |
| PubChem | 40632 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C12H11NO |
| Masse molaire[1] | 185,221 8 ± 0,010 9 g/mol C 77,81 %, H 5,99 %, N 7,56 %, O 8,64 %, |
| Données pharmacocinétiques | |
| Liaison protéique | 50–58 % |
| Métabolisme | Hépatique (70–80% par CYP1A2 ; moindre contribution de CYP2C9, CYP2C19, CYP2D6 et de CYP2E1) |
| Demi-vie d’élim. | 2,4 h |
| Excrétion |
Urine (80 %) |
| Considérations thérapeutiques | |
| Voie d’administration | oral |
| Unités du SI et CNTP, sauf indication contraire. | |
Commercialisation
Elle est commercialisée sous le nom d’Esbriet en Amérique du Nord et en Europe et sous celui de Pirespa au Japon et en Corée du Sud.
Mode d'action
Elle agit par inhibition de la synthèse de HSP47 induit par le facteur de croissance de transformation TGF-béta[2] et de la synthèse du facteur de nécrose tumorale (TNF-alpha)[3].
| pirfénidone | |
| Informations générales | |
|---|---|
| Princeps |
|
| Classe | Antinéoplasiques et immunomodulateurs, autres immunosuppresseurs, ATC code L04AX05 |
| Forme | gélules ou comprimés dosés à 267 mg, comprimés dosés à 801 mg |
| Administration | per os |
| Laboratoire | InterMune, Roche |
| Identification | |
| No CAS | |
| No ECHA | 100.150.129 |
| Code ATC | L04AX05 |
| DrugBank | 04951 |
La pirfénidone inhibe le facteur de croissance basique des fibroblastes, le facteur de croissance dérivé des plaquettes (en) et la prolifération cellulaire stimulée par le facteur de croissance transformant β (TGF-ß (en)).
Dans les fibromes utérins, la pirfénidone inhibe la prolifération cellulaire et diminue de manière significative les niveaux d'ARN messager codant le collagène de type I et du collagène de type III[4].
Indications
Le , en France, la Haute Autorité de Santé (HAS) estimait que le service médical rendu (SMR) par la pirfénidone est faible et uniquement chez les patients au diagnostic clinique et radiologique confirmé de FPI et avec les critères fonctionnels respiratoires suivants : capacité vitale forcée (CVF) supérieure ou égale à 50 % et diffusion libre du CO (DLCo) supérieure ou égale à 35 %[5].
Le , InterMune Inc., l'entreprise pharmaceutique qui commercialise le médicament, publie les résultats de l'étude de phase III ASCEND. Celle-ci montre que « comparativement au placebo, la pirfénidone a diminué la progression de la maladie, comme en ont témoigné la fonction pulmonaire, la tolérance à l’exercice et la survie sans progression chez les patients atteints de FPI. Le traitement a objectivé un profil d’effets indésirables acceptable et une diminution de la mortalité[6]. »
Depuis 2015, la pirfénidone est en phase IV.
Effets secondaires
Les effets indésirables rapportés sont[5] :
- fatigue ;
- myalgie, arthralgie ;
- réaction de photosensibilisation, éruption cutanée ;
- dyspepsie, nausées, diarrhées ;
- reflux gastro-œsophagien ;
- augmentation de l'alanine aminotransférase, augmentation de l'aspartate aminotransférase, augmentation de la gamma glutamyl transpeptidase ;
- infection des voies respiratoires supérieures, infection des voies urinaires ;
- perte de poids, anorexie, perte d'appétit ;
- insomnie ;
- vertiges, maux de tête, somnolence, dysgueusie ;
- bouffées de chaleur.
Le , l'Agence nationale de sécurité du médicament et des produits de santé (ANSM) publie une mise à jour importante de sécurité et de nouvelles recommandations concernant les risques d’atteintes hépatiques d’origine médicamenteuse avec Esbriet (pirfénidone)[7]. Cet article précise que des cas graves de lésions hépatiques d’origine médicamenteuse ont été récemment signalés avec la pirfénidone, dont certains d'issue fatale.
Un bilan hépatique (ALAT, ASAT, bilirubine) doit être réalisé avant l’initiation d’un traitement par pirfénidone. Par la suite, un bilan doit être réalisé mensuellement pendant les 6 premiers mois de traitement puis tous les 3 mois pendant toute la durée du traitement[7].
Un examen clinique et un bilan de la fonction hépatique doivent être rapidement réalisés chez les patients présentant des symptômes évoquant une atteinte hépatique d’origine médicamenteuse, tel que fatigue, anorexie, gêne abdominale supérieure droite, urines foncées ou ictère[7].
Une augmentation des transaminases peut nécessiter une réduction de dose, une interruption de traitement ou un arrêt définitif du traitement par pirfénidone. En cas d’augmentation significative des aminotransférases hépatiques avec une hyperbilirubinémie ou en cas de signes et symptômes cliniques d’atteinte hépatique d’origine médicamenteuse, le traitement par pirfénidone doit être arrêté définitivement[7].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Nakayama S., Mukae H., Sakamoto N., Kakugawa T., Yoshioka S., Soda H., Oku H., Urata Y., Kondo T., Kubota H., Nagata K. (ja), Kohno S., « Pirfenidone inhibits the expression of HSP47 in TGF-beta1-stimulated human lung fibroblasts », Life sciences (en), vol. 82, nos 3-4, , p. 210-217 (PMID 18093617, lire en ligne, consulté le ).
- (en) Grattendick K.J., Nakashima J.M., Feng L., Giri S.N., Margolin S.B., « Effects of three anti-TNF-alpha drugs: etanercept, infliximab and pirfenidone on release of TNF-alpha in medium and TNF-alpha associated with the cell in vitro », International Immunopharmacology, vol. 8, no 5, , p. 679-687 (PMID 18387510, lire en ligne, consulté le ).
- (en) Byung-Seok Lee, Solomon B. Margolin et Romana A. Nowak, « Pirfenidone: A Novel Pharmacological Agent That Inhibits Leiomyoma Cell Proliferation and Collagen Production », The Journal of Clinical Endocrinology & Metabolism, vol. 83, no 1, , p. 219–223 (ISSN 0021-972X, DOI 10.1210/jcem.83.1.4503, lire en ligne, consulté le ).
- Haute Autorité de Santé, « Progrès thérapeutique mineur dans la fibrose pulmonaire idiopathique légère à modérée », (consulté le ).
- InterMune, Inc., « Résultats de l’essai de phase III ASCEND sur la pirfénidone dans la fibrose pulmonaire idiopathique présentés au congrès de l’American Thoracic Society et publiés dans le New England Journal of Medicine » [PDF], (consulté le ).
- « Mise à jour Importante de sécurité et nouvelles recommandations concernant les risques d’atteintes hépatiques d’origine médicamenteuse - Lettre aux professionnels de santé », sur ansm.sante.fr, Agence nationale de sécurité du médicament, (consulté le ).
Voir aussi
Bibliographie
- Revue Prescrire, « Fibrose pulmonaire idiopathique : éviter la pirfénidone », (consulté le ).
Articles connexes
Liens externes
- Page spécifique dans la base de données sur les produits pharmaceutiques (Canada)
- Compendium suisse des médicaments : spécialités contenant Pirfénidone
- Page spécifique sur le Répertoire Commenté des Médicaments, par le Centre belge d'information pharmacothérapeutique
- Page spécifique sur le Vidal.fr