Phosphure de titane(III)
Le phosphure de titane(III) est un composé chimique de formule TiP. Il s'agit d'une poudre gris anthracite d'aspect métallique et thermiquement très stable, peu attaquée par les acides même à chaud. Il cristallise dans le système hexagonal selon le groupe d'espace P63/mmc (no 194) avec pour paramètres a = 348,7 pm et c = 1 165 pm[1].
| Phosphure de titane(III) | |||
| |||
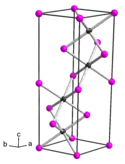
| __ Ti __ P Structure cristalline du phosphure de titane(III) |
|||
| Identification | |||
|---|---|---|---|
| Nom UICPA | phosphanylidynetitane | ||
| Nom systématique | phosphure de titane(III) | ||
| Synonymes |
phosphure de titane |
||
| No CAS | |||
| No ECHA | 100.031.680 | ||
| No CE | 234-862-6 | ||
| PubChem | 82856 | ||
| SMILES | |||
| InChI | |||
| Apparence | solide gris anthracite[1] | ||
| Propriétés chimiques | |||
| Formule | PTi [Isomères] |
||
| Masse molaire[2] | 78,841 ± 0,001 g/mol P 39,29 %, Ti 60,71 %, |
||
| Propriétés physiques | |||
| T° fusion | 1 860 °C[1] | ||
| Masse volumique | 3,94 g/cm3[1] | ||
| Précautions | |||
| SGH[3] | |||
  Attention |
|||
| Transport[3] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
Il peut être obtenu directement à partir des éléments par synthèse sous pression :
Il est également possible de le produire en faisant réagir de la phosphine PH3 avec du tétrachlorure de titane TiCl4 à 750 °C. La réaction à une température de 800 à 1 000 °C d'une poudre finement divisée d'hydrure de titane TiH2 avec un mélange PH3 / H2 permet d'obtenir des phosphures à faible teneur en phosphore TiP0,1-0,6[1].
Le phosphure de titane(III) peut être utilisé comme catalyseur en synthèse organique[4].
Notes et références
- (de) Georg Brauer, en collaboration avec Marianne Baudler, Handbuch der Präparativen Anorganischen Chemie, 3e éd. révisée, vol. 2, Ferdinand Enke, Stuttgart, 1978, p. 1383. (ISBN 3-432-87813-3)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Titanium Phosphide Sputtering Target », sur https://www.americanelements.com/, American Elements (en) (consulté le ).
- (en) Dale L. Perry, Handbook of Inorganic Compounds, 2e éd., Taylor & Francis, 2011, p. 488. (ISBN 1-4398-1462-7)
