Oxime de cyclohexanone
L'oxime de cyclohexanone est un composé organique de formule chimique C5H10CNOH. Cette oxime se présente sous la forme d'un solide blanc formé de cristaux incolores. Elle intervient dans la production du nylon 6. On peut l'obtenir par condensation de cyclohexanone C5H10CO et d'hydroxylamine NH2OH[4] :
| Oxime de cyclohexanone | |
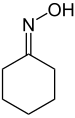
| |
| Structure de l'oxime de cyclohexanone | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.002.613 |
| No CE | 202-874-0 |
| No RTECS | GW1925000 |
| PubChem | 7517 |
| SMILES | |
| InChI | |
| Apparence | poudre solide blanche inflammable[1] |
| Propriétés chimiques | |
| Formule | C6H11NO [Isomères] |
| Masse molaire[2] | 113,157 6 ± 0,006 1 g/mol C 63,68 %, H 9,8 %, N 12,38 %, O 14,14 %, |
| Propriétés physiques | |
| T° fusion | 90 °C[1] |
| T° ébullition | 206 à 210 °C[1] |
| Solubilité | 16 g/L[1] |
| Masse volumique | 0,98 g/cm3[1] |
| Point d’éclair | 94 °C[1] |
| Précautions | |
| SGH[1] - [3] | |
   Danger |
|
| NFPA 704[3] | |
| Transport[1] | |
| Unités du SI et CNTP, sauf indication contraire. | |
Un autre procédé industriel fait réagir le cyclohexane C6H12 avec le chlorure de nitrosyle NOCl, ce qui est une réaction radicalaire, méthode économiquement intéressante car le cyclohexane est bien meilleur marché que la cyclohexanone.
La principale réaction impliquant l'oxime de cyclohexanone est le réarrangement de Beckmann donnant l'ε-caprolactame :
La réaction est catalysée par l'acide sulfurique H2SO4, mais les procédés industriels emploient des acides solides[5].
Notes et références
- Entrée « Cyclohexanone oxime » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 2 octobre 2021 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Fiche du composé Cyclohexanone oxime, 97% », sur Alfa Aesar (consulté le ).
- (en) J. C. Eck et C. S. Marvel, « ε-Benzoylaminocaproic Acid », Organic Syntheses, vol. 19, , p. 20 (DOI 10.15227/orgsyn.019.0020, lire en ligne)
- (en) Avelino Corma et Hermenegildo Garcia, « Organic reactions catalyzed over solid acids », Catalysis Today, vol. 38, no 3, , p. 257-308 (DOI 10.1016/S0920-5861(97)81500-1, lire en ligne)


