Indice de saponification
L'indice de saponification (Is) d'un lipide est la masse d'hydroxyde de potassium KOH, exprimée en milligrammes, nécessaire pour neutraliser les acides gras libres et saponifier les acides gras estérifiés contenus dans un gramme de matière grasse.
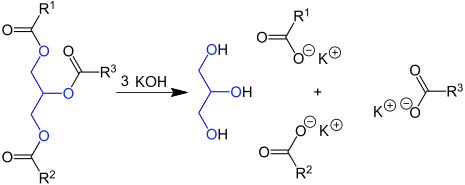
L'indice de saponification d'une matière grasse est obtenu par une expérience faite en laboratoire. Cet indice présente le grand intérêt de permettre l'utilisation d'une matière grasse sans en connaître précisément la composition, toujours complexe et variable dans le cas des matières grasses d'origine naturelle. C'est le cas en savonnerie.
Un indice de saponification théorique peut être calculé avec la formule suivante :
- avec :
- 56 (g/mol), la masse molaire de KOH (matière nécessaire pour neutraliser les molécules d'acides gras libres et saponifier les molécules d'acides gras estérifiées) ;
- M, la masse molaire de l'acide gras étudié.
Si le corps gras analysé est un triglycéride pur, l'indice de saponification permet de connaître sa masse molaire (donc sa composition moléculaire et éventuellement sa structure).
Si le corps gras analysé contient un mélange de glycérides et d'acides gras libres, la mesure de l'indice de saponification ne permet pas de connaître directement sa masse molaire. Il faut d'abord déterminer l'indice d'acide et en déduire l'indice d'ester.
Cet indice est déterminé à chaud (contrairement à l'indice d'acide).
Le calcul d'un indice théorique de saponification n'est pas d'un très grand intérêt car, hormis en laboratoire avec des matières grasses pures de composition connue, l'expérience montre que dans la majorité des cas l'indice théorique calculé diffère de l'indice vrai mesuré.
L'indice de saponification peut être déterminé suivant la norme NF EN ISO 3657[1].
Exemples
Indice de saponification par la soude
Si la saponification est réalisée avec de la soude (hydroxyde de sodium de formule NaOH), il faut remplacer la masse molaire de KOH (56,1 g/mol) par celle de NaOH (40,0 g/mol), soit la relation :
- .
Soit :
- .
Sources
- Firestone, D., Physical and Chemical Characteristics of Oils, Fats, and Waxes, 2e éd., AOCS Press, Urbana, IL, 2006.
- Gunstone, F.D., Harwood, J.L. et Dijkstra, A.J., éds., The Lipid Handbook, 3e éd., CRC Press, Boca Raton, FL, 2006.
- Dawson, R.M.C., Elliott, D.C., Elliott, W.H. et Jones, K.M., Data for Biochemical Research, 3e éd., Clarendon Press, Oxford, 1986.
- Altman, P.L. et Dittmer, D.S., éds., Biology Data Book, 2e éd., vol. 1, Federation of American Societies for Experimental Biology, Bethesda, MD, 1972.
- Baud, Paul, Traité de chimie industrielle, 4e éd., t. III, Industries organiques, Masson et Cie Éditeur, 1951.


