Favipiravir
Le favipiravir, ou T-705, est une pyrazine organofluorée produite par la société japonaise Toyama Chemical et utilisée comme antiviral contre les virus à ARN, notamment les orthomyxovirus (dont les différents virus de la grippe), le virus du Nil occidental, le virus de la fièvre jaune, le virus de la fièvre aphteuse (en) ainsi que d'autres flavivirus, arénavirus, bunyavirus, alphavirus[2], et peut être contre le coronavirus SARS-CoV-2 responsable de la pandémie de maladie à coronavirus de 2019-2020[3]. Autorisé sur le marché en janvier 2014, le Favipiravir est autorisé au Japon pour lutter contre les pandémies grippales en tant que médicament essentiel. Fujifilm Toyama Chemical a autorisé Zhejiang HISUN Pharmaceutical Co., Ltd. à produire ce médicament en République populaire de Chine, et en 2019, après l’expiration du brevet en Chine continentale, d’autres fabricants ont également commencé à produire ce médicament (médicament générique).
| Favipiravir | |
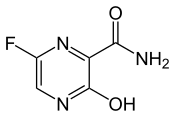 Structure du favipiravir |
|
| Identification | |
|---|---|
| Nom UICPA | 5-fluoro-2-oxo-1H-pyrazine-3-carboxamide |
| No CAS | |
| PubChem | 492405 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C5H4FN3O2 [Isomères] |
| Masse molaire[1] | 157,102 6 ± 0,005 5 g/mol C 38,23 %, H 2,57 %, F 12,09 %, N 26,75 %, O 20,37 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Caractéristiques
Le favipiravir, ou T-705, est une pyrazine organofluorée.
On pense qu'il agit par inhibition sélective de l'ARN polymérase ARN-dépendante de ces virus, car il n'interagit ni avec la transcription de l'ADN en ARN ni avec la réplication de l'ADN dans les cellules de mammifères[2].
Législation
En 2014, le Japon approuve le Favipiravir pour le traitement de souches virales résistantes aux antiviraux existants[4]. La société Toyama Chemical espérait initialement en faire un médicament qui pourrait concurrencer le Tamiflu. Cependant, les expériences sur animaux ont révélé son potentiel tératogène sur le fœtus. L'accord pour la production par le Ministère de la Santé du Japon a alors été considérablement retardé et limité aux cas d'urgence au Japon[5].
En mars 2015 aux États-Unis, la Food and Drug Administration achève son étude clinique de phase III concernant la sécurité et l'efficacité du Favipiravir dans le traitement de la grippe[6].
En mars 2015 en Chine, l'antiviral est approuvé sous le nom de Favilavir, également pour le traitement de la grippe. En février 2020, l'agrément est étendu pour des essais cliniques concernant le traitement du COVID-19, à la suite de résultats prometteurs dans le traitement de cette maladie et avec des effets secondaires minimes. Le médicament générique est fabriqué en Chine par la Zhejiang Hisun Pharmaceutical Company[7].
Le 22 mars 2020, l'Italie approuve l'usage expérimental du Favipiravir dans le traitement contre le COVID-19. Des essais cliniques démarrent alors dans les trois régions les plus affectées par l'épidémie : la Lombardie, la Vénétie et l'Émilie-Romagne[8]. Cependant, l'Agence Italienne de Pharmacie prend la peine de prévenir la population que les preuves de son efficacité dans ce cas sont encore rares et préliminaires[9].
Le 30 mai 2020 Russe, Le Ministère russe de la santé a approuvé une version générique de favipiravir nommée Avifavir.
Usages médicaux
Deux études publiées au printemps 2014 ont indiqué que cette molécule avait été testée avec succès contre la maladie à virus Ebola sur des souris, et s'était montrée efficace même lorsqu'elle était administrée six jours après l'exposition de ces animaux au virus[10] - [11].
Un essai clinique a été lancé en Guinée le 17 décembre 2014 pour tester son efficacité sur l'homme[12].
En mars 2020, alors que sévit une pandémie de COVID-19, l'OMS envisage d'inclure le favipiravir dans son essai clinique mondial, appelé Solidarity, pour évaluer son efficacité contre le SARS-CoV-2 chez l'humain[13], alors qu'au même moment deux études menées à Shenzhen et Wuhan en Chine donnent des premiers résultats favorables en ce sens. Il y a néanmoins des contre-indications concernant les femmes enceintes du fait de possibles malformations du fœtus[14]. Il semble également fonctionner moins bien lorsque le virus s'est déjà multiplié selon le ministère japonais de la Santé[15].
Un essai de phase 2 en double aveugle, randomisé, contrôlé par placebo ne supporte pas l'utilisation du favipiravir aux doses couramment utilisées, chez les patients ambulatoires atteints de COVID-19 non compliqué[16].
Une revue systématique et une méta-analyse d'essais contrôlés randomisés sur un traitement à base de favipiravir n'ont pas rapporté de bénéfice supplémentaire significatif pour les patients atteints de COVID-19[17].
Effets secondaires
Il existe des preuves que l'utilisation pendant la grossesse peut être nocive pour le bébé[18]. Des effets tératogènes et embryotoxiques ont été mis en évidence sur quatre espèces animales[18] - [19].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Fujifilm décolle à Tokyo, l'un de ses médicaments efficace contre le Covid-19 selon Pékin », Le Figaro, (lire en ligne, consulté le ).
- (en) Frederick Hayden et Nahoko Shindo, « Influenza virus polymerase inhibitors in clinical development », Current Opinion in Infectious Diseases, vol. 32, no 2, , p. 176-186 (PMID 30724789, PMCID 6416007, DOI 10.1097/QCO.0000000000000532, lire en ligne, consulté le ).
- (ja) « 条件付き承認で普及に足かせ富山化学インフル薬の“無念” », Diamond Online, (lire en ligne, consulté le ).
- (en) « Phase 3 Efficacy and Safety Study of Favipiravir for Treatment of Uncomplicated Influenza in Adults - T705US316 », sur clinicaltrials.gov (consulté le ).
- (en) Zhang Yangfei, « Potential coronavirus drug approved for marketing », China Daily, (lire en ligne, consulté le ).
- (it) Giuseppe Pietrobelli, « Coronavirus, il Veneto sperimenta l’antivirale giapponese Favipiravir. Ma l’Aifa: “Ci sono scarse evidenze scientifiche su efficacia” », il Fatto Quotidiano, (lire en ligne, consulté le ).
- (it) « AIFA precisa, uso favipiravir per COVID-19 non autorizzato in Europa e USA, scarse evidenze scientifiche sull’efficacia », sur Agenzia italiana del farmaco, (consulté le ).
- « Guinée : Essai clinique à Guéckédou du médicament expérimental, « Favipiravir »(MSF) », sur Intellivoire.net, (consulté le )
- « COVID 19 : un essai européen et un essai mondial pour évaluer plusieurs stratégies thérapeutiques », sur VIDAL (consulté le )
- « Avigan, un traitement japonais efficace contre le coronavirus, selon la Chine », CNews, (lire en ligne, consulté le ).
- « Les bons résultats d'un antigrippal japonais pour lutter contre le Covid-19 », L'Indépendant, (lire en ligne, consulté le ).
- Marisa Holubar, Aruna Subramanian, Natasha Purington et Haley Hedlin, « Favipiravir for Treatment of Outpatients With Asymptomatic or Uncomplicated Coronavirus Disease 2019: A Double-Blind, Randomized, Placebo-Controlled, Phase 2 Trial », Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, vol. 75, no 11, , p. 1883–1892 (ISSN 1537-6591, PMID 35446944, PMCID 9047233, DOI 10.1093/cid/ciac312, lire en ligne, consulté le )
- Shao-Huan Lan, Chih-Cheng Lai, Shen-Peng Chang et Li-Chin Lu, « Favipiravir-based treatment for outcomes of patients with COVID-19: a systematic review and meta-analysis of randomized controlled trials », Expert Review of Clinical Pharmacology, vol. 15, no 6, , p. 759–766 (ISSN 1751-2441, PMID 35579014, DOI 10.1080/17512433.2022.2078701, lire en ligne, consulté le )
- Kimiyasu Shiraki et Tohru Daikoku, « Favipiravir, an anti-influenza drug against life-threatening RNA virus infections », Pharmacology & Therapeutics, vol. 209, , p. 107512 (ISSN 1879-016X, PMID 32097670, PMCID 7102570, DOI 10.1016/j.pharmthera.2020.107512, lire en ligne, consulté le )
- Victoria Pilkington, Toby Pepperrell et Andrew Hill, « A review of the safety of favipiravir - a potential treatment in the COVID-19 pandemic? », Journal of Virus Eradication, vol. 6, no 2, , p. 45–51 (ISSN 2055-6640, PMID 32405421, PMCID 7331506, DOI 10.1016/S2055-6640(20)30016-9, lire en ligne, consulté le )
Liens externes
- « Favipiravir », sur Drug Information Portal, U.S. National Library of Medicine
- « Avifavir », sur Référence de drogue russe., Medum.ru