Disulfure de fer
Le disulfure de fer est un composé chimique de formule FeS2, constitué du cation de fer Fe2+ et de l'anion disulfure S22−. Il se présente sous la forme d'un solide combustible cristallisé inodore, pratiquement insoluble dans l'eau, ayant la couleur du laiton. Il constitue deux minéraux, la pyrite et la marcassite.
| Disulfure de fer | |
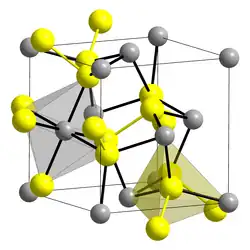 __ Fe2+ __ __ S22− Maille cristalline du disulfure de fer |
|
| Identification | |
|---|---|
| Nom UICPA | disulfure de fer(II) |
| Synonymes | |
| No CAS | |
| No ECHA | 100.031.903 |
| No CE | 215-167-7 |
| PubChem | 123110 |
| SMILES | |
| InChI | |
| Apparence | solide cristallisé inodore couleur laiton |
| Propriétés chimiques | |
| Formule | FeS2 [Isomères] |
| Masse molaire[1] | 119,975 ± 0,012 g/mol Fe 46,55 %, S 53,45 %, |
| Propriétés physiques | |
| Masse volumique | 5,0 à 5,2 g/cm3[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
Il peut être obtenu en faisant réagir du sulfure de fer FeS avec du soufre élémentaire :
Il peut également être obtenu en faisant passer du sulfure d'hydrogène H2S sur de l'oxyde de fer(III) Fe2O3 porté au rouge :
Par chauffage, le disulfure de fer libère son soufre et brûle en libérant du dioxyde de soufre SO2 et de l'oxyde de fer(III) Fe2O3 :
Il était autrefois largement utilisé pour la production d'acide sulfurique H2SO4, et sert aujourd'hui essentiellement à réaliser des accumulateurs lithium-ion dits « lithium-sulfure de fer », dont la cathode est constituée de disulfure de fer FeS2.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Iron disulfide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 2 mars 2013 (JavaScript nécessaire)


