Dibenzothiophène
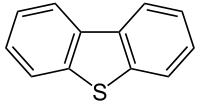
Le dibenzothiophène (DBT) est un composé aromatique tricyclique, constitué de deux cycles de benzène fusionnés avec un cycle de thiophène central.
| Dibenzothiophène | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | dibenzothiophène | |
| Synonymes |
DBT, sulfure de diphénylène |
|
| No CAS | ||
| No ECHA | 100.004.613 | |
| No CE | 205-072-9 | |
| SMILES | ||
| InChI | ||
| Apparence | Cristal incolore | |
| Propriétés chimiques | ||
| Formule | C12H8S [Isomères] |
|
| Masse molaire[1] | 184,257 ± 0,015 g/mol C 78,22 %, H 4,38 %, S 17,4 %, |
|
| Propriétés physiques | ||
| T° fusion | 98,85 °C ± 1,0[2] | |
| T° ébullition | 332,55 °C[2] | |
| Solubilité | insoluble dans l'eau, soluble dans le benzène. | |
| Point triple | [2] | |
| Thermochimie | ||
| ΔfusH° | 21,708 kJ·mol-1 à [2] | |
| Précautions | ||
| Directive 67/548/EEC | ||
| Écotoxicologie | ||
| DL50 | 470 mg·kg-1 (souris, oral)[3] | |
| Unités du SI et CNTP, sauf indication contraire. | ||
Il se présente sous la forme d'un cristal incolore, et réagit chimiquement de façon similaire à l'anthracène. Cet hétérocycle tricyclique, et plus spécifiquement ses dérivés alkylés sont largement présents dans les fractions les plus lourdes du pétrole[4].
Synthèses et réactions
Le dibenzothiophène est préparé par réaction entre le biphényle et le dichlorure de soufre, en présence de trichlorure d'aluminium[5].
Sa réduction par le lithium résulte en la rupture d'une liaison C-S. Une S-oxydation donne une sulfone plus labile que le dibenzothiophène initial. Avec le n-butyllithium, l'hétérocycle subit une lithiation par étape, aux positions 4 et 6.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « », sur NIST/WebBook, consulté le 30 juin 2010
- Fundamental and Applied Toxicology. Vol. 12, Pg. 787, 1989.
- Teh C. Ho "Deep HDS of diesel fuel: chemistry and catalysis" Catalysis Today 2004, Volume 98, pp. 3-18. DOI 10.1016/j.cattod.2004.07.048
- L. H. Klemm, Joseph J. Karchesy "Dibenzothiophene from biphenyl and derivatives" Journal of Heterocyclic Chemistry, 1978, Volume 15 Issue 4, Pages 561 - 563. DOI 10.1002/jhet.5570150407
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Dibenzothiophene » (voir la liste des auteurs).