Bacillus subtilis
Bacillus subtilis est une bactérie catalase-positive que l'on trouve habituellement dans le sol, mais c'est surtout une espèce ubiquitaire.


| Règne | Bacteria |
|---|---|
| Embranchement | Firmicutes |
| Classe | Bacilli |
| Ordre | Bacillales |
| Famille | Bacillaceae |
| Genre | Bacillus |
- Bacillus globigii
- Bacillus natto
- Bacillus uniflagellatus
- Vibrio subtilis
Description
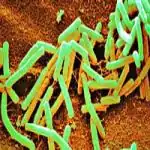

Comme son embranchement l'indique, c'est une bactérie à gram +.
Sa longueur varie de 2 à 4 µm et sa largeur de 0,5 à 2 µm. Elle a pour forme cellulaire des bâtonnets droits à bout arrondis. Elle est mobile grâce à une ciliature péritriche (un système de flagelle qui recouvre tous les côtés de la surface d'une bactérie). Elle est aérobie stricte, sa température optimale est de 40 °C (espèce mésophile) et son type trophique est chimiohétérotrophe. Enfin, son temps de génération est d'environ 26 minutes. Les conditions optimales de croissance de cette souche se situent pour un pH compris entre 5,5 et 8,5, et à une température de 10 °C à 50 °C.
Comme d'autres espèces, B. subtilis peut se constituer une coque protectrice dure (endospore) lui permettant de tolérer des conditions environnementales difficiles ou extrêmes. Bacillus subtilis a été considérée comme aérobie stricte jusqu'en 1998. Il s'agit en fait d'une espèce aérobie facultative qui croît en utilisant du nitrate ou du nitrite comme accepteur d'électrons, ou par fermentation. Elle peut donc survivre à des changements de niveaux d'oxygène dans son environnement[1].
B. subtilis peut produire ou co-produire des biofilms[2] qui peuvent abriter d'autres espèces, éventuellement pathogènes.
Elle n'est pas considérée comme pathogène pour l'homme, mais elle peut contaminer des aliments et peut exceptionnellement provoquer une intoxication alimentaire.
Ses spores peuvent survivre à de très hautes températures, telles que celles communément utilisées pour cuire les aliments. Elle peut être responsable de la présence de zones collantes ou gluantes dans le pain. Néanmoins, une souche de B. subtilis (anciennement connu sous le nom Bacillus natto) est utilisée dans la production commerciale au Japon d'une préparation alimentaire appelée nattô.
D'autres souches de B. subtilis ont d'autres applications commerciales. Par exemple, la souche B. subtilis QST 713 (commercialisé sous le QST 713 ou Serenade) a une activité fongicide naturelle et est pour cette propriété employée comme agent de lutte biologique en agriculture[3]
B. subtilis peut servir à repeupler la flore intestinale par un bacille antibiorésistant, non pathogène.
C'est un organisme de choix pour l'étude de la sécrétion protéique et un des outils ou modèles génétiques les plus aisément manipulables avec la levure.
Observation macroscopique de la colonie
Forme irrégulière
- translucide
- couleur blanc crème ou jaune
- élévation : bossue
- surface brillante
- marge dentelée
- consistance gluante
Une bactérie modèle
Bacillus subtilis est fréquemment utilisé comme outil génétique comme Escherichia coli et les levures[4]. Son étude approfondie comme modèle des bactéries gram+ a permis d’établir les voies de métabolisme cellulaire et la régulation cellulaire. Le séquençage total de son génome a été réalisé pour la première fois en 1997 par Kunst[5] puis révisé par Zeigler en 2008. Ceci a permis de mettre en place de nouvelles approches expérimentales dites globales comme la transcriptomique et l’analyse des 4 200 gènes contenus dans son génome.
B. subtilis est un excellent modèle pour l'étude de bactéries pathogènes, telles que Staphylococcus aureus, Streptococcus pneumoniae, Bacillus anthracis, responsable de la maladie du charbon, Bacillus cereus, à l'origine d'infections alimentaires ou encore Listeria monocytogenes. On l'utilise pour chercher à répondre à des questions telles que :
- Quelles sont les stratégies génétiques qu'utilisent ces bactéries pour se développer, ou provoquer des maladies ?
- Comment se multiplient-elles ? (contrôle de la différenciation cellulaire)
- Comment se protègent-elles ? (par les biofilms, la sporulation, etc.)
- Peuvent-elles transférer des gènes entre elles ?
- Comment combattre une bactérie pathogène au sein d'un organisme infecté ?
- Comment manipuler génétiquement une bactérie ?
- une bactérie aérobie peut être produire du méthane, et comment[6] ?
Une meilleure connaissance des génomes permettra de répondre à beaucoup de ces questions.
En termes de popularité dans les laboratoires, B. subtilis est l'équivalent Gram-positif de Escherichia coli, qui est très étudiée comme modèle de bactérie Gram-négative.
Une source productrice de protéines pour l'industrie
Sa capacité à croître rapidement, à atteindre de hautes densités cellulaires et à sécréter un grand nombre de molécules en a fait une ressource suscitant l’intérêt des industries agroalimentaires et sanitaires pour ses enzymes et les industries pharmaceutiques et cosmétologiques pour ses molécules à large spectre d’activités biologiques, notamment les antibiotiques. Bacillus subtilis est capable de produire des molécules peptidiques qui ne sont pas issues du dogme central de la biologie moléculaire, qui englobe les peptides synthétisés par les ribosomes ; de tels peptides sont fabriqués par la synthèse peptidique non ribosomale ou NRPS (pour non ribosomal peptide synthesis en anglais).
L'industrie agroalimentaire, pharmaceutique et biochimique, s'intéresse aussi à Bacillus subtilis. Elle est, en effet, source d'enzymes industrielles telles les amylases, utilisées dans l'industrie du pain, ou encore des protéases et cellulases, dans l'industrie des détergents.
La variété natto de B. subtilis sert au Japon à fabriquer le natto, un plat traditionnel à base de soja fermenté.
Sa capacité à produire des antibiotiques, comme la bacitracine en fait un organisme d'intérêt également pour l'industrie pharmaceutique.
De plus Bacillus Subtilis est aussi utilisé comme hôte hétérologue alternatif à Escherichia Coli car la bactérie possède une membrane Gram +[7].
Un exemple d'adaptation
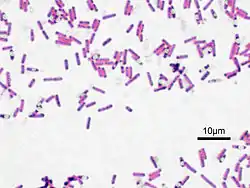
Bacillus subtilis est une bactérie qui forme des spores capables de survivre dans des conditions extrêmes, révélant une adaptation très ancienne.
Sur la centaine de gènes contrôlant cette sporulation, la plupart sont déjà connus. On cherche via ce modèle à comprendre la survie remarquable, à des conditions encore plus extrêmes, des archées. En comparant les génomes de ces deux types de micro-organismes, les étapes de l'adaptation et de l'évolution seront mieux comprises.
Réglementation
Sur le plan de la réglementation des produits phytopharmaceutiques :
- pour l’Union européenne : la souche QST 713 (identique à la souche AQ 713) de Bacillus subtilis est inscrite à l’annexe I de la directive 91/414/CEE par la directive 2007/6/CE.
- pour la France : Bacillus subtilis QST 713 est autorisée dans la composition de préparations bénéficiant d’une autorisation de mise sur le marché.
Elle est employée comme agent de lutte biologique contre la pourriture grise (Botrytis cinerea) de la vigne.
Le séquençage complet du génôme de la souche QST 713 a révélé qu'elle appartenait en fait à l'espèce Bacillus velezensis[8].
Références
- (en) Michiko M. Nakano et Peter Zuber, « ANAEROBIC GROWTH OF A “STRICT AEROBE” ( BACILLUS SUBTILIS ) », Annual Review of Microbiology, vol. 52, no 1, , p. 165–190 (ISSN 0066-4227 et 1545-3251, DOI 10.1146/annurev.micro.52.1.165, lire en ligne, consulté le )
- Bridier A, Le Coq D, Dubois-Brissonnet F, Thomas V, Aymerich S, Briandet R. ; The spatial architecture of Bacillus subtilis biofilms deciphered using a surface-associated model and in situ imaging. PLoS One. 2011 Jan 18; 6(1):e16177. Epub 2011 Jan 18. (Résumé)
- Biopesticides, par l'EPA
- Tufts Univ Boston MA:ASM press, 2001, Bacillus subtilis and its closest relatives: from genes to cells coauteur Sonenshein et al
- The complete genome of sequence of the gram-positive bacterium bacillus subtilis, 1997, Nature, coauteur Kunst et al
- V. I. Bruskov, Zh. K. Masalimov et A. V. Chernikov, « [No title found] », Doklady Biochemistry and Biophysics, vol. 384, nos 1/6, , p. 181–184 (DOI 10.1023/A:1016036617585, lire en ligne, consulté le )
- Wenjing Cui, Laichuang Han, Feiya Suo et Zhongmei Liu, « Exploitation of Bacillus subtilis as a robust workhorse for production of heterologous proteins and beyond », World Journal of Microbiology & Biotechnology, vol. 34, no 10, , p. 145 (ISSN 1573-0972, PMID 30203131, DOI 10.1007/s11274-018-2531-7, lire en ligne, consulté le )
- (en) Caroline Pandin, Dominique Le Coq, Julien Deschamps et Régis Védie, « Complete genome sequence of Bacillus velezensis QST713: A biocontrol agent that protects Agaricus bisporus crops against the green mould disease », Journal of Biotechnology, vol. 278, , p. 10–19 (DOI 10.1016/j.jbiotec.2018.04.014, lire en ligne, consulté le )