Tellurocystéine
La tellurocystéine est un acide L-α-aminé analogue de la cystéine et de la sélénocystéine dans lequel un atome de tellure remplace respectivement l'atome de soufre et de sélénium.
| Tellurocystéine | |
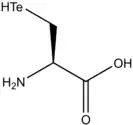
| |
| Structure de la L-tellurocystéine | |
| Identification | |
|---|---|
| Nom UICPA | acide (2R)-2-amino-3-λ1-tellanylpropanoïque |
| PubChem | 129631934 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C3H6NO2Te |
| Masse molaire[1] | 215,69 ± 0,03 g/mol C 16,71 %, H 2,8 %, N 6,49 %, O 14,84 %, Te 59,16 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
L'énergie de liaison du tellure au carbone n'est que de 200 kJ·mol-1, à comparer à 234 kJ·mol-1 pour le sélénium et 272 kJ·mol-1 pour le soufre[2], ce qui explique probablement que la tellurocystéine est normalement absente des êtres vivants, contrairement à ses homologues protéinogènes que sont la cystéine et la sélénocystéine, et demeure peu étudiée[3].
Cependant, certains organismes comme le champignon Aspergillus fumigatus sont capables d'incorporer la tellurocystéine et la tellurométhionine dans leurs protéines lorsqu'on les fait croître dans un milieu dépourvu de soufre[4]. On a observé que la tellurocystéine, lorsqu'elle est incorporée à une glutathion S-transférase, inhibe efficacement l'aminoacylation, tandis qu'elle active les glutathion peroxydases[5].
La L-tellurocystéine peut être obtenue en faisant réagir du tellure avec du (2R)-2-[(tert-butoxycarbonyl)amino]-3-iodopropionate de méthyle dans le tétrahydrofurane en présence de triéthylborohydrure de lithium, ce qui donne une huile rouge qui est acidifiée puis traitée à la soude avant adjonction d'acide citrique pour amener son pH à 4,0 et former un solide orange après filtration et séchage[6].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Tristram Chivers et Risto S. Laitinen, « Tellurium: a maverick among the chalcogens », Chemical Society Reviews, vol. 44, no 7, , p. 1725-1739 (DOI 10.1039/C4CS00434E, lire en ligne)
- (en) Robert K. Poole, Advances in Microbial Physiology, vol. 53, Elsevier, 2007. (ISBN 9780080560649)
- (en) Shadia E. Ramadan, A. A. Razak, A. M. Ragab et M. El-Meleigy, « Incorporation of tellurium into amino acids and proteins in a tellurium-tolerant fungi », Biological Trace Element Research, vol. 20, no 3, , p. 225-232 (PMID 2484755, DOI 10.1007/BF02917437, lire en ligne)
- (en) Xiaoman Liu, Louis A. Silks, Cuiping Liu, Morgane Ollivault‐Shiflett, Xin Huang, Jing Li, Guimin Luo, Ya‐Ming Hou, Junqiu Liu et Jiacong Shen, « Incorporation of Tellurocysteine into Glutathione Transferase Generates High Glutathione Peroxidase Efficiency », Angewandte Chemie, vol. 121, no 11, , p. 2054-2057 (PMID 19199319, DOI 10.1002/ange.200805365, lire en ligne)
- (en) Emily M. Stocking, Jessie N. Schwarz, Hans Senn, Michael Salzmann et Louis A. Silks, « Synthesis of L-selenocystine,L-[77Se]selenocystine and L-tellurocystine », Journal of the Chemical Society, Perkin Transactions 1, no 16, , p. 2443-2448 (DOI 10.1039/A600180G, lire en ligne)