Souris de laboratoire
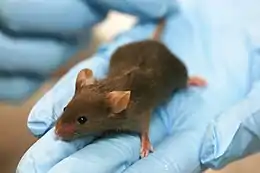
L'expression « souris de laboratoire » désigne un rongeur sentient utilisé dans le cadre de recherches scientifiques ou de tests biologiques, par exemple allergologiques ou cancérologiques. Les laboratoires utilisent également l’expression « modèle murin ».

Histoire
Les souris communes (Mus musculus) ont été et continuent à être beaucoup utilisées comme organismes modèles en biologie, par exemple en génétique, en embryologie, en oncologie, en pharmacologie ou en toxicologie.
Depuis 2015, plus d’un million de souris sont utilisées chaque année dans les laboratoires français[1] - [2]. À l’échelle de l’Union européenne, ce nombre monte à plus de cinq millions[3].
Intérêts et limites de l'usage des souris comme modèles
Avantages
Les souris présentent plusieurs avantages pour les laboratoires dont celui d'avoir un cycle de développement et de vie court, un élevage facile à faible coût, une petite taille et une reproduction prolifique.
Un autre intérêt majeur est qu'il s'agit de mammifères dont le génome reste proche de celui de l'espèce humaine (99 % de gènes homologues entre l'homme et la souris, c'est-à-dire de gènes proches mais pas forcément identiques[4]). Elles constituent l'espèce la plus souvent utilisée en expérimentation animale, notamment pour la recherche médicale et la toxicologie, en particulier pour l'établissement d'indicateurs, comme la DL50 qui est un indicateur de la toxicité aiguë.
Limites
Les premières limites toxicologiques et éthologiques sont que la souris n’a pas, en cage ou en laboratoire, un comportement normal, et rarement exactement la même sensibilité que l’homme aux produits toxiques, médicaments, rayonnements, etc. Il reste donc nécessaire de multiplier le nombre d’espèces utilisées pour fiabiliser certains résultats (avec le rat de laboratoire, hamster, chien, singe, etc.)[5].
Une autre limite est sa courte durée de vie qui fait qu'on ne peut tester sur elle les effets délétères de certaines molécules ou facteurs agissant sur le long ou très long terme. Les extrapolations de la souris à des organismes à durée de vie plus longue sont potentiellement sources de biais.
Conditions de vie
Élevage
.JPG.webp)
Âge de mise à la reproduction : 8 semaines.
Après l'accouplement, il est possible de vérifier si celui-ci a réussi (en regardant si le bouton vaginal est présent au niveau de l'appareil génital de la femelle). Ceci fait, il faut séparer les femelles accouplées des mâles sexuellement actifs.
Pour répondre à la demande des laboratoires, des élevages spécialisés produisent des souches murines fortement standardisées[6].
Normes de détention et environnement de l'animal
Des normes de base sont définies par la réglementation française[7] et européenne[8] par espèce. Ces normes fixent notamment des seuils minimum et maximum de température correspondant aux normes physiologiques des souris ainsi qu'une réglementation sur l’hygrométrie, la ventilation, l'environnement acoustique et lumineux tout en respectant les statuts sanitaires imposés. La réglementation prescrit une surveillance sanitaire et un contrôle quotidien par les animaliers ou les expérimentateurs avec une fiche de suivi et un registre d'entrées et de sorties des animaux.
La réglementation indique que les animaux « doivent disposer d'un espace suffisant présentant une complexité adéquate pour leur permettre d'exprimer un large répertoire de comportements normaux ». Un nombre de souris est donc fixé en fonction du poids des individus pour définir la taille minimum des cages. Ainsi, la taille minimale d'une cage contenant trois ou quatre souris adultes (de plus de 25 g) est de 330 cm² (15 × 22 cm, soit un peu plus grand qu'une demi-feuille A4).
Selon les projets de recherche, les souris peuvent être dans des cages individuelles. Dans ce cas, la réglementation prévoit que « la durée de l'isolement doit être limitée à la période minimale nécessaire et des contacts visuels, auditifs, olfactifs et/ou tactiles doivent être maintenus avec les autres animaux ». Aucune limite de durée n'est fixée par défaut. Cela pouvant être un isolement dû à une récupération de l'animal post-chirurgie ou bien lié à un protocole expérimental particulier suivant un modèle précis et encadré. A contrario, les cages peuvent être "enrichies" ce qui signifie que des ajouts sont réalisés pour permettre aux souris d'exprimer un comportement normal et adapté (ajouts de jouets, cachettes, litière supplémentaire...).
Douleur
La réglementation européenne considère comme relevant de l'expérimentation animale toute utilisation d'un animal vertébré, d'un céphalopode ou d'une forme larvaire ou fœtale antérieure au derniers tiers du développement, dès lors que l'utilisation est susceptible « de causer à cet animal une douleur, une souffrance, une angoisse ou des dommages durables équivalents ou supérieurs à ceux causés par l'introduction d'une aiguille effectuée conformément aux bonnes pratiques vétérinaires »[9]. En Europe, par définition, l'expérimentation animale est donc source de souffrances physiques et/ou psychiques à différents degrés pour les animaux utilisés.
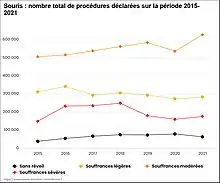
Quatre degrés de gravité sont définis : sans réveil, léger, modéré, sévère. D’après la réglementation, cette classification « est fondée sur les effets les plus graves que risque de subir un animal donné après mise en œuvre de toutes les mesures de raffinement appropriées »[10] – ce qui signifie qu'il s'agit d'évaluer les souffrances endurées par les animaux malgré l’utilisation d’anesthésiques et d’analgésiques. Cette classification ne prend pas en considération les souffrances éventuelles inhérentes à la captivité elle-même.
D'après les données statistiques recueillies par le ministère chargé de la Recherche depuis 2014, environ un tiers des expériences impliquant des souris sont de gravité « sans réveil » ou « légère », les deux tiers restants sont composés de procédures « modérées » ou « sévères »[1] - [2].
Ces degrés de gravité ainsi que la mise en place de points limites se doivent d'être finement justifiés au vu du projet scientifique. Une fois entré dans un protocole expérimental, l'animal est surveillé en permanence afin de déceler le moindre signe de douleur ou de stress (physiologique, comportemental, d'apparence).
Exemples d'expériences
Depuis 2022, la base de données européenne ALURES fournit les résumés non techniques des projets d’expérimentation animale approuvés dans l’Union européenne. Des filtres sont disponibles pour y découvrir les plus récentes expériences approuvées utilisant des souris[11].
Des résumés de certains de ces projets, classés par espèce, niveau de souffrance et type de recherches, sont également fournis sur le site web documentaire spécialisé[1] créé et entretenu par l’association One Voice.
Cas particuliers
Souris nude
Les souris « nude » ont un système immunitaire déficient, ce qui permet aux tumeurs humaines de pousser sur ces souris quand elles sont greffées.
L'avantage de ce modèle est que les tumeurs sont très pures (non contaminées par des cellules normales) et que de nombreux traitements peuvent être essayés.
Ce modèle présente un problème éthique spécifique, l’absence de système immunitaire et la greffe de tumeurs entrainant des conditions de détention et des souffrances non négligeables pour ces souris.
Souris Kaguya
La souris prénommée Kaguya est la première souris ayant pour parents deux femelles, sans clonage[12] - [13].
Autres souches génétiquement modifiées

En génétique, les généticiens ont créé de très nombreuses lignées de souris transgéniques, qui sont considérées comme autant d'outils pour la recherche. Il s'agit de souris dont le patrimoine génétique a été modifié artificiellement.
La méthode la plus simple pour ce faire est l'injection d'un segment d'ADN comportant le gène à étudier directement dans le noyau de l'œuf fécondé. En cas de succès de l'opération, le gène est incorporé en un ou plusieurs exemplaires de façon aléatoire. Une méthode plus sophistiquée permet de modifier directement un gène, aboutissant à une souris KO (« Knock-out » avec inactivation d'un gène) ou KI (« Knock-in ») avec insertion d'un gène actif :
- le gène à insérer est mis en place dans un vecteur (plasmide ou virus), entouré de séquences ADN identiques à celui de la cellule normale à la position où on désire l'introduire. Ce gène est couplé avec un gène de sélection (résistance à un antibiotique ou production d'une protéine fluorescente par exemple) qui permettra de prouver la bonne intégration du premier dans le génome ;
- on fait pénétrer le vecteur porteur du gène dans une cellule embryonnaire ;
- on sélectionne alors les cellules ayant intégré le gène grâce à la propriété du gène de sélection. Ces cellules sont alors multipliées en culture et sont injectées dans un blastocèle de souris (cavité d'un embryon). Le tout est réimplanté dans l'utérus ;
- des souriceaux mosaïque sont alors obtenus : une partie de ses cellules ont un patrimoine génétique normal et une autre partie un patrimoine modifié avec inclusion du gène étudié ;
- le croisement répété de ces souris mosaïque aboutit dans un certain nombre de cas à des souris homozygotes dont toutes les cellules contiennent le gène modifié.
Une structure américaine, le Jackson Laboratory, possède toutes les lignées de souris transgéniques existantes[14].
Les biologistes ont réussi à isoler et cultiver des cellules totipotentes embryonnaires de souris (cellules ES), capables de coloniser la lignée germinale d’un embryon hôte. Ils commencent à pouvoir partiellement contrôler le processus de recombinaison homologue entre une séquence d’ADN nu introduite de l’extérieur et l’ADN chromosomique.
À partir de 1987, on a pu induire une mutagenèse « ciblée » sur un allèle résidant des cellules ES, ce qui élargit encore la liste des mutations induites possibles conduisant à pouvoir imaginer presque tous les types de modifications génétiques biologiquement possibles (des mutations nulles et ponctuelles aux délétions en passant par les translocations de gènes...). Puis des moyens nouveaux de la biologie moléculaire ont rendu possible l’induction de mutations au sein d’un type cellulaire choisi et/ou à un instant donné du cycle de développement de la souris.
Durant près de trois décennies, le génome de la souris de laboratoire a ainsi fait l’objet de manipulations délibérées de plus en plus complexes, qui ont servi à mieux comprendre la fonction de nombreux gènes chez les mammifères[15].
Questions éthiques
Modifications génétiques
Comme pour d’autres espèces d’animaux utilisés en laboratoire, des questions de bioéthique, d'éthique animale et d’éthique environnementale sont posées par l’expérimentation animale in vivo, notamment quand elle est source de stress, douleurs et/ou souffrance intenses ou prolongées pour l’animal (il existe des souches de souris manipulées pour développer des cancers ou d’autres maladies graves), ou quand il s’agit de créer par transgénèse ou d’autres moyens des souris génétiquement modifiées ou dans le cas de création de chimères génétiques animal-humain[16] ou de volonté de brevetage du vivant[17].
Ces questions se posent différemment selon que le point de vue de l’observateur est biocentré ou anthropocentré[18], ou encore sentiocentré.
Éthique animale
Il existe un consensus parmi les spécialistes de philosophie morale, de philosophie politique et d’éthique animale pour dire que l’espèce n’est pas un critère pertinent pour décider si un individu a droit à une considération morale. Ce consensus a été exprimé en 2022 par plusieurs centaines de spécialistes dans la Déclaration de Montréal sur l’exploitation animale. Pour ces spécialistes, le critère d’intérêt est la sentience, c’est-à-dire la capacité à « ressentir du plaisir, de la douleur et des émotions ». Dans cette perspective, tout individu sentient doit voir ses intérêts pris en compte lors des délibérations morales sans que son espèce serve à pondérer le poids accordé à ces intérêts[19].
Comme le dit François Jaquet (spécialiste d’éthique animale et de méta-éthique) en 2022, la posture actuelle est irrationnelle puisqu’elle invoque des principes déontologistes pour protéger les personnes humaines impliquées dans des recherches tout en s’appuyant sur une éthique utilitariste pour l’utilisation des autres espèces. Une éthique rationnelle consisterait au contraire à appliquer les mêmes principes (qu’ils soient déontologistes ou conséquentialistes) à l’ensemble des individus sentients, quelle que soit leur espèce – ce qui aurait pour conséquence la suppression de la totalité des expérimentations animales pratiquées de nos jours[20].
Hommage
Une statue de souris de laboratoire anthropomorphique avec des lunettes et une blouse de laboratoire en train de tricoter une double hélice d'ADN a été sculptée en son honneur à Novossibirsk une ville de Russie, en Sibérie occidentale[21]. Ce monument est situé dans un parc en face de l'Institut de cytologie et de génétique de la cité scientifique d'Akademgorodok, et a été achevé le .
Notes et références
- « Les chiffres de l’expérimentation animale en France », sur experimentation-animale.com (consulté le )
- « Enquête statistique sur l'utilisation des animaux à des fins scientifiques », sur enseignementsup-recherche.gouv.fr (consulté le )
- « Nombre d'animaux utilisés dans l'Union européenne depuis 2015 », sur ALURES (base de données des chiffres de l'expérimentation animale dans l'Union européenne) (consulté le )
- « Du génome de la souris à celui de l'homme », sur http://www.futura-sciences.com.
- Boisseau-Lebreuil, M. T. (1975). « Sensibilité comparée de divers animaux de laboratoire à l'infection par instillations nasales de la phase saprophytique d'Emmonsia crescens Emmons & Jellison, 1960: Fréquence et intensité du parasitisme, réactions histopathologiques ». Mycopathologia, 56(3), 143-148 (résumé).
- Daniel Langlois-Berthelot, Marcelin Berthelot : un savant engage, Paris, Lattès, , 374 p. (ISBN 978-2-7096-2164-9, OCLC 406967298)
- « Arrêté du 1er février 2013 fixant les conditions d'agrément, d'aménagement et de fonctionnement des établissements utilisateurs, éleveurs ou fournisseurs d'animaux utilisés à des fins scientifiques et leurs contrôles », sur Legifrance, (consulté le )
- « Directive 2010/63/UE », sur eur-lex.europa.eu (consulté le )
- « Utilisation d'animaux vivants à des fins scientifiques (Articles R214-87 à R214-137 du Code rural et de la pêche maritime) », sur Legifrance (consulté le )
- « Arrêté du 1er février 2013 relatif à l'évaluation éthique et à l'autorisation des projets impliquant l'utilisation d'animaux dans des procédures expérimentales », sur Legifrance (consulté le )
- « Liste de projets d'expérimentation animale utilisant des souris ou des rats approuvés en France depuis 2022 », sur ALURES (base de données européenne de Résumés Non Techniques en expérimentation animale) (consulté le )
- , Radio-Canada - Création de souris sans mâle
- , Pour la Science - Actualité - Sans père, des souris vivent plus longtemps...
- Base de données en libre accès du Jackson Laboratory
- Babinet, C., & Cohen-Tannoudji, M. (2000). Vingt ans d'interventions délibérées sur le génome de la souris: une révolution dans l'approche génétique de la biologie des mammifères ; , Med Sci (Paris), 2000, Vol. 16, no 1; p. 31-42 (Fiche résumé/Inserm
- Ethikrat D (2011) Les êtres mixtes humain-animal dans la recherche , Avis du comité national allemand d’éthique (édition originale allemande titrée : « Mensch-Tier-Mischwesen in der Forschung » ), (ISBN 978-3-941957-51-0)
- Chevassus-au-Louis, B. (2004). L'appropriation du vivant: de la biologie au débat social. Les Dossiers de l'environnement de l'INRA, (27), 91-108.
- Beaufays, J. P., Spano, L., & Di Pietro, E. La souris dans nos laboratoires.(PDF, 17 pages)
- « Déclaration de Montréal sur l’exploitation animale », (consulté le )
- « Table ronde HECTOR 4/4: (Con)sciences » (consulté le )
- « Novossibirsk », sur https://russieautrement.com/ (consulté le ).
Voir aussi
Articles connexes
Lien externe
- Souris de laboratoire, sur Futura-Sciences
Bibliographie
- Beaufays, J. P., Spano, L., & Di Pietro, E. La souris dans nos laboratoires.(PDF, 17 pages)