Permanganate de calcium
Le permanganate de calcium est un comburant. Il est composé d'ions calcium et d'ions permanganate.
| Permanganate de calcium | |
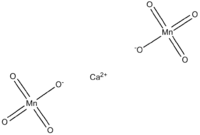
| |
| Identification | |
|---|---|
| Nom UICPA | dipermanganate de calcium |
| No CAS | |
| No ECHA | 100.030.280 |
| No CE | 233-322-7 |
| No RTECS | EW3860000 |
| PubChem | 24959 |
| Propriétés chimiques | |
| Formule | Ca(MnO4)2 |
| Masse molaire[1] | 277,949 ± 0,006 g/mol Ca 14,42 %, Mn 39,53 %, O 46,05 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Il est obtenu par réaction du permanganate de potassium et du chlorure de calcium ou de la réaction du permanganate d'aluminium et de l'oxyde de calcium.
Applications
Il est utilisé afin d'aider à blanchir les dents dans certains dentifrices[2].
Sécurité
Si le matériau combustible est finement divisé, le mélange obtenu peut être explosif. Le contact avec l'acide sulfurique, le benzène, le sulfure de carbone, l'éther diéthylique, l'éthanol et le pétrole peut provoquer des incendies ou des explosions. Des mélanges avec l'anhydride acétique peuvent également provoquer des explosions si celui-ci n'est pas conservé au froid.
Références
- F. A. Cotton, G. Wilkinson, C. A. Murillo, and M. Bochmann (April 1999). Advanced Inorganic Chemistry, 6th Édition. Wiley-VCH. (ISBN 0-471-19957-5)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Permanganate containing whitening compositions and methods of their use, consulté le 20 janvier 2013
Cet article est issu de wikipedia. Text licence: CC BY-SA 4.0, Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.