Lacune de miscibilité
Une lacune de miscibilité est une zone d'un diagramme de phase (ou, plus généralement, les conditions de température, pression et composition globale) où coexistent deux phases de mêmes structure et symétries mais de compositions différentes. Les lacunes de miscibilité se rencontrent à l'état liquide comme à l'état solide. Dans un diagramme de phase, la courbe qui délimite une lacune de miscibilité est dénommée courbe de coexistence ou, plus précisément[alpha 1], solvus.
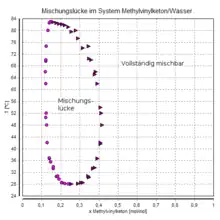
Pour l'application des lois thermodynamiques caractérisant les changements de phase (règle des phases, formule de Clapeyron, etc.) il s'agit de deux phases distinctes, mais en termes de structure et de symétries il s'agit d'une phase unique. On peut notamment passer continûment, dans le diagramme de phase, de la phase riche (en un certain constituant) à la phase pauvre sans franchir la courbe de coexistence.
Dans le diagramme de phase la lacune de miscibilité se referme à une température maximale dite température critique (Tc) ou température critique supérieure (TCS), au-dessus de laquelle les deux constituants du système sont miscibles en toutes proportions. Elle peut aussi se refermer à une température minimale, dite température critique inférieure (TCI), au-dessous de laquelle les deux constituants sont à nouveau miscibles en toutes proportions. Une lacune d'immiscibilité comportant les deux températures critiques est souvent qualifiée de boucle d'immiscibilité. La température critique inférieure ne s'observe que rarement dans le cas des solutions solides.
Terminologie
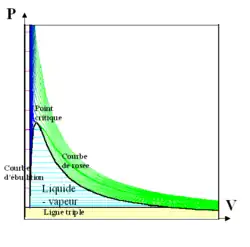
L'Union internationale de chimie pure et appliquée (UICPA) a défini en 2004[1] une lacune de miscibilité comme « la zone à l'intérieur d'une courbe de coexistence dans un diagramme de phase isobare (température vs composition) ou isotherme (pression vs composition »[alpha 2]. Cette formulation pourrait laisser penser qu'elle s'applique à toute coexistence de deux phases dans un diagramme de phase isobare ou isotherme (l'UICPA ne précise pas que les deux phases ont les mêmes structure et symétries, et l'expression « courbe de coexistence » est ambiguë), et par exemple au domaine diphasé liquide-solide présent dans la plupart des diagrammes binaires. Mais l'IUPAC ajoute dans une note : « On observe une lacune de miscibilité au-dessous d'une température critique supérieure (TCS) ou au-dessus d'une température critique inférieure (TCI). Dans la lacune de miscibilité il coexiste au moins deux phases »[alpha 3]. Cette mention d'une température critique indique bien que les deux phases qui coexistent dans la lacune de miscibilité sont en réalité deux variantes d'une unique phase caractérisée par sa structure et ses symétries, exactement comme les deux phases du domaine liquide-gaz du diagramme P-V d'un corps pur, qui n'en forment qu'une au-dessus de la température critique (figure ci-contre).
En pratique on parle aussi de lacune de miscibilité en l'absence d'un diagramme de phase en bonne et due forme, notamment dans le cas de solutions liquides ou solides chimiquement complexes. En magmatologie, par exemple, il peut apparaître quand la température décroît une lacune de miscibilité dans un liquide aluminosilicaté : une phase liquide initialement homogène se sépare en deux liquides immiscibles qui différent notamment par leur teneur en silice SiO2[2].
Origine thermodynamique
Du point de vue thermodynamique, Gibbs a été le premier à expliquer les types de comportement de phases entre une région d'équilibre stable et métastable. Il montre que la condition de stabilité, ou de métastabilité, est que la dérivée seconde de l'enthalpie libre molaire soit positive ou négative. Ainsi selon les conditions de Gibbs, le diagramme de phase d'un système binaire en fonction de la température et de la composition montrant une lacune de miscibilité qui peut être divisée en trois régions stable, métastable et instable[3]. Par ailleurs, l'augmentation de la température entraîne une diminution de la concavité de la lacune de miscibilité. Ainsi dans le cas du diagramme binaire, à température critique, le mélange devient complètement homogène avec des proportions égales entre les deux constituants du mélange ou de l'alliage. Si les points de fusion des composants purs d’un système binaire sont très différents, un diagramme de phase complètement diffèrent est obtenu lorsque l’énergie du mélange augment[4].
Mise en évidence expérimentale
Analyse thermique différentielle
Une étude expérimentale du système Ir-Rh a été faite pour prouver l’existence de la lacune de miscibilité en réalisant des analyses ATD à haute température. Lors de l’échauffement de l’alliage, aucune lacune n’a pu être détectée, ce qui les a amené à dire que cette méthode n’est pas le moyen le plus pertinent pour mener cette analyse. Cependant, sur la phase de refroidissement, un léger effet endothermique a pu être détecté à partir d’une certaine température. Cela pourrait bien correspondre à la démixtion de la solution solide. L'étude de l’alliage Ir50Rh50 avec refroidissement lent a détecté cet effet à partir de 888 °C[5].
Analyse par microscope électronique
L'Utilisation d'un microscope électronique permet la mise en évidence de la microstructure des alliages. L'observation de la microstructure peut en effet révéler des défauts structuraux (grains ou joint grains) entraînant des lacunes de miscibilité dans les alliages. cette technique donne de bonnes informations sur la morphologie des phases[6].
Diffraction des rayons X
L'identification de phase est l'application la plus courante de diffraction de rayons X (DRX) sur poudres. Une fois le diagramme obtenue, on compare les positions et les intensités des pics observés avec une base de référence .On peut ainsi rapidement vérifier les résultats de synthèses, soit une bonne phase cristalline complément homogène ou une phase avec des défauts, donc présentant une lacune de miscibilité, ou un nouveau matériaux[6].
Cette technique permet d'obtenir des mesures des dimensions caractéristiques et de l'avancement de la démixtion. Il est cependant préférable de connaître par ailleurs la morphologie des phases, pour pouvoir interpréter quantitativement les mesures. La DRX est non seulement une analyse rapide mais aussi non destructive par rapport au mélange.
Autres analyses
D'autres types de mesure permettent d'avoir des informations soit sur la composition des phases, soit sur l'avancement de la démixtion, comme l'effet Mossbauer, la résistivité[7] , la calorimétrie et les propriétés magnétiques. La sonde atomique permet d'obtenir à la fois une mesure de la composition des phases et des dimensions caractéristiques, si l’échantillonnage est fait sur un nombre suffisant d'atomes[8].
Mécanisme de démixtion
Lorsque le diagramme de variation d'enthalpie libre de la phase cristalline en fonction de la composition possède deux minima séparés par un maximum, le diagramme de phases correspondant présente à l’état solide une lacune de miscibilité[9].
Mais en pratique, dans un fluide, la mobilité intrinsèque des constituants conduit à de brèves fluctuations locales de composition. Tout enrichissement local en un composant étant nécessairement accompagné par un appauvrissement dans une zone immédiatement adjacente. Des fluctuations de composition peuvent également se produire dans un solide à des températures assez élevées, mais plus limitées car les processus de diffusion y sont généralement plus lents que dans un liquide. Dans les deux cas, de telles fluctuations représentent le tout début d’un processus de démixtion[10].
Exemple
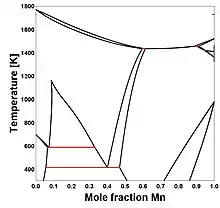
Corne de Nishawa, terme désignant un écart de miscibilité existant lorsque des phases ayant des propriétés magnétiques différentes coexistent dans le diagramme de phases [11]. Par exemple, dans le système Co-Mn, on a la même structure cubique faces centrées mais différentes propriétés magnétiques tel que le cobalt (Co) se comporte comme un ferromagnétique et le manganèse (Mn) comme un paramagnétique à des températures de Curie différentes.
Notes et références
Notes
- Le terme de courbe de coexistence ne s'emploie pas que pour les lacunes de miscibilité, on l'utilise aussi pour d'autres courbes d'un diagramme de phase où coexistent plusieurs phases, par exemple pour la ou les courbes qui délimitent un domaine diphasé liquide-solide.
- Citation originale : Miscibility gap: Area within the coexistence curve of an isobaric phase diagram (temperature vs. composition) or an isothermal phase diagram (pressure vs. composition)[1].
- Citation originale : A miscibility gap is observed at temperatures below an upper critical solution temperature (UCST) or above the lower critical solution temperature (LCST). Its location depends on pressure. In the miscibility gap, there are at least two phases coexisting[1].
Références
- (en) W. J. Work, K. Horie, M. Hess et R. F. T. Stepto, « Definitions of Terms Related to Polymer Blends, Composites, and Multiphase Polymeric Materials (IUPAC Recommendations 2004) », Pure and Applied Chemistry, vol. 76, no 11, , p. 1985-2007 (DOI 10.1351/pac200476111985, lire en ligne [PDF], consulté le ).
- (en) Ilya V. Veksler, Alexander M. Dorfman, Alexander A. Borisov, Richard Wirth et Donald B. Dingwell, « Liquid Immiscibility and the Evolution of Basaltic Magma », Journal of Petrology (en), vol. 48, no 11, , p. 2187-2210 (DOI 10.1093/petrology/egm056).
- Abdel Ait Chaou, « Études thermodynamiques et structurales des alliages Ce-Au et Zr-Ce-Au pour la fabrication de catalyseurs a base d’or : application a l’oxydation selective du monoxyde de carbone en presence d’oxygene », These de l’Universite de Savoie, 2005
- (de) Peter Haasen, Physikalische Metallkunde, (DOI 10.1007/978-3-642-96199-1, lire en ligne)
- Taguett, Amine (1985-....)., Synthèse et étude thermodynamique d'alliages Ir-Rh à l'état massif et en films minces pour la réalisation de capteurs SAW fonctionnant à haute température (700 °C-1000 °C) dans l'air. (OCLC 991596790, lire en ligne)
- D. K. Chaudhuri, P. A. Ravindran et J. J. Wert, « Comparative X‐Ray Diffraction and Electron Microscopic Study of the Transformation‐Induced Substructures in the Iron‐Nickel Martensites and Their Influence on the Martensite Properties », Journal of Applied Physics, vol. 43, no 3, , p. 778–788 (ISSN 0021-8979 et 1089-7550, DOI 10.1063/1.1661280, lire en ligne, consulté le )
- G. Rivaud, J. Guillot et J. Grilhé, « Determination de la lacune de miscibilite par mesures de resistivite - cas de Zn », Scripta Metallurgica, vol. 6, no 5, , p. 411–415 (ISSN 0036-9748, DOI 10.1016/0036-9748(72)90213-x, lire en ligne, consulté le )
- F. BLEY, J. DESPLAT, P. GUYOT et F. LIVET, « Séparations de phases dans les solutions solides métalliques », Le Journal de Physique IV, vol. 04, no C3, , C3–15-C3-24 (ISSN 1155-4339, DOI 10.1051/jp4:1994302, lire en ligne, consulté le )
- « Traite des materiaux volume 1 : introduction a la science des materiaux Coordonnateurs : J.-P. MERCIER, G. ZAMBELLI et W. KURZ 1 volume, 499 pages, 17 chapitres, Troisième édition 1999, Presses Polytechniques et Universitaires Romandes, EPFL - Centre Midi, CH - 1015 Lausanne, (ISBN 2-88074-402-4) », Annales de Chimie Science des Matériaux, vol. 27, no 1, , p. 79 (ISSN 0151-9107, DOI 10.1016/s0151-9107(02)85010-3, lire en ligne, consulté le )
- Vipul Sharma, Ramachandran Balaji, Nisha Kumari et Venkata Krishnan, « SERS Application of Noble Metal–Metal Oxide Hybrid Nanoparticles », dans Noble Metal-Metal Oxide Hybrid Nanoparticles, Elsevier, (ISBN 978-0-12-814134-2, lire en ligne), p. 457–486
- J.-C. Zhao, « PHASE DIAGRAM DETERMINATION USING DIFFUSION MULTIPLES », dans Methods for Phase Diagram Determination, Elsevier, (ISBN 978-0-08-044629-5, lire en ligne), p. 246–272
_Mixture_of_Ethanol_and_Dodecane.png.webp)