Isotopes du béryllium
Le béryllium (Be) possède 12 isotopes connus, de nombre de masse variant de 5 à 16. Un seul de ces isotopes, le béryllium 9 (9Be), est stable, ce qui fait du béryllium un élément monoisotopique. Les radioisotopes du béryllium ayant une durée de vie relativement courte et étant non primordiaux, leur abondance est infime, ce qui fait également du béryllium un élément mononucléidique. La masse atomique standard du béryllium est donc la masse atomique de 9Be, 9,012 182(3) u.
Le béryllium 9 est un nucléide primordial ; on pense que la plupart du béryllium 9 présent dans l'univers a été formé par spallation des rayons cosmiques dans une période entre le Big Bang et la formation du système solaire .
Sur les 11 radioisotopes connus, le plus stable est le béryllium 10 (10Be), avec une demi-vie 1,36 million d'années, suivi par le béryllium 7 (7Be) avec une demi-vie de 53,22 jours. Tous les autres radioisotopes ont une demi-vie inférieure à une minute. Les isotopes plus lourds que 9Be se désintègrent principalement par émission β− en isotopes du bore.
Particularité
Le béryllium est le seul élément monoisotopique avec un nombre de protons pair et aussi le seul à avoir un nombre de neutrons impair, le béryllium 9 possédant 4 protons et 5 neutrons.
Ceci s'explique par le fait que l'isotope ayant le même nombre de protons et de neutrons (4 de chaque), 8Be est trop instable. De par sa composition, il se désintègre très facilement par double désintégration α en deux atomes d'hélium 4, réaction qui est favorisée par la cohésion interne extrême d'un noyau d'hélium 4, ce qui lui donne une demi-vie de 6,7(17)×10−17 secondes. Le béryllium ne peut pas avoir non plus d'isotope stable avec 4 protons et 6 neutrons car le ratio protons/neutrons est beaucoup trop déséquilibré pour un élément aussi léger. Cependant, le béryllium 10, bien que radioactif a une demi-vie de 1,36 million d'années.
Les autres isotopes possibles du béryllium ont des déséquilibres protons/neutrons bien trop importants. Ils sont encore moins stables.
Béryllium 7 et béryllium 10
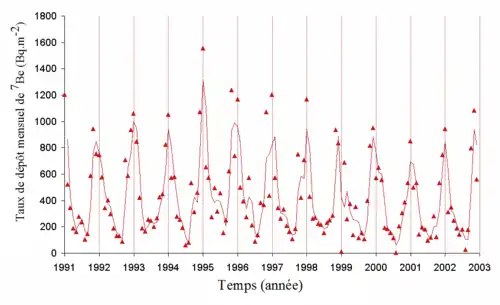
Les isotopes 7Be et 10Be sont tous les deux des nucléides cosmogéniques créés assez récemment dans le système solaire par spallation des rayons cosmiques, tout comme le carbone 14. La teneur de ces deux radioisotopes du béryllium dans l'atmosphère est un indicateur du cycle des taches solaires et de l'activité solaire, ces phénomènes affectant la magnétosphère qui protège la Terre des rayons cosmiques. Le taux avec lequel 7Be, isotope à courte vie, est transféré de l'air au sol dépend en partie de la météorologie locale.
La désintégration de 7Be dans le Soleil est l'une des sources de neutrinos solaires, et le premier type détecté par l'expérience Homestake.
Table des isotopes
| Symbole de l'isotope |
Z (p) | N (n) | Masse isotopique (u) | Demi-vie | Mode(s) de désintégration[1] |
Isotope(s)-fils[n 1] | Spin nucléaire |
|---|---|---|---|---|---|---|---|
| 5Be | 4 | 1 | 5,04079(429)# | p | 4Li | (1/2+)# | |
| 6Be | 4 | 2 | 6,019726(6) | 5,0(3)×10−21 s [0,092(6) MeV] |
2p | 4He | 0+ |
| 7Be[n 2] | 4 | 3 | 7,01692983(11) | 53,22(6) j | CE | 7Li | 3/2- |
| 8Be[n 3] | 4 | 4 | 8,00530510(4) | 6,7(17)×10−17 s [6,8(17) eV] |
fission | 2 4He | 0+ |
| 9Be | 4 | 5 | 9.0121822(4) | Stable | 3/2- | ||
| 10Be | 4 | 6 | 10,0135338(4) | 1,39×106 a | β− | 10B | 0+ |
| 11Be[n 4] | 4 | 7 | 11.021658(7) | 13,81(8) s | β− (97,1 %) | 11B | 1/2+ |
| β−, α (2,9 %) | 7Li | ||||||
| 12Be | 4 | 8 | 12,026921(16) | 21,49(3) ms | β− (99,48 %) | 12B | 0+ |
| β−, n (0,52 %) | 11B | ||||||
| 13Be | 4 | 9 | 13,03569(8) | 0,5(1) ns | n | 12Be | 1/2+ |
| 14Be[n 5] | 4 | 10 | 14,04289(14) | 4,84(10) ms | β−, n (81,0 %) | 13B | 0+ |
| β− (14,0 %) | 14B | ||||||
| β−, 2n (5,0 %) | 12B | ||||||
| 15Be | 4 | 11 | 15,05346(54)# | <200 ns | |||
| 16Be | 4 | 12 | 16,06192(54)# | <200 ns | 0+ | ||
- Isotopes stables en gras.
- Produit par la nucléosynthèse primordiale, mais non primordial car se désintégrant rapidement en 7Li
- Intermédiaire dans la réaction triple alpha de la nucléosynthèse stellaire produisant le 12C
- Possède un halo à un neutron.
- Possède un halo à 4 neutrons.
Remarques
- Les valeurs marquées # ne sont pas purement dérivées des données expérimentales, mais aussi au moins en partie à partir des tendances systématiques. Les spins avec des arguments d'affectation faibles sont entre parenthèses.
Notes et références
- Masse des isotopes depuis :
- (en) G. Audi, A. H. Wapstra, C. Thibault, J. Blachot and O. Bersillon, « The NUBASE evaluation of nuclear and decay properties », Nuclear Physics A, vol. 729, , p. 3–128 (DOI 10.1016/j.nuclphysa.2003.11.001, Bibcode 2003NuPhA.729....3A, lire en ligne [archive du ])
- Compositions isotopiques et masses atomiques standards :
- (en) J. R. de Laeter, J. K. Böhlke, P. De Bièvre, H. Hidaka, H. S. Peiser, K. J. R. Rosman and P. D. P. Taylor, « Atomic weights of the elements. Review 2000 (IUPAC Technical Report) », Pure and Applied Chemistry, vol. 75, no 6, , p. 683–800 (DOI 10.1351/pac200375060683, lire en ligne)
- (en) M. E. Wieser, « Atomic weights of the elements 2005 (IUPAC Technical Report) », Pure and Applied Chemistry, vol. 78, no 11, , p. 2051–2066 (DOI 10.1351/pac200678112051, résumé, lire en ligne)
- Demi-vie, spin et données sur les isomères sélectionnés depuis les sources suivantes :
- (en) G. Audi, A. H. Wapstra, C. Thibault, J. Blachot and O. Bersillon, « The NUBASE evaluation of nuclear and decay properties », Nuclear Physics A, vol. 729, , p. 3–128 (DOI 10.1016/j.nuclphysa.2003.11.001, Bibcode 2003NuPhA.729....3A, lire en ligne [archive du ])
- National Nuclear Data Center, Brookhaven National Laboratory. Information extracted from the NuDat 2.1 database (retrieved Sept. 2005).
- (en) N. E. Holden et D. R. Lide (dir.), CRC Handbook of Chemistry and Physics, CRC Press, , 85e éd., 2712 p. (ISBN 978-0-8493-0485-9, lire en ligne), « Table of the Isotopes », Section 11
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Isotopes of beryllium » (voir la liste des auteurs).
Voir aussi
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |