Ion nitrosonium
L’ion nitrosonium est l'oxycation NO+, dans lequel l'atome d'azote est lié à un atome d'oxygène par une triple liaison, le cation portant dans son ensemble une charge positive. On trouve généralement cet ion dans des sels :
- perchlorate de nitrosyle (NO)ClO4 ;
- acide nitrosylsulfurique (NO)SO4H ;
- tétrafluoroborate de nitrosyle (NO)BF4 ;
- octofluoroxénate de nitrosonium (NO)2XeF8.
| Ion nitrosonium | |
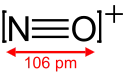 Structure de l'ion nitrosonium |
|
| Identification | |
|---|---|
| Nom UICPA | oxydoazote(1+) |
| Synonymes |
nitrilooxonium |
| No CAS | |
| ChEBI | 29120 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | NO [Isomères] |
| Masse molaire[1] | 30,006 1 ± 0,000 5 g/mol N 46,68 %, O 53,32 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Ces composés sont des oxydants forts, tout comme l'ion NO+ lui-même[2]. Les sels de perchlorate ClO4− et de tétrafluoroborate BF4− sont légèrement solubles dans l'acétonitrile CH3CN. Le tétrafluoroborate de nitrosyle (NO)BF4 peut être purifié par sublimation de 200 à 250 °C sous 0,01 mmHg (1,3 Pa).
L'ion nitrosonium NO+ est souvent confondu avec l'ion nitronium NO2+, agent actif des nitrations. Ces deux espèces sont pourtant bien différentes : le second est un électrophile plus efficace que le premier, ce qui est prévisible étant donné que l'ion nitronium est dérivé d'un acide fort, l'acide nitrique HNO3, tandis que l'ion nitrosonium dérive d'un acide faible, l'acide nitreux HNO2.
NO+ est isoélectronique avec le monoxyde de carbone CO et le diazote N2.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Neil G. Connelly et William E. Geiger, « Chemical Redox Agents for Organometallic Chemistry », Chemical Reviews, vol. 96, no 2, , p. 877-910 (PMID 11848774, DOI 10.1021/cr940053x, lire en ligne)