Fluorure d'uranyle
Le fluorure d'uranyle est un composé inorganique de la famille des oxyfluorures, de formule brute UO2F2. Il se présente sous forme d'un solide jaune cristallisé, hygroscopique, qui vire à l'orange en s'humidifiant. Il est stable jusqu'à environ 300 °C, température à laquelle il se décompose en octaoxyde de triuranium U3O8, difluor F2 et fluorure d'oxygène OF2.
| Fluorure d'uranyle | |
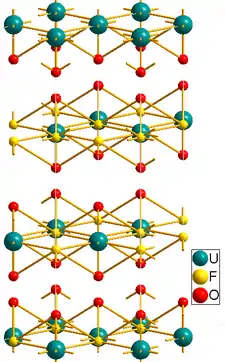
| |
| Structure cristalline du fluorure d'uranyle. | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.033.529 |
| No CE | 236-898-8 |
| Propriétés chimiques | |
| Formule | UO2F2 |
| Masse molaire[1] | 308,024 5 ± 0,000 6 g/mol F 12,34 %, O 10,39 %, U 77,28 %, |
| Propriétés physiques | |
| T° fusion | décomposition à 300 °C en U3O8, F2 et OF2[2] |
| Précautions | |
 Composé radioactif |
|
| SGH[3] | |
   Danger |
|
| Unités du SI et CNTP, sauf indication contraire. | |
C'est un intermédiaire dans la conversion de l'hexafluorure d'uranium UF6 en oxydes d'uranium et uranium métallique. Il résulte également de la réaction de l'humidité de l'air sur l'hexafluorure d'uranium : lorsque ce dernier est libéré par accident dans l'atmosphère, il forme du fluorure d'uranyle qu'on retrouve sur le sol sous forme de dépôts solides :
Cette réaction survient lorsque UF6 est aussi bien à l'état solide qu'à l'état gazeux, mais est bien entendu nettement plus rapide à l'état gazeux.
D'autres solides se forment, essentiellement des produits d'addition tels que des fluorures hydratés d'uranium et des hydrates de fluorure d'uranyle UO2F2·nH2O.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- International Bio-Analytical Industries, Inc.