Facteur déterminant des testicules
Le facteur déterminant du testicule (ou TDF), également connu comme sex-determining region Y (SRY), est une protéine de liaison à l'ADN (également connue sous le nom de protéine de régulation ou facteur de transcription) codée par le gène SRY. SRY est un gène du chromosome Y responsable de la détermination du sexe chez les Thériens (mammifères placentaires et marsupiaux)[1] ; les mutations dans ce gène conduisent à une gamme de Troubles du développement sexuel (DSD) avec différents effets sur le phénotype et le génotype.
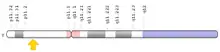
TDF est une protéine de liaison à l'ADN membre de la famille des SOX (SRY-like box). Lorsque complexé avec la protéine SF1 (en), TDF agit comme un facteur de transcription qui peut réguler d'autres facteurs de transcription, dont le plus important SOX9. Son expression provoque la différenciation des cellules de Sertoli qui vont former les cordons testiculaires primaires en encapsulant les cellules germinales (future tubes séminifères où se passe la spermatogenèse). Les cellules de Sertoli produisent l'hormone anti-Müllérienne et contrôlent la différenciation des cellules de Leydig qui vont commencer à sécréter la testostérone[2]. Le gène SRY commence à s'exprimer normalement entre 6 et 8 semaines après la formation du fœtus, et inhibe le développement de la gonade en ovaire.
Évolution du gène et régulation
L'évolution
SRY peut avoir surgi à partir d'une duplication du gène SOX3 lié au chromosome X, un membre de la famille Sox[3] Cette duplication est survenue après la scission entre les monotrèmes et les Thériens. Les monotrèmes n'ont pas de gène SRY et de certains de leurs chromosomes sexuels présentent des homologies avec ceux des oiseaux[4]. Le gène SRY subit des mutations rapides et la régulation de son expression est difficile à étudier parce que la détermination du sexe n'est pas un phénomène très conservé dans le règne animal[5].
Régulation
La souris constitue le principal animal modèle utilisé pour l'étude du gène SRY. La compréhension de la régulation de son expression est complexe car même au sein des espèces mammifères, sa séquence protéique est très peu conservée. Le seul groupe conservé entre la souris et les autres mammifères est la région qui est responsable de la liaison à l'ADN (HMG-box). Des mutations dans cette région peuvent causer un renversement de sexe, où le sexe gonadique est opposé au sexe génétique[6]. La région promotrice de SRY étant elle aussi peu conservée et ses éléments régulateurs restent mal connus. Une région de 400 à 600 paires de bases (pb) en amont du site d'initiation de la transcription présente des homologies dans des groupes de mammifères proches. Les études in vitro du promoteur humain de SRY ont montré qu'une région d'au moins 310 pb en amont du site d'initiation de la transcription est nécessaire pour l'expression du gène. Il a aussi été montré que la liaison de trois facteurs de transcription (SF1, Sp1 et WT1) sur le promoteur du gène humain, influence de l'expression de SRY[6].
Il existe également des preuves que les protéines GATA4 et FOG2 contribuent à l'activation de SRY en s'associant avec son promoteur. Leur mode de fonctionnement n'est pas clair, mais l'induction de mutations sur les gènes FOG2 et GATA4 produit des niveaux de transcription de SRY significativement plus bas[7] Des études suggèrent que FOG2 et GATA4 pourraient s'associer avec des protéines de remodelage des nucléosomes pour activer SRY[8].
Fonction
Pendant la gestation, les cellules mères des gonades qui se trouvent le long de la crête génitale sont dans un état bipotentiel, ce qui signifie qu'elles possèdent la capacité de devenir des cellules testiculaires (des cellules de Sertoli et de Leydig) ou ovariennes (cellules de la granulosa et de cellules de la thèque). SRY dirige la différenciation des testicules par l'activation des facteurs de transcription spécifiques tel que SOX9, un facteur de transcription avec un site de liaison à l'ADN très similaire à SRY. SOX9 active à son tour l'expression d'un facteur de croissance (Fgf9), qui lui-même entraîne une régulation à la hausse de SOX9. Une fois que le bon niveau d'expression de SOX9 est atteint, les cellules bipotentielles se différencient en cellules de Sertoli[9].
Influence sur le sexe
Les embryons se développent de façon identique, quel que soit le sexe génétique, jusqu'à un certain point dans le développement durant lequel les gonades se différencient en ovaires ou en testicules en fonction de la présence ou de l'absence du chromosome Y. Par conséquent, SRY joue un rôle important dans la détermination du sexe. Un mâle typique possède un caryotype XY. Les personnes qui héritent d'un chromosome Y normal et de plusieurs chromosomes X sont toujours de sexe masculin (comme dans le syndrome de Klinefelter, qui a un caryotype XXY). Des recombinaisons génétiques atypiques au cours de croisements (crossing-over) lors du développement du spermatozoïde peuvent entraîner des caryotypes qui ne correspondent pas à leur expression phénotypique.
La plupart du temps, lorsqu'un spermatozoïde a subi un crossing-over au cours de sa méiose, le gène SRY reste sur le chromosome Y. S'il est transféré au chromosome X, cependant, le chromosome Y n'aura pas de gène SRY et ne peut plus lancer le développement des testicules. Les descendants qui héritent de ce chromosome Y auront le syndrome de Swyer, caractérisé par un caryotype XY et un phénotype femelle. Le chromosome X résultant de ce crossing-over a maintenant un gène SRY, et donc la capacité à initier le développement des testicules. Les descendants qui héritent de ce chromosome X vont avoir une condition appelée syndrome du mâle XX, caractérisé par un caryotype XX, et un phénotype mâle. Alors que la plupart des XX les mâles développent des testicules, certains peuvent présenter une différentiation gonadique incomplète, où les gonades présenteront à la fois des caractéristiques testiculaires et ovariennes (ovotestis). Le syndrome du mâle XX est infertile, probablement à cause de l'inactivation (aléatoire ou non aléatoire) du chromosome X contenant le gène SRY dans certaines cellules[10].
Tandis que la présence ou l'absence de SRY détermine généralement le développement des testicules, il a été suggéré qu'il existe d'autres facteurs qui affectent la fonctionnalité de SRY[11] Des personnes ayant le gène SRY se développent en tant que femmes, soit parce que le gène lui-même est défectueux ou muté, ou parce que l'un des facteurs qui l'activent est défectueux[12]. Cela peut se produire chez les personnes présentant des caryotype XY, XXY, ou XX SRY-positif.
Voir aussi
Articles connexes
Références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Testis determining factor » (voir la liste des auteurs).
- Wallis MC, Waters PD, Graves JA, « Sex determination in mammals - Before and after the evolution of SRY », Cell. Mol. Life Sci., vol. 65, no 20, , p. 3182–95 (PMID 18581056, DOI 10.1007/s00018-008-8109-z)
- Mittwoch U, « The race to be male », New Scientist, vol. 120, no 1635, , p. 38–42
- Katoh K, Miyata T, « A heuristic approach of maximum likelihood method for inferring phylogenetic tree and an application to the mammalian SOX-3 origin of the testis-determining gene SRY », FEBS Lett, vol. 463, nos 1–2, , p. 129–32 (PMID 10601652, DOI 10.1016/S0014-5793(99)01621-X)
- Veyrunes F, Waters PD, Miethke P, Rens W, McMillan D, Alsop AE, Grützner F, Deakin JE, Whittington CM, Schatzkamer K, Kremitzki CL, Graves T, Ferguson-Smith MA, Warren W, Marshall Graves JA, « Bird-like sex chromosomes of platypus imply recent origin of mammal sex chromosomes », Genome Res., vol. 18, no 6, , p. 965–73 (PMID 18463302, PMCID 2413164, DOI 10.1101/gr.7101908)
- Bowles J, Schepers G, Koopman P, « Phylogeny of the SOX family of developmental transcription factors based on sequence and structural indicators », Dev Biol, vol. 227, no 2, , p. 239–55 (PMID 11071752, DOI 10.1006/dbio.2000.9883)
- Ely D, Underwood A, Dunphy G, Boehme S, Turner M, Milsted A, « Review of the Y chromosome, Sry and hypertension », Steroids, vol. 75, no 11, , p. 747–53 (PMID 19914267, PMCID 2891862, DOI 10.1016/j.steroids.2009.10.015)
- Knower KC, Kelly S, Harley VR, « Turning on the male--SRY, SOX9 and sex determination in mammals », Cytogenet. Genome Res., vol. 101, nos 3-4, , p. 185–98 (PMID 14684982, DOI 10.1159/000074336, lire en ligne [archive du ])
- Theodore Friedman, Advances in Genetics Vol 76, 108, Elsevier Inc, (lire en ligne)
- https://www.ncbi.nlm.nih.gov/pubmed/25246082
- Margarit E, Coll MD, Oliva R, Gómez D, Soler A, Ballesta F, « SRY gene transferred to the long arm of the X chromosome in a Y-positive XX true hermaphrodite », Am. J. Med. Genet., vol. 90, no 1, , p. 25–8 (PMID 10602113, DOI 10.1002/(SICI)1096-8628(20000103)90:1<25::AID-AJMG5>3.0.CO;2-5)
- Polanco JC, Koopman P, « Sry and the hesitant beginnings of male development », Dev. Biol., vol. 302, no 1, , p. 13–24 (PMID 16996051, DOI 10.1016/j.ydbio.2006.08.049)
- Biason-Lauber A, Konrad D, Meyer M, DeBeaufort C, Schoenle EJ, « Ovaries and female phenotype in a girl with 46,XY karyotype and mutations in the CBX2 gene », Am. J. Hum. Genet., vol. 84, no 5, , p. 658–63 (PMID 19361780, PMCID 2680992, DOI 10.1016/j.ajhg.2009.03.016)