ETBE
L’ETBE, ou éther éthyle tertiobutyle (en anglais : ethyl tert-butyl ether), est un additif pour carburant oxygéné couramment utilisé dans la production d'essence à partir de pétrole brut. Constituant avec l'éthanol de la filière biocarburant essence, il présente des propriétés égales ou supérieures à celles de l'éthanol, et est plus facile à mettre en œuvre d'un point de vue technique et logistique. En particulier, contrairement à l'éthanol, il ne favorise pas l'évaporation des carburants et n'absorbe pas l'humidité de l'air. Il est une alternative au méthyl tert-butyl éther (MTBE).
| Éther éthyle tertiobutyle (ETBE) | |
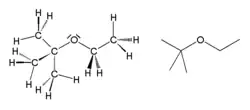 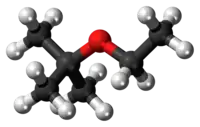 Structure de l'éther éthyle tertiobutyle (ETBE). |
|
| Identification | |
|---|---|
| Synonymes |
|
| No CAS | |
| No ECHA | 100.010.282 |
| No CE | 211-309-7 |
| PubChem | |
| Apparence | Liquide incolore |
| Propriétés chimiques | |
| Formule | C6H14O [Isomères] |
| Masse molaire[1] | 102,174 8 ± 0,006 1 g/mol C 70,53 %, H 13,81 %, O 15,66 %, |
| Propriétés physiques | |
| T° fusion | −94 °C[2] |
| T° ébullition | 73 °C[2] |
| Solubilité | 12 g·L-1 (25 °C)[2] |
| Masse volumique | 0,74 g·cm−3[2] |
| Point d’éclair | −19 °C |
| Pression de vapeur saturante | 173 hPa (25 °C)[2] |
| Précautions | |
| Directive 67/548/EEC | |
 Xi  F |
|
| Composés apparentés | |
| Isomère(s) | Hexanol |
| Autres composés | |
| Unités du SI et CNTP, sauf indication contraire. | |
Production
La synthèse de l'ETBE est réalisée par addition catalytique d'éthanol sur l'isobutène :
.png.webp)
Théoriquement, il faut 45 g d'éthanol pour produire 100 g d'ETBE. Cependant, dans la pratique, il faut presque 50 g d'éthanol pour obtenir 100 g d'ETBE.
L'Institut français du pétrole (IFP), dès le début des années 1990, s'est impliqué dans la mise au point et le développement d'un procédé de production d'ETBE. La tension de vapeur des mélanges essence/ETBE est plus faible que celle des mélanges essence/éthanol, et répond ainsi aux spécifications des essences. Ces travaux se sont traduits par la construction en France par Total de trois unités industrielles de fabrication d'ETBE (production globale de 200 000 tonnes par an).
Utilisation
L'ETBE peut être incorporé jusqu'à 22 % (normes EN228) en volume dans l'essence. Bien qu'il présente des propriétés supérieures à celles de l'éthanol, le gouvernement français a incité début 2007 à développer la filière E85 (85 % d'éthanol dans l'essence). Le mélange éthanol/essence présente un certain nombre d'inconvénients, notamment un plus faible pouvoir de combustion que l'ETBE, mais ce dernier est très soluble dans l'eau et de faible biodégradabilité[3], ce qui en fait un polluant problématique pour les nappes aquifères[4].
Volatilité
Concernant les problèmes de volatilité, l'éthanol est moins volatil que l'ETBE (températures d'ébullition respectives : 78 °C et 73 °C). Cependant, l'éthanol forme des azéotropes avec les fractions légères de l'essence, augmentant ainsi la volatilité des mélanges éthanol/essence, comparativement aux mélanges ETBE/essence.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Ethyl-tert-butylether » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 03/01/2009 (JavaScript nécessaire)
- Cédric Malandain, Les gènes eth responsables de l’oxydation de l’éthyl tert-butyl éther (ETBE) : fonctionnalité, régulation et application (thèse), 21 décembre 2007.
- Comme l'ont illustré les récentes difficultés rencontrées dans l'agglomération bordelaise, dont le réseau d'adduction a dû être en grande partie vidangé (cf. ce reportage)