Dihydroergotamine
La dihydroergotamine est un médicament dérivé de l'ergot de seigle principalement utilisé dans le traitement de la migraine qui a été introduit dans les années 1970, sous la marque Séglor et Ikaran. Elle est utilisée également au long cours dans le traitement de l'hypotension, en particulier l'hypotension secondaire aux neuroleptiques, et comme traitement de fond antimigraineux. Elle est administrée par voie nasale (spray), orale ou injectable et présente une efficacité similaire au sumatriptan.
| Dihydroergotamine | |
| |
| Identification | |
|---|---|
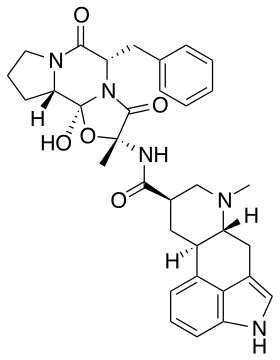
| Nom UICPA | (2R,4R,7R)-N-[(1S,2S,4R,7S)-7-benzyl-2-hydroxy-4-methyl-5,8-dioxo-3-oxa-6,9-diazatricyclo[7.3.0.02,6]dodecan-4-yl]-6-methyl-6,11-diazatetracyclo[7.6.1.02,7.012,16]hexadeca-1(16),9,12,14-tetraene-4-carboxamide |
| No CAS | |
| No ECHA | 100.007.386 |
| Code ATC | N02 |
| DrugBank | DB00320 |
| Propriétés chimiques | |
| Formule | C33H37N5O5 [Isomères] |
| Masse molaire[1] | 583,677 4 ± 0,031 5 g/mol C 67,91 %, H 6,39 %, N 12 %, O 13,71 %, |
| Données pharmacocinétiques | |
| Excrétion | |
| Unités du SI et CNTP, sauf indication contraire. | |
Elle agit en provoquant une constriction des vaisseaux sanguins cérébraux, ce qui diminue la douleur provoquée par la migraine.
En cas de surdosage peuvent apparaître des symptômes d'ergotisme : accident ischémique des extrémités (favorisé par l'association avec les antibiotiques de la famille des macrolides).
Elle produit des atteintes valvulaires cardiaques selon le même mécanisme que le Benfluorex (Médiator), ainsi que des fibroses rétro-péritonéales.
Suspension de la délivrance en France
L'Agence nationale de sécurité du médicament et des produits de santé (ANSM) a suspendu l'autorisation de mise sur le marché (AMM) des produits contenant de la dihydroergotamine le 24 septembre 2013[2]. En effet, une évaluation européenne des médicaments contenant de la dihydroergotamine, dihydroergocristine, dihydroergocryptine-caféine et nicergoline a été réalisée par le comité des médicaments à usage humain (CHMP). Les produits dérivés ergotés indiqués dans le traitement aigu de la crise de migraine ne sont pas concernés.
La survenue de cas graves de fibrose et d’ergotisme identifiés par les autorités sanitaires françaises avec ces dérivés ergotés a déclenché cette évaluation. Celle-ci a mis en évidence une efficacité limitée des quatre substances actives précitées avec des risques qui ne sont plus contrebalancés par leurs bénéfices. Ces dérivés ergotés ne doivent donc plus être utilisés et vont faire prochainement l’objet d’une suspension d’AMM et d’un rappel de lots[2].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Suspension d’AMM des médicaments par voie orale contenant : dihydroergotamine, dihydroergocristine, dihydroergocryptine-caféine, nicergoline - Lettre aux professionnels de santé », sur ansm.sante.fr,
Voir aussi
| Dihydrogotamine | |
| Informations générales | |
|---|---|
| Princeps |
|
| Identification | |
| DCI | 2022 |
| No CAS | |
| No ECHA | 100.007.386 |
| Code ATC | N02CA01 |
| DrugBank | 00320 |
Liens externes
- Compendium suisse des médicaments : spécialités contenant Dihydroergotamine