Cacodyle
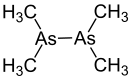
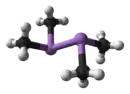
Le cacodyle ou tétraméthyldiarsane est un composé organique contenant de l'arsenic, un alkylarsine de formule semi-développée (CH3)2As-As(CH3)2. C'est un liquide huileux toxique avec une odeur d'ail. Le cacodyle subit une combustion spontanée dans l'air sec. C'est aussi une partie minoritaire du liquide fumant de Cadet (d'après le chimiste français Louis Claude Cadet de Gassicourt).
| Cacodyle | |||
  |
|||
| Identification | |||
|---|---|---|---|
| Nom UICPA | diméthylarsanyl(diméthyl)arsane tétraméthyldiarsane |
||
| Synonymes |
tétraméthyldiarsine |
||
| No CAS | |||
| No ECHA | 100.006.766 | ||
| No CE | 207-440-4 | ||
| PubChem | 79018 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide huileux avec une odeur piquante | ||
| Propriétés chimiques | |||
| Formule | C4H12As2 [Isomères] |
||
| Masse molaire[1] | 209,981 3 ± 0,004 1 g/mol C 22,88 %, H 5,76 %, As 71,36 %, |
||
| Propriétés physiques | |||
| T° fusion | −5 °C[2] | ||
| T° ébullition | 163 °C[2] | ||
| Précautions | |||
| SGH[2] | |||
 |
|||
| Transport[2] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
Préparation
L'oxyde de cacodyle, (CH3)2AsOAs(CH3)2 est préparé par la réaction de l'acétate de potassium avec du trioxyde d'arsenic :
- 4 KCH3CO2 + As2O3 → OAs2(CH3)4 + 2 K2CO3 + 2 CO2
Une réduction ultérieure ou dismutation de ce composé dans une réaction chimique donne un mélange de plusieurs composés de l'arsenic méthylé dont le tétraméthyldiarsane.
Une autre synthèse beaucoup plus efficace fait réagir du chlorure de diméthylarsine, Cl-As(CH3)2 et du diméthylarsine, HAs(CH3)2 :
- As(CH3)2Cl + As(CH3)2H → As2(CH3)4 + HCl
Histoire

Jöns Jacob Berzelius a inventé le nom de kakodyl (plus tard changé en cacodyl) pour le radical diméthylarsinyle, (CH3)2As-, à partir des racines grecques kakodes, « nauséabond » et hyle « matière »[3].
Le cacodyle, initialement fabriqué à partir de l'arsenic distillé avec de l'acétate de potassium, a été étudié par Edward Frankland et Robert Bunsen. Il est considéré comme l'un des premiers composés organométalliques découverts.
En 1836, Robert Bunsen en dit : « l'inhalation de ce corps produit des picotements instantanés des mains et des pieds, et même vertige et insensibilité… Il est remarquable que lorsque l'on inhale ce composé, la langue se couvre d'une couche noire, avant même qu'aucun des autres effets délétères ne soit perceptible ».
Ces travaux de Bunsen sur le cacodyle l'ont conduit à postuler l'existence du radical méthyle.
Utilisation
Le cacodyle a aussi été utilisé pour prouver la théorie radicale de Berzelius, qui a entraîné à une large utilisation de cacodyle dans les laboratoires de recherche. Après que la théorie radicale a été établie, l'intérêt pour cette substance toxique à mauvaise odeur a fortement diminué.
Pendant la Première Guerre mondiale, l'utilisation de cacodyle parmi les gaz de combat a été envisagée, mais en fin de compte, elle n'a jamais été utilisée pendant cette guerre. Plus récemment, la chimie inorganique a découvert les propriétés du cacodyle comme ligand des métaux de transition.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Cacodyl » (voir la liste des auteurs).
- John H. Burns and Jürg Waser, The Crystal Structure of Arsenomethane., J. Am. Chem. Soc., 1957, vol. 79(4), p. 859–864. DOI 10.1021/ja01561a020.
- Dietmar Seyferth, Cadet's Fuming Arsenical Liquid and the Cacodyl Compounds of Bunsen, Organometallics, 2001, vol. 20(8), p. 1488–1498.DOI 10.1021/om0101947.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Tetramethyldiarsine » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais) (JavaScript nécessaire)
- J. J. Berzelius, Jahresber., 1839, vol.18, p. 487.
