Bromure de magnésium
Le bromure de magnésium (MgBr2) est un composé inorganique du magnésium et de bromure.
| Bromure de magnésium | |
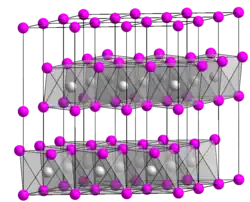
| |
| __ Mg2+ __ Br− | |
| Identification | |
|---|---|
| Nom UICPA | Bromure de magnésium |
| No CAS | |
| No ECHA | 100.029.246 |
| No CE | 232-170-9 |
| PubChem | 82241 |
| Apparence | solide blanc |
| Propriétés chimiques | |
| Formule | MgBr2 |
| Masse molaire[1] | 184,113 ± 0,003 g/mol Br 86,8 %, Mg 13,2 %, |
| Propriétés physiques | |
| T° fusion | 711 °C[2] |
| Solubilité | 1 015 g·l-1 (eau, 20 °C) Légèrement soluble dans l'alcool[3] |
| Masse volumique | 3,72 g·cm-3 (25 °C)[2] |
| Cristallographie | |
| Système cristallin | trigonal |
| Symbole de Pearson | hP3 |
| Classe cristalline ou groupe d’espace | P3m1, n° 164 |
| Précautions | |
| SGH[2] | |
 |
|
| NFPA 704 | |
| Unités du SI et CNTP, sauf indication contraire. | |
Propriétés
Le bromure de magnésium se présente sous la forme d'un solide blanc hygroscopique. Il est soluble dans l'eau et légèrement soluble dans l'éthanol.
Occurrence
Le bromure de magnésium est naturellement présent en petites quantités dans certains minéraux, tels que la bischofite et la carnallite. Il est aussi présent dans l'eau de mer (à une concentration d'environ 70 g m3[4], d'où il peut être obtenu par évaporation. Il est particulièrement présent dans l'eau de la mer Morte[5] - [6].
Synthèse
Le bromure de magnésium peut être synthétisé de diverse façon par réaction entre composés du magnésium et du brome, en particulier l'acide bromhydrique. On peut notamment citer
- la réaction avec l'hydroxyde de magnésium (obtenu à partir du chlorure de magnésium) :
- Mg(OH)2 + 2 HBr → MgBr2 + 2 H2O
- la réaction avec l'oxyde de magnésium, où le produit final est obtenu par cristallisation[6] :
- MgO + 2 HBr → MgBr2 + H2O
- la réaction avec le carbonate de magnésium. Dans ce cas le produit est le solide recueilli après évaporation[5] :
- MgCO3 + 2 HBr → MgBr2 + H2O +CO2
Il est également possible de le produire directement à partir de magnésium métallique et de dibrome. C'est réaction doit se passer dans l'éther anhydre, car sinon la réaction lors de l'ajout de dibrome est violente.
- Mg + Br2 → MgBr2
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé Magnesium bromide, consultée le 14 novembre 2015.
- « Fiche du composé Magnesium bromide », sur Acros (consulté le ).
- (de) article « Brom » sur Seilnacht.
- Gruyter, W. Concise Encyclopedia Chemistry, Walter de Gruyter & Company: Berlin, 1993; 612
- Lewis, R.J. Hawley’s Condensed Chemical Dictionary, 15th ed.; John Wiley &Sons Inc.:New York, 2007; 777
