Amphimedon queenslandica
Amphimedon queenslandica est une espèce d'éponges (Porifera) appartenant à la classe des démosponges.

Elle est présente au sein de la Grande Barrière de corail près de l’Australie, et se développe sur le corail mort dans les zones où l’eau est peu profonde. Son squelette est riche en spongine mais contient peu de microsclères[2].
Son génome a été séquencé en 2009 et depuis elle est considérée comme un animal modèle pour la recherche concernant la biologie évolutive du développement[3].
Le génome d’Amphimedon queenslandica contient plusieurs gènes codant des facteurs de transcription ou encore des gènes impliqués dans l’indication du patron de développement. Son répertoire de gènes indique que l’ancêtre des métazoaires possédait déjà un bagage semblable à celui des bilatériens plus modernes[3]. Amphimedon queenslandica produit également un nombre important d’embryons et de larves tout au long de l’année ce qui représente un atout important lorsque vient le temps de choisir un animal pour étudier l’ADN[2].
Amphimedon queenslandica et l'évolution de la complexité
Les éponges sont des organismes de choix pour les scientifiques qui étudient l’origine des processus ayant mené à la multicellularité chez les métazoaires, puisqu’elles sont considérées comme étant les métazoaires les plus anciens. Bien que l’absence d’un système nerveux ainsi que d’un intestin ait relégué les éponges au stade de Parazoaire, elles restent pertinentes puisqu’elles possèdent des gènes clés responsables du patron de développement et de la signalisation et leur embryon très similaire à celui des animaux. Il y a aussi plusieurs gènes conservés chez les animaux qui ne sont pas présents dans le génome d’A. queenslandica, cela indique qu’il y a eu une expansion du génome des animaux à la suite de leur divergence avec les éponges ou bien une perte de gènes chez ceux-ci, ces gènes étant probablement liés à la complexité des organismes[3].
Le génome de A. queenslandica donne des informations sur les six éléments importants qui sont associés à la multicellularité chez les métazoaires soit :
- La régulation du cycle cellulaire et de la croissance
- La mort cellulaire programmée
- L’adhésion cellule-cellule et cellule-matrice
- La signalisation du développement et la régulation des gènes
- La reconnaissance du soi
- La différentiation cellulaire
Régulation du cycle cellulaire et de la croissance
Les principaux éléments impliqués dans la machinerie cellulaire et le cycle cellulaire étaient présents chez les premiers organismes eucaryotes, cependant, certains mécanismes de grande importance sont apparus beaucoup plus récemment. Par exemple, les gènes codant les protéines p53, p63 et p73 qui sont impliqués dans la suppression de tumeurs sont présents chez tous les organismes eucaryotes (unicellulaires et multicellulaires), par contre, la kinase HIPK qui phosphoryle p53 et la ligase ubiquitine MDM2 qui régule p53 sont plutôt spécifique aux métazoaires (qui sont multicellulaires)[3].
Apoptose et mort cellulaire programmée
Contrairement aux composants de la machinerie cellulaire et régulateurs du cycle cellulaire, les processus menant à la mort programmée des cellules sont une caractéristique unique aux animaux et ces processus se complexifient, plus l’animal chez lequel il se trouve est complexe (plus complexe chez les animaux bilatériens). En effet, chaque processus responsable de la mort programmée des cellules (extrinsèque et intrinsèque) nécessite la présence de caspases qui sont dans les faits une famille de cystéines protéases et spécifique aux métazoaires. A. queenslandica possède en son génome le matériel génétique nécessaire pour les initiateurs de caspases avec les domaines de recrutement et précurseurs de mort caractéristiques de ceux-ci[3].
Adhésion cellule-cellule et cellule-matrice
Chez Monosiga (un choanoflagellé unicellulaire), les domaines de deux familles de protéines responsables de l’adhésion entre cellules sont présents, il s’agit des cadhérines et des immunoglobulines. Chez A. queenslandica, les cadhérines sont différentes et possèdent une architecture qui est propre aux cadhérines retrouvées chez les métazoaires. Les récepteurs extracellulaires intégrines a et b sont présents chez A. queenslandica et les autres métazoaires, mais sont absents chez Monosiga et les autres organismes eucaryotes qui ne font pas partie des métazoaires ce qui laisse croire qu’ils sont présents seulement chez les organismes multicellulaires[3].
Signalisation développementale et transcription
Il y a plusieurs différences entre les éponges comme A. queenslandica et le reste des métazoaires qui semblent être dues à la différence dans la complexité de la morphologie. En effet, les éponges ne semblent pas posséder de mésoderme, l’étude du génome d’A. queenslandica vient corroborer cette hypothèse puisque celui-ci ne possède pas de gènes codant les facteurs de transcription impliqués dans le développement du mésoderme. Cependant, elles possèdent les facteurs transcription qui sont nécessaires à la différentiation des muscles et nerfs, même si elles sont dépourvues de système nerveux. A. queenslandica est par contre dépourvue de certains gènes Hox et autres facteurs de transcription impliqués dans la formation du système nerveux et dans le patron de développement[3].
Reconnaissance du soi et immunité innée
L’évolution de la multicellularité est associée à l’apparition de mécanismes de défense pour éviter l’entrée de pathogènes. L’analyse du génome d’A. queenslandica a permis de conclure que bien que certains gènes de l’immunité aient été présents tôt dans l’évolution des organismes eucaryotes, il reste que la plupart de ces gènes sont propres aux animaux et sont apparus plus tard dans l’évolution comme les récepteurs Toll-like et les récepteurs interleukin-1.
Le génome d’A. queenslandica encode des facteurs d’agrégation qui permettent l’adhésion entre cellules et pourraient être impliqués dans la reconnaissance du soi (immunologie). La présence de plusieurs gènes reliés à l’agrégation chez A. queenslandica indique que la reconnaissance du soi pourrait être sous le contrôle d’une famille multigénique[3].
Différenciation cellulaire
Chez les éponges, les cellules se regroupent pour former une couche semblable à un tissu, mais ce n’en est pas un. La formation d’un vrai tissu épithélial, qui implique l’alignement de cellules avec une polarité, des jonctions et la formation d’une membrane basale, semble être une innovation des eumétazoaires. A. queenslandica, possède quelques protéines reconnues comme étant spécifiques aux métazoaires et jouant un rôle dans la détermination de la polarité des cellules épithéliales, le reste de la machinerie est apparu plus tard dans l’évolution chez les organismes plus complexes[3].
Évolution des protéines qui lient l'ARN (RNA binding proteins)
Les protéines liant l’ARN (RBP ou RNA binding proteins) jouent un rôle important dans plusieurs processus biologique, comme la régulation de l’expression des gènes. Les RBP ont été étudiées dans plusieurs organismes, mais on en connait peu sur la façon dont ont évolué ces protéines. Il y a un bon nombre de RBP qui ont été identifiées chez A. queenslandica ce qui peut donner une idée sur la forme et la fonction que prenait ces protéines lors de leur émergence chez un organisme basal comme A. queenslandica.
La plupart des protéines qui lient l’ARN sont apparues avant la divergence entre les eumétazoaires et les éponges. Plusieurs RBP jouent un rôle crucial dans la régulation des processus et du développement des organismes bilatérales, mais chez les éponges elles ne sont pas d’une si grande importance. Cela laisse croire que les RBP, lorsqu’elles sont apparues, avaient un autre rôle ancestral qui diffère de celui joué chez les bilatériens du présent. Même si le rôle des RBP diffère selon l’espèce, elles restent importantes pour la multicellularité, comme le prouve la conservation d’environ 200 RBP chez différentes lignées d’animaux qui sont séparés depuis plusieurs millions d’années ce qui suggère que ces protéines ont joué un rôle important dans le maintien de la multicellularité depuis son origine[4].
Expression de Wnt et TGF-β chez Amphimedon queenslandica
Les mécanismes d’adhésion entre cellules et de coopération cellulaire étaient une condition clé à respecter dans l’évolution des métazoaires, cependant, l’évolution de ces mécanismes est plus ou moins bien connue bien que certains éléments impliqués durant le développement embryonnaire ait été retrouvé chez plusieurs types d’éponges. L’étude du génome d’A. queenslandica et de l’expression des gènes Wnt et TGF-β durant le développement embryonnaire constitue un pas en avant vers la compréhension des systèmes de détermination du patron de développement présents chez le dernier ancêtre commun des eumétazoaires[5].
Les gènes Wnt et TGF-β sont impliqués dans le développement des organismes, dans l’organisation du patron de développement et ils sont exprimés durant le développement embryonnaire de A. queenslandica ce qui sous-entend que ces gènes sont apparus avant la divergence entre les éponges et les eumétazoaires. Chez A. queenslandica, l’expression tôt de ces gènes dans le développement laisse croire qu’ils jouent un rôle dans la détermination de la polarité axiale. Lorsque l’embryon d’A queenslandica commence à présenter un axe postérieur-antérieur, l’expression de Wnt est surtout dans le pôle postérieur tandis que TGF-β est exprimé au pôle antérieur[5].
Wnt et TGF-β semblent agir ensemble pour moduler le patron de développement des cellules et ce depuis le dernier ancêtre commun à tous les métazoaires. Selon toute vraisemblance, le dernier ancêtre commun de tous les métazoaires existants possédait donc la capacité de former des structures complexes[5].
Répertoire de RCPG chez Amphimedon queenslandica
A. queenslandica possède un grand répertoire de récepteurs couplés aux protéines G ou RCPG (G protein-coupled receptor ou GPCR), environ 220, ces protéines appartiennent à quatre familles : Glutamate, Rhodopsine, Adhesion et Frizzled. Il y a peu de séquences orthologues lorsqu’on compare les protéines de la famille Rhodopsine de cette éponge avec ceux retrouvées chez les eumétazoaires et les bilatériens. Les RCPG de type Rhodopsine ont donc considérablement divergé de ceux retrouvés chez les autres métazoaires basaux.
A. queenslandica possède plusieurs RCPG de type Adhésion, soit environ 40. Cela représente l’une des premières expansions de ce type de récepteur dans l’évolution des métazoaires. L’expansion de ces récepteurs très tôt dans l’évolution des métazoaires a probablement été causé par l’évolution de la multicellularité chez les premiers métazoaires, car la capacité d’adhésion entre cellules est une composante primordiale de la multicellularité. Un autre fait intéressant par rapport à cette famille de RCPG est qu’au moins huit de ses représentantes possèdent un domaine de liaison à une hormone (hormon binding motif ou HRM domain), cependant il n’y a pas de signe d’hormones chez les porifères[6].
Évolution de la gastrulation
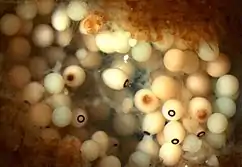
Pendant le développement d’A. queenslandica, les couches de cellules qui se forment lors de l’embryogénèse n’ont pas de relations avec les couches de cellules qui sont présentes au stade juvénile. Malgré le manque de détermination d’identité cellulaire et de stabilité dans cette éponge, le facteur de transcription GATA est exprimé de manière constante dans les couches de cellules interne de l’éponge. Ce facteur de transcription est hautement conservé chez les eumétazoaires et est un marqueur endo mésodermique. Néanmoins, il semble que les couches cellulaires des éponges ne soient pas homologues à ceux des eumétazoaires. L’expression du facteur de transcription GATA dans les couches internes de l’éponge suggère une relation ancestrale avec l’endo mésoderme des eumétazoaires et que le rôle ancestral de GATA dans la signalisation des cellules des couches internes, précéderait l’origine des différents feuillets embryonnaires (endoderme, mésoderme, ectoderme). La gastrulation et la formation des feuillets embryonnaires est donc apparue tôt dans l’évolution des eumétazoaires après leur divergence avec les porifères et ce, à partir de processus de développement préexistants qui étaient utilisés pour la signalisation simple des cellules chez les premiers animaux multicellulaires. L’évolution des gènes permettant la détermination des feuillets cellulaires est le résultat de l’émergence de couches cellulaires primitives et de mécanismes contrôlant cette ségrégation des cellules. La majorité des gènes jouant un rôle dans la gastrulation chez les eumétazoaires ainsi que dans la détermination des feuillets cellulaires, sont apparues après la divergence des eumétazoaires et des porifères. Le fait que le facteur de transcription GATA soit exprimé chez tous les métazoaires ainsi que les ligands pour Wnt et TGF-β, laisse croire que ces gènes étaient essentiels dans le développement des premiers animaux, ils devaient jouer un rôle critique dans la transmission d’informations concernant le positionnement des cellules. La combinaison de ces gènes avec de nouveaux gènes apparus plus tard chez les eumétazoaires, a permis la spécification des couches cellulaire et l’émergence des feuillets cellulaires tel qu’on les connait aujourd’hui chez les eumétazoaires[7].
Notes et références
- Catalogue of Life Checklist, consulté le 25 janvier 2018
- N.A. John, Rob Hooper et W.M. Van Soest, A new species of Amphimedon (Porifera, Demospongiae, Haplosclerida, Niphatidae) from the Capricorn-Bunker Group of Islands, Great Barrier Reef, Australia: target species for the sponge genome project, Zootaxa Magnolia Press no 1314, 2006, p. 31-39.
- M. Srivastava, O. Simakov, J. Chapman, B. Fahey, M. Gauthier, T. Mitros, et al., The Amphimedon queenslandica genome and the evolution of animal complexity, Nature, 466 (7307), 2010 : 720-726.
- P. Kerner, S. Degnan, L. Marchand, B. Degnan, M. Vervoort, Evolution of RNA-Binding Proteins in Animals: Insights from Genome-Wide Analysis in the Sponge Amphimedon queenslandica, Molecular Biology And Evolution, 28 (8), 2011 : 2289-2303.
- M. Adamska, S. Degnan, K. Green, M. Adamski, A. Craigie, C. Larroux, B. Degnan, Wnt and TGF-β Expression in the Sponge Amphimedon queenslandica and the Origin of Metazoan Embryonic Patterning, Plos ONE, 2 (10), : e1031.
- A. Krishnan, R. Dnyansagar, M. Almén, M. Williams, R. Fredriksson, N. Manoj, H. Schiöth, The GPCR repertoire in the demosponge Amphimedon queenslandica: insights into the GPCR system at the early divergence of animals, BMC Evolutionary Biology, 14 (1), 2014.
- N. Nakanishi, S. Sogabe, B. Degnan, Evolutionary origin of gastrulation: insights from sponge development, BMC Biology, 12 (1), 2014 : 26.
Référence taxonomiques
- (en) Référence Animal Diversity Web : Amphimedon queenslandica (consulté le )
- (en) Référence BioLib : Amphimedon queenslandica Hooper & van Soest, 2006 (consulté le )
- (en) Référence Catalogue of Life : Amphimedon queenslandica Hooper & van Soest, 2006 (consulté le )
- (en) Référence NCBI : Amphimedon queenslandica (taxons inclus) (consulté le )
- (en) Référence World Register of Marine Species : espèce Amphimedon queenslandica Hooper & van Soest, 2006 (consulté le )
Liens externes
- Ressources relatives au vivant :
- Portail sur Encyclopedia of life
- Répertoire des facteurs de transcription chez A. queenslandica
- Présentation sur le microbiome d'A. queenslandica
- Présentation sur l'expression de Wnt et TGF-β chez A. queenslandica http://slideplayer.fr/slide/1749998/