Acide subérique
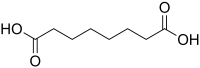
L'acide subérique ou acide octanedioïque est un composé organique de la famille des acides dicarboxyliques, de formule C8H14O4. Il se présente sous la forme d'un solide cristallin blanc inodore, très légèrement soluble dans l'eau, combustible mais peu inflammable[1]. Il est notamment utilisé dans la synthèse de composés pharmaceutiques et dans l'industrie du plastique.
| Acide subérique | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| Nom systématique | acide octanedioïque | |
| No CAS | ||
| No ECHA | 100.007.283 | |
| PubChem | 10457 | |
| SMILES | ||
| InChI | ||
| Apparence | poudre cristalline blanche inodore[1] | |
| Propriétés chimiques | ||
| Formule | C8H14O4 [Isomères] |
|
| Masse molaire[2] | 174,194 4 ± 0,008 6 g/mol C 55,16 %, H 8,1 %, O 36,74 %, |
|
| pKa | 4,526 ; 5,498[3] | |
| Propriétés physiques | ||
| T° fusion | 139 à 142 °C[1] | |
| T° ébullition | 229 à 231 °C (20 hPa)[1] | |
| Solubilité | 1,6 g·L-1 (eau, 20 °C) | |
| T° d'auto-inflammation | 430 °C[1] | |
| Point d’éclair | 210 °C[1] | |
| Précautions | ||
| SGH[1] | ||
 |
||
| Transport[1] | ||
non soumis à réglementation |
||
| Unités du SI et CNTP, sauf indication contraire. | ||
Occurrence

L'acide subérique est naturellement présent dans le liège[4], d'où il tire son nom (en latin suber), sous la forme de la subérine[5], ainsi que dans certaines bufotoxines[6].
Synthèse
L'acide subérique peut être produit synthétiquement par oxydation du liège ou de l'huile de ricin par l'acide nitrique. Il peut être également obtenu par carbonylation de l'hexane-1,6-diol.
Utilisations
L'acide subérique est utilisé dans la production de polyamides et de polyesters[6]. Les esters de l'acide subérique sont utilisés comme plastifiants[7].
Notes et références
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Korksäure » (voir la liste des auteurs).
- Entrée « Octanedioic acid » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 1er avril 2020 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Bretti, C., Crea, F., Foti, C. et Sammartano, S., « Solubility and Activity Coefficients of Acidic and Basic Nonelectrolytes in Aqueous Salt Solutions. 2. Solubility and Activity Coefficients of Suberic, Azelaic, and Sebacic Acids in NaCl(aq), (CH3)4NCl(aq), and (C2H5)4NI(aq) at Different Ionic Strengths and at t = 25 °C », J. Chem. Eng. Data, vol. 51, no 5, , p. 1660–1667 (DOI 10.1021/je060132t)
- Albert Gossauer: Struktur und Reaktivität der Biomoleküle, Verlag Helvetica Chimica Acta, Zürich, 2006, p. 354, (ISBN 978-3-906390-29-1).
- Suberin - Lexikon der Biologie (présentation en ligne)
- Korksäure - Lexikon der Chemie (présentation en ligne)
- (de) « Octandisäure », sur Römpp Online, Georg Thieme Verlag (consulté le )