Acide aconitique
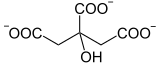
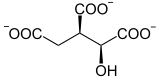
L’acide aconitique, ou acide équisétique, est un acide tricarboxylique de formule HOOC–CH2–C(COOH)=CH–COOH. Il existe deux isomères de cet acide tricarboxylique : l'acide cis-aconitique et l'acide trans-aconitique. La base conjuguée du premier, le cis-aconitate, est un intermédiaire de l'isomérisation du citrate en isocitrate par l'aconitase dans le cycle de Krebs.
| Acide aconitique | |
 Structure de l'acide cis-aconitique (à gauche) et de l'acide trans-aconitique (à droite) |
|
| Identification | |
|---|---|
| No CAS | (isomère cis) (isomère trans) |
| No ECHA | 100.007.162 |
| No CE | 207-877-0 |
| PubChem | 643757 (isomère cis) 444212 (isomère trans) |
| ChEBI | 32805 |
| SMILES | |
| InChI | |
| Apparence | solide incolore cristallisé |
| Propriétés chimiques | |
| Formule | C6H6O6 [Isomères] |
| Masse molaire[1] | 174,108 2 ± 0,007 g/mol C 41,39 %, H 3,47 %, O 55,14 %, |
| Précautions | |
| SGH[2] | |
 Attention |
|
| Unités du SI et CNTP, sauf indication contraire. | |
L'acide aconitique résulte in vitro également de la déshydratation de l'acide citrique, ce qui peut être réalisé par chauffage ou bien à l'aide d'acide sulfurique H2SO4[3] :
- HOOC–CH2–HOC(COOH)–CH2–COOH → H2O + HOOC–CH2–C(COOH)=CH–COOH.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé cis-Aconitic acid ≥ 98%, consultée le 14 juillet 2016.
- (en) William F. Bruce, « Aconitic Acid », Organic Syntheses, vol. 2, , p. 12 (DOI 10.15227/orgsyn.017.0001, lire en ligne)
Voir aussi
Cet article est issu de wikipedia. Text licence: CC BY-SA 4.0, Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.