Tricine (tampon)
La tricine (ainsi nommée d'après le tris et la glycine) est un composé organique faisant partie des tampons de Good[2]. Son pKa d'environ 8,15 à 20 °C présente un certain intérêt comme tampon pour des applications en biochimie.
| Tricine | |
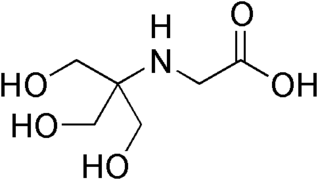
| |
| Identification | |
|---|---|
| Nom UICPA | N-(2-Hydroxy-1,1-bis(hydroxyméthyl)éthyl)glycine |
| No CAS | |
| No ECHA | 100.024.721 |
| PubChem | 79784 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C6H13NO5 [Isomères] |
| Masse molaire[1] | 179,171 1 ± 0,007 4 g/mol C 40,22 %, H 7,31 %, N 7,82 %, O 44,65 %, |
| pKa | 8,15 à 20 °C |
| Unités du SI et CNTP, sauf indication contraire. | |
Applications
La tricine est couramment utilisée comme tampon en électrophorèse. Plus polarisée que la glycine, elle migre plus rapidement. Sa plus grande force ionique augmente le mouvement des ions et diminue celui des protéines, ce qui permet de mieux séparer les protéines de faible poids moléculaires (de 1 à 100 kDa) avec moins d'acrylamide[3]. Le tampon tricine à 25 mmol/L s'est avéré le plus efficace de ceux testés pour l'étude de l'ATP par luciférase[4]. La tricine participe aussi à la recapture de radicaux libres HO•, limitant ainsi les dommages cellulaires dus aux radiations[5].
Références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Tricine » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Norman E. Good, G. Douglas Winget, Wilhelmina Winter et Thomas N. Connolly, « Hydrogen Ion Buffers for Biological Research », Biochemistry, vol. 5, no 2, , p. 467–477 (ISSN 0006-2960, DOI 10.1021/bi00866a011, lire en ligne, consulté le )
- (en) Hermann Schägger et Gebhard von Jagow, « Tricine-sodium dodecyl sulfate-polyacrylamide gel electrophoresis for the separation of proteins in the range from 1 to 100 kDa », Analytical Biochemistry, vol. 166, no 2, , p. 368–379 (ISSN 0003-2697, DOI 10.1016/0003-2697(87)90587-2, lire en ligne, consulté le )
- J. J. Webster, J. C. Chang, E. R. Manley et H. O. Spivey, « Buffer effects on ATP analysis by firefly luciferase », Analytical Biochemistry, vol. 106, no 1, , p. 7–11 (ISSN 0003-2697, PMID 7191217, DOI 10.1016/0003-2697(80)90111-6, lire en ligne, consulté le )
- (en) Mark Hicks et Janusz M. Gebicki, « Rate constants for reaction of hydroxyl radicals with Tris, Tricine and Hepes buffers », FEBS Letters, vol. 199, no 1, , p. 92–94 (ISSN 0014-5793, DOI 10.1016/0014-5793(86)81230-3, lire en ligne, consulté le )