Nitrite d'amyle
Le nitrite d'amyle est un composé chimique de la famille des nitrites d'alkyle, de formule C5H11ONO. Il est volatil et nocif. Il a des propriétés de vasodilatateur[5] et fut initialement utilisé comme médicament, par exemple pour stopper l'érection lorsqu'un patient possède une sonde urinaire, afin de soulager ce dernier de l'irritation causée par l’érection.
| Nitrite d'amyle | |||
| |||
| Identification | |||
|---|---|---|---|
| DCI | nitrite de 3-méthylbutyle | ||
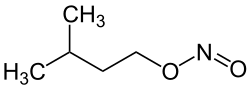
| Nom UICPA | Nitrite d'amyle | ||
| No CAS | |||
| No CE | 203-770-8 | ||
| Code ATC | V03 | ||
| Apparence | liquide jaune, d'odeur caractéristique[1]. | ||
| Propriétés chimiques | |||
| Formule | C5H11NO2 [Isomères] C5H11ONO |
||
| Masse molaire[2] | 117,146 3 ± 0,005 6 g/mol C 51,26 %, H 9,46 %, N 11,96 %, O 27,32 %, |
||
| Propriétés physiques | |||
| T° ébullition | 97 à 99 °C[1] | ||
| Solubilité | dans l'eau : nulle[1] | ||
| Masse volumique | 0,875 g·cm-3[1] | ||
| T° d'auto-inflammation | 209 °C[1] | ||
| Point d’éclair | 3 °C[1] | ||
| Pression de vapeur saturante | à 20 °C : 3,5 kPa[1] | ||
| Précautions | |||
| SGH[3] | |||
  Danger |
|||
| SIMDUT[4] | |||
  B2, D1A, |
|||
| NFPA 704 | |||
| Transport | |||
|
|||
| Caractère psychotrope | |||
| Catégorie | Dépresseur faible | ||
| Mode de consommation |
Inhalation des vapeurs |
||
| Autres dénominations | |||
| Risque de dépendance | Faible | ||
| Composés apparentés | |||
| Autres composés | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
Il est aussi utilisé dans certains pays en cas d'intoxication au cyanure. On l'associe alors au thiosulfate de sodium et au nitrite de sodium.
Son utilisation en inhalation fut par la suite détournée comme drogue récréative dans les milieux festifs et homosexuels, et il fut vendu dans les sex-shops sous le nom de poppers. Il s'est révélé provoquer une déficience passagère de l'immunité, notamment en détruisant des lymphocytes T[6], ce qui l'a fait considérer comme un facteur du SIDA[7], ainsi que d'autres effets indésirables comme des troubles visuels qui l'ont fait interdire à la vente sans prescription médicale. Une étude, commandée en 1978 par Pharmex (fabricant d’une marque de poppers les plus vendues) qui la finança à hauteur de 200 000 dollars, obtint la décision du gouvernement de Californie de libéraliser la vente des nitrites sous forme de désodorisant d’ambiance.
Historique
Le nitrite d'amyle a été synthétisé en 1844 par Antoine Jérôme Balard. Frederick Guthrie décrit l'effet de l'inhalation de petites doses en 1859[8] et Thomas L Brunton l'utilise dans le traitement des affections cardiaques peu après[9], dont l'angine de poitrine[10].
Notes et références
- NITRITE D'AMYLE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Nitrite d'isoamyle » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Moody M, Rubal BJ, Balley SR, Features of the hemodynamic response to amyl nitrite inhalation: Ew aspects of an old tool, Clinical Cardiology, 1993;331:16
- ; Goedert et al. (1982) soulignent que le ratio des lymphocytes dans le sang périphérique est moins élevé chez les utilisateurs que les non-utilisateurs. Hersch et al. démontrent en 1983 les effets immuno-suppresseurs des nitrites sur les leucocytes (globules blancs) du sang périphérique.
- 1994, Harry Haverkos; "Isobutyl nitrite and related compounds", par Nickerson, Parker, Lowry et Swenson, 95 pp.
- Guthrie F, Contributions to the knowledge of the amyl group. 1. Nitryl of amyl and its derivatives, J Chem Soc, 1959;11:245–252
- Fye WB, T. Lauder Brunton and amyl nitrite: a Victorian vasodilator, Circulation, 1986;74:222–229
- Brunton TL, On the use of nitrite of amyl in angina pectoris, Lancet, 1867;2:97
Article connexe
- Poppers
- Slam (sexualité)
