Iodure de zinc
L'iodure de zinc est un corps composé ionique, modélisable par un cation zinc pour deux ions iodures, de formule chimique ZnI2.
| Iodure de zinc | |
| |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.030.347 |
| No CE | 233-396-0 |
| SMILES | |
| InChI | |
| Apparence | cristaux légèrement colorés, granulés blancs hygroscopiques, brunit à l'air ou à la lumière, inodore, goût salé |
| Propriétés chimiques | |
| Formule | ZnI2 |
| Masse molaire[1] | 319,19 ± 0,02 g/mol I 79,52 %, Zn 20,49 %, |
| Propriétés physiques | |
| T° fusion | ≈446 °C[2] |
| T° ébullition | décomposition vers 624 °C-625 °C |
| Solubilité | 4 500 g·L-1 eau à 20 °C, 1g dans 0.2ml eau à 100 °C, 1g dans 2ml glycérol. Librement sol dans alcool, éther. |
| Masse volumique | 4,74 à 25 °C, 4,736 à 20 °C |
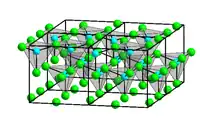
| Cristallographie | |
| Système cristallin | hexagonal |
| Précautions | |
| Directive 67/548/EEC | |
 Xi |
|
| Considérations thérapeutiques | |
| Classe thérapeutique | antiseptique, astringent |
| Unités du SI et CNTP, sauf indication contraire. | |
Solubilité dans l'eau et les autres solvants
Il est très soluble dans l'eau. La solubilité maximale pour 100 g d'eau est de 432 g eau à 18 °C, mais de 511 g d'eau à 100 °C.

Solubilité dans l'eau
Il est soluble également dans les acides et le carbonate d'ammonium, mais aussi l'éthanol, l'éther, ainsi que l'ammoniac.
Usage
Il était utilisé comme un antiseptique puissant au début du XXe siècle.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Perry's Chemical Engineer's Handbook, 6e éd.
Cet article est issu de wikipedia. Text licence: CC BY-SA 4.0, Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.