Coumaroyl-coenzyme A
La coumaroyl-coenzyme A, ou plus précisément la 4-coumaroyl-CoA, est un thioester formé par la réaction entre la fonction acide carboxylique de l'acide paracoumarique (acide 4-hydroxycinnamique) et la fonction thiol de la coenzyme A.
| Coumaroyl-coenzyme A | |
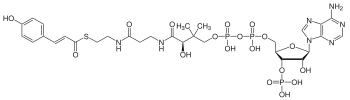 |
|
| Identification | |
|---|---|
| Synonymes |
4-coumaroyl-CoA |
| No CAS | |
| PubChem | 5280329 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C30H42N7O18P3S [Isomères] |
| Masse molaire[1] | 913,677 ± 0,039 g/mol C 39,44 %, H 4,63 %, N 10,73 %, O 31,52 %, P 10,17 %, S 3,51 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
C'est la forme « activée » de l'acide paracoumarique, utilisée en biosynthèse.
Formation
La coumaroyl-CoA est formée par réaction entre l'acide paracoumarique (en fait sa base conjuguée, le 4-coumarate) et la coenzyme A, réaction catalysée par une enzyme, la 4-coumarate-CoA ligase (4CL), et aidée énergétiquement par l'hydrolyse d'une molécule d'ATP en AMP et pyrophosphate inorganique :
- 4-coumarate + CoA + ATP 4-coumaryl-CoA + AMP + PPi
Synthèses
La coumaroyl-CoA est la forme « activée » de l'acide paracoumarique, ce qui le rend susceptible de participer à de nombreuses synthèses biochimiques.
La coumaroyl-CoA est un élément clé dans la synthèse des chalcones, et donc des flavonoïdes, par la voie métabolique des phénylpropanoïdes. Il réagit en général avec trois molécules de malonyl-CoA, réaction catalysée par une enzyme spécifique, une chalcone synthase. On peut citer ainsi la 6'-déoxychalcone synthase dont l'action produit l'isoliquiritigénine, ou encore la naringinine-chalcone synthase produisant la naringinine-chalcone (phlorétine).
La coumaroyl-CoA participe à la formation de stilbènes, toujours par réaction avec trois molécules de malonyl-CoA, avec l'action d'une enzyme de type stilbène synthase. On peut notamment citer le 3,4',5-trihydroxystilbène formé par l'action de la trihydroxystilbène synthase.
La coumaroyl-CoA participe aussi à la formation du N-(4-guanidinobutyl)-4-hydroxycinnamamide par réaction avec l'agmatine catalysée par l'agmatine N4-coumaroyltransférase ou encore à la formation du 4-coumaroylshikimate par réaction le shikimate (base conjuguée de l'acide shikimique), réaction catalysée par la shikimate O-hydroxycinnamoyltransférase.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
