Acide perbromique
L'acide perbromique est un composé chimique de formule HBrO4. Contrairement à l'acide periodique HIO4, il ne peut être obtenu par dismutation thermique de l'acide bromique HBrO3, mais uniquement à partir de solutions de bromates BrO3− à l'aide d'oxydants très énergiques tels que le fluor F2 ou le difluorure de xénon XeF2, ou encore par oxydation anodique :
| Acide perbromique | |
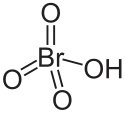  Structure de l'acide perbromique |
|
| Identification | |
|---|---|
| No CAS | |
| PubChem | 192513 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | HBrO4 |
| Masse molaire[1] | 144,91 ± 0,002 g/mol H 0,7 %, Br 55,14 %, O 44,16 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
L'acide perbromique est un acide fort très oxydant. C'est le moins stable des oxoacides d'halogène(VII). Il se décompose rapidement en acide bromique HBrO3 et oxygène O2. Il réagit avec les bases pour former des sels de bromate.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
Cet article est issu de wikipedia. Text licence: CC BY-SA 4.0, Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.