Acétylacétonate de sodium
L’acétylacétonate de sodium est un composé chimique de formule Na(O2C5H7). C'est un sel du cation sodium Na+ et de l'anion acétylacétonate C5H7O2−, base conjuguée du tautomère énolique de l'acétylacétone. Il se présente sous la forme d'un solide blanc soluble dans l'eau dans lequel le cation Na+ est lié aux centres énolate[2]. On l'obtient par déprotonation de l'acétylacétone[3] :
| Acétylacétonate de sodium | |
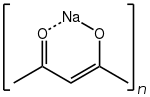
| |
| Structure de l'acétylacétonate de sodium | |
| Identification | |
|---|---|
| Nom UICPA | pentane-2,4-dionate de sodium |
| Nom systématique | 2,4-pentanedionate de sodium |
| Synonymes |
acétylacétonate de sodium |
| No CAS | |
| No ECHA | 100.035.847 |
| No CE | 239-448-9 |
| PubChem | 6008486 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C5H7NaO2 |
| Masse molaire[1] | 122,097 6 ± 0,005 1 g/mol C 49,18 %, H 5,78 %, Na 18,83 %, O 26,21 %, |
| Cristallographie | |
| Système cristallin | monoclinique |
| Classe cristalline ou groupe d’espace | P21/c (no 14) [2] |
| Paramètres de maille | Hydrate Na(O2C5H7)·H2O : a = 1 110,2 pm, b = 605,8 pm, c = 1 028,7 pm, β = 104,50°, Z = 4[2]. |
| Unités du SI et CNTP, sauf indication contraire. | |
La substance anhydre est obtenue par déprotonation de l'acétylacétone avec de l'hydrure de sodium NaH dans un solvant aprotique tel que le tétrahydrofurane[4] (THF) :
Il donne du tétraacétyléthane [C5H6O2H]2 par oxydation, par exemple sous l'action de l'iode I2[3] :
- I2 + 2 Na(O2C5H7) ⟶ [C5H6O2H]2 + 2 NaI.
Il réagit avec les sels métalliques pour donner des acétylacétonates de métal. L'alkylation de l'acétylacétonate peut donner un éther d'énol (alkylation O) ou un dérivé 3-substitué de l'acétylacétone (alkylation C).
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) J. J. Sahbari et M. M. Olmstead, « Structure of sodium acetylacetonate monohydrate, Na[C5H7O2].H2O », Acta Crystallographica Section C, vol. 39, no 8, , p. 1037-1038 (DOI 10.1107/S0108270183007283, lire en ligne).
- (en) Robert G. Charles, « Tetraacetylethane », Organic Syntheses, vol. 39, , p. 61 (DOI 10.15227/orgsyn.039.0061, lire en ligne).
- (en) Marie E. Krafft, Martin J. Procter et Khalil A. Abboud, « Synthesis of molybdenum dicarbonyl complexes bearing tethered homoallylic amines and sulfides », Organometallics, vol. 18, no 7, , p. 1122-1124 (DOI 10.1021/om9807102, lire en ligne).


