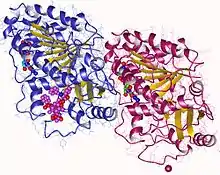
Tubuline
La tubuline est la protéine structurale des microtubules, un constituant majeur du cytosquelette. Elle a une masse moléculaire d'environ 100 kDa.
Composition
Elle est composée de 2 sous-unités non identiques :
- la tubuline α de masse moléculaire d'environ 50 kDa et à un pHI de l'ordre de 5,3 - 5,8 et est liée au GTP ;
- la tubuline β de masse moléculaire d'environ 50 kDa et à un pHI de l'ordre de 5,3 - 5,6 et est liée au GTP, qu'elle a la capacité d'hydrolyser. C'est l'état de cette sous-unité qui définit l'état « GTP » ou « GDP » de la tubuline. Il existe plusieurs isotypes de cette tubulines, dont TUBB, TUBB1, TUBB2A, TUBB2B, TUBB2C, TUBB3, TUBB4, TUBB4Q, TUBB6 et TUBB8.
Ces deux sous-unités, issues de l'expression de deux gènes différents (gène α et gène β), sont donc très semblables et ne diffèrent en fait que par quelques acides aminés (5 à 10 % de la chaîne).
Fonction
Microtubules
La tubuline dirige la dynamique des microtubules. Suivant sa concentration dans la cellule, elle va en diriger la polymérisation ou la dépolymérisation.
- Si la concentration de tubuline-GTP est élevée, des dimères α-β se polymérisent, formant les protofilaments. Ces protofilaments s'associent entre eux sur leur longueur et forment ainsi le microtubule. L'assemblage de protofilament peut également conduire à l'obtention d'un flagelle, comme dans les spermatozoïdes par exemple.
- Si la concentration de tubuline-GTP dans la cellule est trop faible, les protofilaments vont se dépolymériser et se dégrader.
Dans la cellule, les microtubules rayonnent d'une structure cytosolique visible au microscope électronique appelée centrosome. Toutes les cellules eucaryotes animales en possèdent un dans leur cytoplasme ; les cellules végétales, elles, possèdent une autre structure, non visible en microscopie, qui est appelée « centre organisateur des microtubules ».
Les microtubules sont assemblés à partir de dimères d'α- et de β-tubuline. Ces sous-unités sont légèrement acides, avec un point isoélectrique compris entre 5,2 et 5,8[2]. Chacune a un poids moléculaire d'environ 50 kDa[3].
Pour former les microtubules, les dimères d'α- et de β-tubuline se lient au GTP et s'assemblent sur les extrémités (+) des microtubules lorsqu'ils sont à l'état lié au GTP[4]. La sous-unité de β-tubuline est exposée sur l'extrémité plus du microtubule, tandis que la sous-unité d'α-tubuline est exposée sur l'extrémité moins. Après l'incorporation du dimère dans le microtubule, la molécule de GTP liée à la sous-unité β-tubuline finit par s'hydrolyser en GDP par le biais de contacts interdimères le long du protofilament du microtubule[5]. La molécule de GTP liée à la sous-unité α-tubuline n'est pas hydrolysée pendant tout le processus. Le fait que le membre β-tubuline du dimère de tubuline soit lié au GTP ou au GDP influence la stabilité du dimère dans le microtubule. Les dimères liés au GTP ont tendance à s'assembler en microtubules, tandis que les dimères liés au GDP ont tendance à se désagréger ; ce cycle du GTP est donc essentiel pour l'instabilité dynamique du microtubule.
Microtubules bactériens
Des homologues de l'α- et de la β-tubuline ont été identifiés dans le genre de bactéries Prosthecobacter[6]. Ils sont désignés BtubA et BtubB pour les identifier comme des tubulines bactériennes. Toutes deux présentent une homologie avec les α- et β-tubulines[7]. Bien que leur structure soit très similaire à celle des tubulines eucaryotes, elles présentent plusieurs caractéristiques uniques, notamment un repliement sans chaperon et une faible dimérisation[8]. Des études in vitro montrent que les BtubA/B forment des « mini-microtubules » à quatre brins[9], contrairement aux microtubules eucaryotes, qui en contiennent généralement 13.
Pharmacologie
La tubuline possède 3 sites de liaison, qui sont les cibles de médicaments anticancéreux ; le site du Taxol, de la Vinblastine et de la colchicine. La colchicine et la Vinblastine se lient à la tubuline et inhibent sa polymérisation, c'est-à-dire la formation de microtubules, immobilisant les neutrophiles et abaissant l'inflammation. Le Taxol inhibe la dépolymérisation des microtubules.
Références
- (en) J. Löwe, H. Li, K. H. Downing et E. Nogales, « Refined structure of αβ-tubulin at 3.5 Å resolution », Journal of Molecular Biology, vol. 313, no 5, , p. 1045-1057 (PMID 11700061, DOI 10.1006/jmbi.2001.5077, lire en ligne)
- Williams RC, Shah C, Sackett D, « Separation of tubulin isoforms by isoelectric focusing in immobilized pH gradient gels », Analytical Biochemistry, vol. 275, no 2, , p. 265–7 (PMID 10552916, DOI 10.1006/abio.1999.4326)
- « tubulin in Protein sequences », sur EMBL-EBI
- Heald R, Nogales E, « Microtubule dynamics », Journal of Cell Science, vol. 115, no Pt 1, , p. 3–4 (PMID 11801717, DOI 10.1242/jcs.115.1.3
 )
) - Howard J, Hyman AA, « Dynamics and mechanics of the microtubule plus end », Nature, vol. 422, no 6933, , p. 753–8 (PMID 12700769, DOI 10.1038/nature01600, Bibcode 2003Natur.422..753H, S2CID 4427406)
- (en) C. Jenkins, R. Samudrala, I. Anderson, B.P. Hedlund, G. Petroni, N. Michailova, N. Pinel, R. Overbeek, G. Rosati et J.T. Staley, « Genes for the cytoskeletal protein tubulin in the bacterial genus Prosthecobacter », Proceedings of the National Academy of Sciences of the United States of America, vol. 99, no 26, , p. 17049–54 (PMID 12486237, PMCID 139267, DOI 10.1073/pnas.012516899, Bibcode 2002PNAS...9917049J).
- Martin-Galiano AJ, Oliva MA, Sanz L, Bhattacharyya A, Serna M, Yebenes H, Valpuesta JM, Andreu JM, « Bacterial tubulin distinct loop sequences and primitive assembly properties support its origin from a eukaryotic tubulin ancestor », The Journal of Biological Chemistry, vol. 286, no 22, , p. 19789–803 (PMID 21467045, PMCID 3103357, DOI 10.1074/jbc.M111.230094
 )
) - Schlieper D, Oliva MA, Andreu JM, Löwe J, « Structure of bacterial tubulin BtubA/B: evidence for horizontal gene transfer », Proceedings of the National Academy of Sciences of the United States of America, vol. 102, no 26, , p. 9170–5 (PMID 15967998, PMCID 1166614, DOI 10.1073/pnas.0502859102
 , Bibcode 2005PNAS..102.9170S)
, Bibcode 2005PNAS..102.9170S) - Deng X, Fink G, Bharat TA, He S, Kureisaite-Ciziene D, Löwe J, « Prosthecobacter BtubAB show dynamic instability », Proceedings of the National Academy of Sciences of the United States of America, vol. 114, no 29, , E5950–E5958 (PMID 28673988, PMCID 5530688, DOI 10.1073/pnas.1705062114
 )
)
- Microtubule Polymerization Dynamics. Arshad Desai and Thimoty J.Mitchison. Ann. Rev. Cell. Dev. Biol. (1997) 13:83-117.