Sorbitane
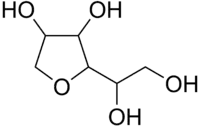
Le sorbitane est un polyol de la famille des oxolanes. C'est le produit de la réaction de déshydratation du sorbitol, d'où son nom (en anglais sorbitan, contraction de sorbitol anhydride, anhydride de sorbitol). Il existe sous la forme de plusieurs stéréoisomères car il y a quatre atomes de carbone asymétrique dans sa structure, mais le principal composé désigné sous ce nom et utilisé est le 1,4-D-sorbitan ou (2R,3S,4R)-2-[(1R)-1,2-dihydroxyéthyl]tétrahydrofuran-3,4-diol. C'est un intermédiaire dans la conversion du sorbitol en isosorbide[4]. Le sorbitane est principalement utilisé dans la production de tensioactifs tels que les polysorbates, d'importants agents émulsifiants, avec une demande annuelle totale de plus de 10 000 tonnes en 2012[5].
| Sorbitane | |
| |
| Identification | |
|---|---|
| Nom UICPA | (3S)-2-(1,2-dihydroxyéthyl)tétrahydrofuran-3,4-diol |
| No CAS | |
| No ECHA | 100.032.415 |
| No CE | 235-671-0 |
| PubChem | 103023 |
| SMILES | |
| InChI | |
| Apparence | solide[1], mais le plus souvent rencontré sous forme d'huile ou de sirop de couleur sombre[2]. |
| Propriétés chimiques | |
| Formule | C6H12O5 [Isomères] |
| Masse molaire[3] | 164,156 5 ± 0,007 1 g/mol C 43,9 %, H 7,37 %, O 48,73 %, |
| Propriétés physiques | |
| T° ébullition | 111 à 112 °C[1] |
| Solubilité | soluble dans l'eau, le méthanol, l'éthanol et l'isopropanol[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
Synthèse
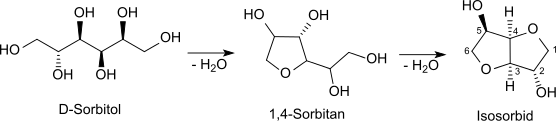
Le sorbitane est produit par la première étape de déshydratation du sorbitol. Une déshydratation supplémentaire donne de l'isosorbide. La réaction de déshydratation produit habituellement du sorbitane comme un mélange d'éthers cycliques, avec des cycles à cinq ou six sommets (1,4-anhydrosorbitol, 1,5-anhydrosorbitol et 1,4,3,6-dianhydrosorbitol)[6]. Le 1,4-anhydrosorbitol est le produit de réaction majoritaire. Le taux de formation de sorbitane est généralement supérieur à celui de l'isosorbide, ce qui permet de le produire de manière sélective, en contrôlant soigneusement les conditions de réaction. Curieusement la réaction de déshydratation peut se produire même en présence d'un excès d'eau[7].
Tensioactifs dérivés
Les esters
Les esters de sorbitane (aussi connu comme spans) sont des tensioactifs non ioniques utilisés comme émulsifiants dans la préparation d'émulsions, de crèmes et d'onguents à usage pharmaceutique et cosmétique. Certains d'entre eux sont également utilisés comme additifs alimentaires. Lorsqu'ils sont utilisés seuls, ils produisent des émulsions stables de type w/O (les plus courants ont une HLB comprise entre 1,8 et 8,6), mais ils sont fréquemment utilisés avec un polysorbate dans des proportions variables pour produire des émulsions w/O ou o/W à volonté avec différentes textures et consistances.
- Esters de sorbitane (Spans)
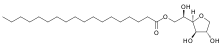 Monostéarate de sorbitane (Span 60, E491)
Monostéarate de sorbitane (Span 60, E491)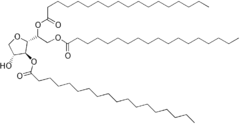 Tristéarate de sorbitane (Span 65, E492)
Tristéarate de sorbitane (Span 65, E492)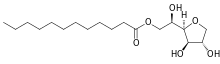 Monolaurate de sorbitane (Span 20, E493)
Monolaurate de sorbitane (Span 20, E493)
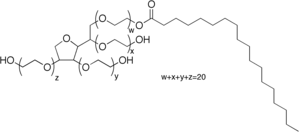
Les polysorbates
Les esters de sorbitane éthoxylés sont connus comme les polysorbates (aussi sous le nom de marque Tween). Ils forment une classe importante d'émulsifiants utilisés dans une large gamme de préparations, y compris des produits pharmaceutiques et alimentaires.
Références
- US-Patent US 2,390,395, Sorbitan and process for making the same, Inventeur : Sol Soltzberg ,Cessionnaire : Atlas Powder Co., publié le 4 décembre 1945.
- US-Patent US 7,649,099, Method of forming a dianhydrosugar alcohol, Inventeur : Johnathan E. Holladay et al., Cessionnaire : Battelle Memorial Institute, publié le 19 janvier 2010.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Marcus Rose et Regina Palkovits, « Isosorbide as a Renewable Platform chemical for Versatile Applications-Quo Vadis? », ChemSusChem, vol. 5, no 1, , p. 167–76 (PMID 22213713, DOI 10.1002/cssc.201100580)
- Hirokazu Kobayashi et Atsushi Fukuoka, « Synthesis and utilisation of sugar compounds derived from lignocellulosic biomass », Green Chemistry, vol. 15, no 7, , p. 1740 (ISSN 1463-9262, DOI 10.1039/c3gc00060e)
- Merck Index, 12e Edition, p. 8872
- Aritomo Yamaguchi, Norihito Hiyoshi, Osamu Sato et Masayuki Shirai, « Sorbitol dehydration in high temperature liquid water », Green Chemistry, vol. 13, no 4, , p. 873 (ISSN 1463-9262, DOI 10.1039/c0gc00426j)