Réaction de formose
La réaction de formose, découverte par le chimiste russe Alexandre Boutlerov en 1861[1] - [2], consiste principalement à polymériser le formaldéhyde pour former des sucres y compris des pentoses (sucres à cinq atomes de carbone). Formose est un mot-valise formé par la contraction des termes formaldéhyde et aldose.
Mécanisme réactionnel
La réaction est catalysée par une base et un métal divalent comme l'hydroxyde de calcium. Les étapes intermédiaires font intervenir des aldolisations, des rétroaldolisations et des isomérisations aldose-cétose. Les molécules intermédiaires formées sont le glycolaldéhyde, le glycéraldéhyde, le dihydroxyacétone et des tétroses. En 1959, le chimiste américain Ronald Breslow a proposé le mécanisme réactionnel suivant[3] :
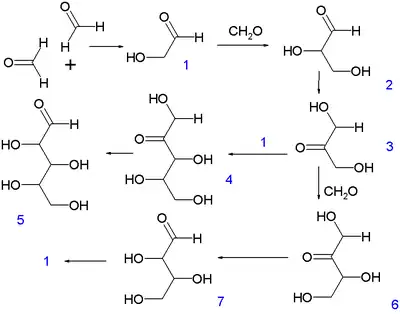
La réaction débute par la condensation de deux molécules de formaldéhyde pour former le glycolaldéhyde (1) qui réagit ensuite par aldolisation avec le formaldéhyde pour former le glycéraldéhyde (2). Une isomérisation aldose-cétose donne le dihydroxyacétone (3) qui peut réagir avec le glycéraldéhyde pour former le ribulose (4) et par isomérisation le ribose (5). Le dihydroxyacétone peut aussi réagir avec le formaldéhyde pour former un cétotétrose (érythrulose) (6) puis par isomérisation un aldotétrose (érythrose et thréose) (7). L'aldotétrose peut ensuite redonner deux molécules de glycéraldéhyde par une réaction de rétroaldolisation.
Importance
La réaction de formose a suscité de nombreux travaux dans le cadre de la recherche sur l'abiogenèse[4] car elle permet d'obtenir à partir d'une molécule simple, le formaldéhyde, des sucres complexes comme le ribose et mener ensuite à la synthèse de l'ARN. Dans une expérience simulant les conditions de la Terre primitive, des pentoses ont été obtenus à partir d'un mélange de formaldéhyde, de glycéraldéhyde et de borates comme la colémanite Ca2B6O115H2O ou la kernite Na2B4O7[5]. L'intérêt pour la réaction de formose s'est encore accru lorsque les recherches en astrochimie ont confirmé la présence de formaldéhyde et de glycolaldéhyde dans le milieu interstellaire[6].
Cependant, on peut penser que dans les conditions initiales sur terre il y a quatre milliards d’années, il y avait des océans, et il est vraisemblable que la vie soit apparue dans un milieu aqueux, du moins cette hypothèse parait-elle plausible[7].
Ce milieu essentiellement constitué d’eau pose toutefois un sérieux problème de compatibilité avec la réaction de formose mise en avant par de nombreux auteurs pour l’élaboration des sucres, les premiers précurseurs du vivant à partir d’une molécule très simple, le formaldéhyde qui pourrait ainsi avoir joué un rôle important à l’origine de la vie.
En effet, à partir du formaldéhyde, en présence d’une base comme l’hydroxyde de calcium, une réaction d’aldolisation (la réaction de formose) extrêmement lente peut se produire et conduire à des sucres, mais cette réaction reste en compétition avec la réaction de Cannizzaro, très rapide, qui conduit irréversiblement à une molécule de méthanol et une molécule d’acide formique[8]. Dans ce contexte, la réaction de formose est aussi mise en question par le fait que dans l’eau, le formaldéhyde n’existe pas en tant que tel (uniquement à l’état de trace < 0,01 %). Il s’hydrate spontanément en gem-diol et se polymérise[9] et aussi d'après H. J. Cleaves II. Ainsi, la réaction de formose ne peut pas se produire dans n’importe quelles conditions qui sont déterminantes mais difficiles à réaliser dans un milieu aqueux. Pour remédier à ce problème de l’eau peu compatible avec la réaction de formose et, de plus, incompatible avec la synthèse des nucléosides à partir d’un sucre (ribose) et d’une base (adénine, guanine, uracile, cytosine) qui supposerait l’élimination d’une molécule d’eau dans un milieu aqueux, ce qui est chimiquement impossible, certains auteurs ont imaginé que le « solvant » initial aurait été, le formaldéhyde dans un milieu sec (désert)[10]. Dans le formaldéhyde, en effet, la synthèse des nucléosides à partir de bases formylées et de sucre est possible d’après S. A. Benner. Mais la présence de formaldéhyde dans une « soupe prébiotique » reste problématique, car la formation de formaldéhyde en grande quantité n’est observée nulle part sur terre, et la synthèse de formaldéhyde théoriquement possible par hydrolyse de l'acide cyanhydrique, la réaction de radicaux formyles, la réaction photochimique du gaz carbonique sur l'eau, ou l'oxydation partielle du méthanol n’est pas évidente, sans un catalyseur de la « chimie moderne » et/ou sans des conditions extrêmes (de température, par exemple)[11]. Il est aussi produit dans l'atmosphère actuelle sous l'action des rayons solaires et du dioxygène sur le méthane atmosphérique, mais en quantités limitées (quelques ppm). Par ailleurs, l’apport très hypothétique de formaldéhyde d’origine extraterrestre envisagé par certains auteurs[12], sur une terre primitive essentiellement couverte d’eau, ne résoudrait pas le problème pour les raisons évoquées ci-dessus. Toutefois, malgré ces limitations, un certain nombre d’auteurs estiment possible la production de formaldéhyde dans un milieu prébiotique et considèrent même que les conditions favorables auraient pu être réunies pour que la réaction de formose se produise. Quoi qu’il en soit, cette réaction ne peut pas expliquer, à elle seule, une biogenèse primitive de l'ARN, hypothèse souvent avancée, car à partir de sucres résultant de la réaction de formose, beaucoup d’étapes supplémentaires sont nécessaires pour parvenir à un ARN codant (synthèse des nucléotides, polymérisation des nucléotides dans un certain ordre, mémorisation, capacité d’autoréplication, etc.) d'après H. J. Cleaves II. Ainsi, l’enchaînement et la mémorisation de tous les évènements initiaux qui ont permis l’apparition des premières entités capables de se reproduire reste difficile à expliquer, et comme le suggère S. Mann, l’origine de la vie demeure, à ce jour, très mystérieuse et constitue un défi majeur pour la science moderne qui devrait être capable de réaliser une transition de la matière inerte vers des premières formes de vie ex novo dans un laboratoire, ce qui n’est pas du tout le cas actuellement[13] - [14].
Références
- A. M. Butlerov, « Einiges über die chemische Structur der Körper », Zeitschrift für Chemie, vol. 4, , p. 549–560.
- Leslie E. Orgel, « Self-organizing biochemical cycles », PNAS, vol. 97, no 23, , p. 12503-12507 (DOI 10.1073/pnas.220406697).
- R. Breslow, « On the Mechanism of the Formose Reaction », Tetrahedron Letters, vol. 21, , p. 22–26.
- Albert Eschenmoser, « The search for the chemistry of life's origin », Tetrahedron, vol. 63, no 52, , p. 12821-12844 (DOI 10.1016/j.tet.2007.10.012).
- A. Ricardo et al., « Borate Minerals Stabilize Ribose », Science, vol. 303, no 5655, , p. 196 (DOI 10.1126/science.1092464).
- D. T. Halfen et al., « A Systematic Study of Glycolaldehyde in Sagittarius B2(N) at 2 and 3 mm: Criteria for Detecting Large Interstellar Molecules », The Astrophysical Journal, vol. 639, , p. 237-245 (DOI 10.1086/499225).
- CNRS, « Les origines de la vie », 2018.
- H.-J. Kim, A. Ricardo, H. I. Illangkoon, M. J. Kim, M. A. Carrigan, F. Frye et S. A. Benner, Synthesis of Carbohydrates in Mineral-Guided Prebiotic Cycles, J. Am. Chem. Soc., 2011, 133, 9457-9468.
- J. March, Advanced Organic Chemistry, 4e éd., Wiley Interscience, 1992, p. 883, 972.
- S. A. Benner, H.-J. Kim et M. A. Carrigan, Asphalt, Water and the Prebiotic Synthesis of Ribose, Ribonucleosides and RNA, Accounts of Chemical Research, 2012, vol. 46, 2025-2034.
- H. J. Cleaves II, The prebiotic geochemistry of formaldehyde, Precambrian Research, 164 (2008) 111-118.
- A. Ricardo, M. A. Carrigan, A. N. Olcott et S. A. Benner, Borate Minerals Stabilize Ribose, Science, 2004, 303, p. 196.
- S. Mann, Systems of Creation: The Emergence of Life from Nonliving Matter, Accounts of Chemical Research, 2012, 45(12), 2131-2141.
- S. Mann, The Origins of Life: Old Problems, New Chemistries, Angewandte Chemie International Edition, 2013, 52, p. 155-162.