Hexacarbonyle de molybdène
L'hexacarbonyle de molybdène est un composé chimique de formule Mo(CO)6. Il se présente comme un solide blanc cristallisé ininflammable, pratiquement insoluble dans l'eau et peu soluble dans les solvants apolaires. Stable au contact de l'air, il se décompose au-dessus de 150 °C en libérant du monoxyde de carbone CO et du dioxyde de carbone CO2.
| Hexacarbonyle de molybdène | |
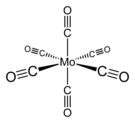  Structure de l'hexacarbonyle de molybdène  Poudre de cristaux de Mo(CO)6 |
|
| Identification | |
|---|---|
| Synonymes |
hexacarbonylmolybdène |
| No CAS | |
| No ECHA | 100.034.271 |
| No CE | 237-713-3 |
| PubChem | 98885 |
| ChEBI | 30508 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche cristallisée |
| Propriétés chimiques | |
| Formule | C6MoO6 |
| Masse molaire[1] | 264,02 ± 0,03 g/mol C 27,3 %, Mo 36,35 %, O 36,36 %, |
| Propriétés physiques | |
| T° fusion | décomposition au-dessus de 150 °C[2] en CO et CO2 |
| Masse volumique | 1,96 g·cm-3[2] |
| Précautions | |
| SGH[2] | |
 Danger |
|
| Transport[2] | |
| Unités du SI et CNTP, sauf indication contraire. | |
Il s'agit d'un carbonyle de métal constitué d'un atome de molybdène central coordonné à six ligands carbonyle CO, respectant la règle des 18 électrons, dans lequel la liaison Mo–C à une longueur de 206 pm.
Il peut être obtenu par réduction de chlorure de molybdène(VI) MoCl6 à l'aide de triéthylaluminium Al(C2H5)3 dans une atmosphère de monoxyde de carbone CO sous pression :
Cette réaction est toutefois rarement mise en œuvre au laboratoire car elle requiert des équipements coûteux alors que l'hexacarbonyle de molybdène peut être acheté à des prix raisonnables.
Applications
L'hexacarbonyle de molybdène est largement employé en chimie des composés organométalliques car un ou plusieurs de ses ligands carbonyle peuvent être déplacés par d'autres ligands, en l'occurrence organiques. Il réagit par exemple avec la 2,2'-bipyridine pour donner du Mo(CO)4(bipy). La photolyse aux ultraviolets d'une solution de Mo(CO)6 dans le tétrahydrofurane (THF) conduit au Mo(CO)5(THF). De nombreux carbonyles de métal sont ainsi photoactivables.
Mo(CO)6 est également utilisé dans les techniques de dépôt assisté par faisceau d'électrons car il est facilement vaporisé par les électrons et sa décomposition libère du molybdène[3]. On l'emploie également dans les réactions de métathèse des alcynes et dans la réaction de Pauson-Khand.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Hexacarbonylmolybdenum » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 11 mai 2013 (JavaScript nécessaire)
- (en) S. J. Randolph, J. D. Fowlkes et P. D. Rack, « Focused, Nanoscale Electron-Beam-Induced Deposition and Etching », Critical Reviews in Solid State and Materials Sciences, vol. 31, no 3, , p. 55-89 (lire en ligne) DOI 10.1080/10408430600930438
