Herpèsvirus humain type 8
Human gammaherpesvirus 8
| Royaume | Duplodnaviria |
|---|---|
| Règne | Heunggongvirae |
| Embranchement | Peploviricota |
| Classe | Herviviricetes |
| Ordre | Herpesvirales |
| Famille | Herpesviridae |
| Sous-famille | Gammaherpesvirinae |
| Genre | Rhadinovirus |
- Human herpesvirus 8[1]
L’Herpèsvirus humain type 8, Human gammaherpesvirus 8 (synonyme : Human herpesvirus 8, HHV-8) est, comme toutes les espèces de virus de la famille des Herpesviridae, un virus à ADN double-brin enveloppé. Il fait partie de la sous-famille des Gammaherpesvirinae et du genre Rhadinovirus. Il est découvert en 1994 par Patrick S. Moore et Yuan Chang, virologistes américains qui établissent notamment que ce virus, également appelé virus de l'herpès associé au sarcome de Kaposi, était responsable de la pathologie éponyme.
Transmission
Le réservoir est exclusivement humain. Le mode de transmission du HHV8 reste imparfaitement connu mais les voies prépondérantes sont la voie salivaire et la voie sexuelle. Ce virus, tout comme le VIH, touche tout particulièrement les homosexuels, la transmission chez les hétérosexuels étant beaucoup moins documentée. Les rapports orogénitaux sont particulièrement contaminants. La transmission horizontale a également été démontrée. Enfin, il existe un risque lors de la transplantation d’organes. La séroprévalence à ce virus augmente avec l’âge, ce qui laisse supposer qu’un autre mode de transmission inconnu existe.
Physiopathologie
La primoinfection est la première étape de l'infection. Le virus, majoritairement transmis par la salive, se réplique initialement dans les cellules épithéliales de l’oropharynx. Il touche ensuite les lymphocytes B, qui représentent le principal réservoir viral. Le virus entre en latence dans ces lymphocytes. L’expression du génome viral est alors minimale. Le système immunitaire a durant ce stade beaucoup de difficultés pour reconnaître les cellules infectées.
La circulation des lymphocytes B infectés dans les tissus lymphoïdes permet l’infection d’autres lymphocytes B lorsque le cycle se déclenche. Les cellules B infectées par le virus latent peuvent disséminer dans tout le corps par le sang. Le HHV-8 peut également infecter les cellules endothéliales, occasionnant ainsi l’apparition de tumeurs malignes. La transmission est favorisée par une infection des lymphocytes B dans l’oropharynx, ce qui libère le virus dans la salive.
Son génome d'environ 145 kpb code au moins 87 protéines dont, entre autres, un homologue de l'interleukine 6, un analoque à Bcl-2 ou vFLIP, des chimiokines et un récepteur de chimiokines, mais également pour 12 microARN, maturés à partir de certains des transcrits alternatifs de la kaposine.
Ces derniers joueraient un rôle très important lors de la phase de latence du virus, étant les seuls exprimés lors de cette phase parmi seulement 4 autres protéines. Cependant leurs cibles cellulaires sont encore mal connues et restent à être identifiées pour déterminer leur rôle exact dans le cycle viral et l'oncogenèse induite par l'infection.
Après infection, le virus entre dans les lymphocytes via les macropinosomes où il reste à l'état latent, exprimant le latency-associated nuclear antigen (LANA (en)) viral.
Clinique
L’infection au HHV-8 est, tout comme d’autres virus herpétiques humains, habituellement asymptomatique lorsque le système immunitaire est compétent. Dans le cas contraire, diverses complications peuvent survenir. Trois syndromes sont maintenant associés au virus, dont un plus courant : le sarcome de Kaposi.
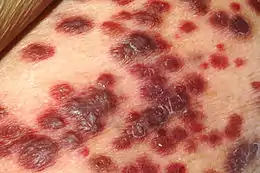
Le sarcome de Kaposi
Le sarcome de Kaposi est une maladie connue au XIXe siècle pour être un cancer peu répandu chez les hommes âgés du bassin méditerranéen. Se présentant sous forme de tumeurs cutanées, la maladie peut parfois atteindre les ganglions et les viscères. Si l’on a établi que le virus jouait un rôle essentiel dans la pathogenèse de cette maladie, les mécanismes exacts de cette maladie restent mal compris : origine des cellules tumorales, réelle nature cancéreuse des lésions…
Lymphome primitif des séreuses
Le lymphome primitif des séreuses est un sous-type de lymphome diffus à grandes cellules B. Très rare, il est systématiquement associé au HHV-8 mais aussi au HHV-4. Il se caractérise par des épanchements de liquide pleural, péritonéal et péricardique dans lesquels on peut retrouver des cellules cancéreuses. Les symptômes sont dus à cet épanchement : dyspnée pour une localisation cardiaque ou pulmonaire et distension abdominale pour une localisation péritonéale.
Le pronostic est défavorable, surtout lorsque la maladie est associée au VIH (ce qui est quasiment toujours le cas). On peut traiter par chimiothérapie couplée avec un traitement antirétroviral pour les patients séropositifs. L'état du système immunitaire influence grandement l’apparition, l’évolution voire la rémission de la maladie.
Maladie de Castleman multicentrique
La maladie de Castleman multicentrique est une prolifération lymphoplasmocytaire polyclonale qui induit un syndrome inflammatoire.
Elle est rare mais potentiellement grave. L’IL-6 joue un rôle majeur dans cette maladie en étant responsable de la stimulation de la plasmocytose ganglionnaire. Le virus HHV-8 joue un rôle prépondérant par le biais de la vIL-6, homologue viral de cette molécule.
Cette maladie est fortement liée au VIH et souvent associée à la maladie de Kaposi. Le pronostic est défavorable et le décès survient souvent par survenue d’un lymphome de haut grade et d’une défaillance multiviscérale.
Diagnostic
Le diagnostic repose majoritairement sur la recherche des anticorps spécifiques par immunofluorescence indirecte. La culture du virus est difficile. La réponse humorale au virus n’est pas encore totalement comprise ; ce dernier exprime différentes protéines qui diffèrent selon le stade latent ou lytique et les tests doivent donc détecter les anticorps correspondant à ces deux phases. Des tests ELISA sont à l’étude. La biologie moléculaire permet la recherche du génome viral par PCR qualitative sur les lymphocytes. La PCR quantitative permet quant à elle d’estimer la charge virale.
Traitement et prophylaxie
Le virus est sensible aux anti-herpétiques in vitro mais il n'existe à ce jour ni traitement spécifique, ni vaccin. Lors d’une co-infection avec le VIH, la prise d’antirétroviraux permet de faire remonter le taux de LT4 et donc d’endiguer l’infection par le HHV-8. Dans le cas d’une contamination par greffe, une diminution des immunosuppresseurs doit être envisagée pour que le système immunitaire puisse lutter contre le virus. En définitive, le pronostic est généralement bon du moment que l’hôte du HHV-8 est immunocompétent.
La prophylaxie passe par des méthodes simples. Le respect des règles d’hygiène basiques permet de limiter la transmission interhumaine, le virus étant peu résistant dans le milieu extérieur. L’utilisation du préservatif et surtout de la digue dentaire est indispensable, les rapports oro-génitaux et oro-anaux étant particulièrement contaminants. Le dépistage pour détecter les porteurs asymptomatiques a son importance. Enfin, la prévention de la maladie et surtout des complications passe également par le dépistage du VIH et, le cas échéant, par la prise d’un traitement antirétroviral pour que le système immunitaire reste compétent et puisse lutter contre le HHV-8.
Notes et références
Référence biologique
- (en) Référence ICTV : Human gammaherpesvirus 8 (consulté le )
Liens externes
- Ressources relatives à la santé :
- (en) Medical Subject Headings
- (cs + sk) WikiSkripta
- Ressource relative au vivant :
- Human Herpesvirus-8: Related Resources HIV InSite (en anglais)