Guanosine monophosphate cyclique
La guanosine monophosphate cyclique (ou GMP cyclique ou GMPc) est un des nucléotides cycliques dérivés de la guanosine triphosphate (GTP).
| Guanosine monophosphate cyclique | |
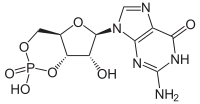
| |
| Identification | |
|---|---|
| Nom UICPA | 2-amino-9-[(1S,6R,8R,9R)-3,9-dihydroxy-3-oxo-2,4,7-trioxa-3λ5-phosphabicyclo[4.3.0]nonan-8-yl]-3H-purin-6-one |
| No CAS | |
| No ECHA | 100.028.765 |
| PubChem | 24316 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C10H12N5O7P [Isomères] |
| Masse molaire[1] | 345,205 3 ± 0,011 9 g/mol C 34,79 %, H 3,5 %, N 20,29 %, O 32,44 %, P 8,97 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
La GMPc agit comme second messager de façon similaire à l'AMP cyclique.
Métabolisme
La synthèse de la GMPc est catalysée par la guanylate cyclase, qui convertit la GTP en GMPc + PPi.
La GMPc est dégradée par certaines phosphodiestérases.
Action
La GMPc agit sur trois types de protéines : la protéine kinase G, certaines phosphodiestérases et certains canaux ioniques dits GMPc-dépendants.
La GMPc influe directement sur le mécanisme érectile chez l'homme et chez la femme. Plus prononcée chez l'homme son action entraîne le relâchement des muscles lisses du pénis, ce qui a pour effet de faciliter le passage du sang en provenance des veines péniennes et d'entraîner le gonflement de la verge. Plus la présence de GMPc est marquée plus l'érection sera durable et forte, et ce jusqu'à la dégradation de la GMPc. Chez la femme un phénomène similaire mais moins fort se produit au niveau du clitoris.
La GMPc est présente chez l'homme dans le sang, dans le liquide pré-séminal et dans le sperme. En cas de taux élevé, une transmission à la femme lors du rapport sexuel est probable, amplifiant le phénomène érectile et la sensibilité du clitoris.
La dégradation de la GMPc intervient normalement après l'orgasme chez l'homme et potentiellement après plusieurs orgasmes chez la femme, par l'action de l'enzyme PDE5.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.