Filament d'actine
Un filament d'actine, ou microfilament, est un homopolymère d'actine, protéine de 42 kDa (Unité de masse atomique). C'est un constituant essentiel du cytosquelette des cellules eucaryotes, ainsi que des fibres musculaires. L'actine représente ainsi environ 10 % du total des protéines d'une cellule animale typique, la moitié étant assemblée en filaments d'actine alors que l'autre moitié est libre dans le cytosol sous forme de monomères d'actine. L'actine sous forme de filaments est parfois appelée actine F (Fibrillaire), tandis que la forme monomérique est appelée actine G (Globulaire).
Structure d'un filament

Un filament d'actine est issu de la polymérisation de plusieurs unités d'actine globulaire avec une rotation de 167° et interagissant via leur grosse sous unité(les petites sous-unités pointant vers l'extérieur du filament donnent l'impression de deux filaments entourés l'un autour de l'autre). Un filament a un diamètre d'environ 7 nm, et une longueur de persistance d'environ 17 μm, soit l'ordre de grandeur du diamètre des cellules.
Chaque filament est polarisé car toutes les molécules d'actine globulaire « pointent » dans la même direction, vers une extrémité appelée (-), l'autre extrémité étant nommée (+). À cette polarité structurelle s'ajoute une polarité de polymérisation. (Voir plus bas).
Dynamique de polymérisation

L'actine G globulaire se polymérise en actine F (filament d'actine).
La polymérisation s'amorce par une phase de nucléation, où sont formés majoritairement des trimères. Les monomères s'assemblent ensuite suivant une double hélice, qui n'a donc pas de centre de symétrie. À l'une des extrémités, notée (+) ou extrémité barbue ou encore en brosse, les constantes cinétiques sont en ordre de grandeur 10 fois supérieures à celles de l'autre extrémité, notée (-) ou extrémité pointue. En outre, les monomères associés à l'ATP (ATP-actine), présents en majorité dans les cellules vivantes, ont plus tendance à polymériser que ceux associés à l'ADP (ADP-actine).
L'actine associée à un filament a tendance à hydrolyser son ATP. Cette propriété est, avec la polarité du filament, à l'origine du phénomène dit de « tapis roulant » (anglais : treadmilling). En effet, l'extrémité (+) va avoir tendance à capter en très grande majorité de l'ATP-actine, favorisant par conséquent la polymérisation à cette extrémité. En revanche, l'extrémité (-) étant moins active, l'actine du filament qui en est proche a passé plus de temps sous forme filamentaire, et est majoritairement sous forme d'ADP-actine. Par conséquent, à l'extrémité (-) l'équilibre est déplacé vers la dépolymérisation.
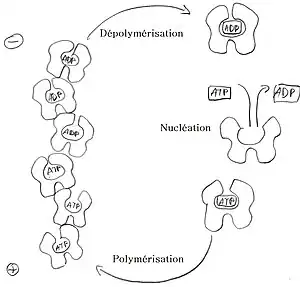
Ces deux déplacements d'équilibre concomitants font que la chaîne croît en permanence du côté (+) et décroît du côté (-). Si on maintient un monomère central fixe, l'ensemble de la chaîne semble donc se déplacer. L'apport d'énergie nécessaire pour maintenir cet état hors équilibre se fait dans le milieu liquide environnant, où l'ADP-actine est régénérée en ATP-actine. Le terme « tapis roulant » suggère que les monomères quittant l'extrémité (-) reviennent se fixer à l'extrémité (+) après un passage en solution. Cependant, aucune masse n'est transportée macroscopiquement. Ce processus permet la réalisation d'un moteur moléculaire qui permet à certaines cellules de se déplacer au moyen d'un lamellipode. Il est aussi à l'origine du mouvement de la bactérie Listeria. Cependant, plusieurs autres protéines sont nécessaires et l'actine seule ne peut pas convertir l'énergie chimique d'hydrolyse de l'ATP en travail.
Protéines associées
Les protéines associées à l'actine (en anglais, Actin associated proteins, ou AAP) sont la clef du contrôle par la cellule de son stock d'actine. Elles permettent de réguler la polymérisation et d'organiser spatialement les filaments. Elles sont à leur tour contrôlées par des protéines régulatrices qui s'insèrent dans le réseau complexe interagissant avec toute la cellule.
Protéines de réticulation
- Fimbrine : maintient les filaments serrés d'actine fasciculée.
- alpha actinine : protéine dimérique liant 2 microfilaments entre eux, les maintenant parallèles entre eux (point focal d'ancrage...). Elle se lie au pôle + pour permettre l'interaction actine-myosine notamment dans le mouvement amiboïde.
- Filamine : bloque l'actine réticulée pour l'empêcher de passer en actine fasciculée.
- Villine : maintient les filaments serrés d'actine fasciculée, spécifique des microvillosités.
- Spectrine : permet l'accrochage du microfilament d'actine à la membrane plasmique
Protéines de stabilisation
- Complexe Tropomyosine
- Ensemble de protéines de coiffes
Protéines de nucléation
Ce sont ces protéines qui permettent d'initier la polymérisation. Il en existe plusieurs types, ayant des modes d'action différents.
- L'Arp2/3, une protéine structuralement proche de l'actine, sert de point de départ à la polymérisation : des monomères d'actine G viennent se lier à elle, entraînant la formation d'un filament. Lorsqu'il est mis en place, l'extrémité moins (-) du microfilament adhère au complexe Arp2/3. La polymérisation évolue donc avec l'extrémité (+) qui induit aussi la croissance du microfilament. Le complexe Arp2/3 est localisé au niveau des jonctions entre filaments d'actine, il est activé par la GTPase Cdc42.
- La formine possède deux domaines riches en proline FH1 et FH2. Des profilines liées chacune à une actine G viennent se lier sur le premier domaine FH1. Ces actines sont alors transférées sur le second domaine FH2, où elles se lient les unes à la suite des autres pour former le filament. La formine est activée par la GTPase Rho.
Protéines de régulation
Ces protéines servent à réguler la quantité d'actine G présente dans le cytoplasme.
- La thymosine se fixe à l'extrémité pointue de l'actine G et empêche l'échange de l'ADP liée à celle-ci par une molécule d'ATP.
- La profiline se fixe à l'actine G et favorise l'échange de l'ADP par de l'ATP, et laisse le côté - de l'actine libre ; il peut ainsi s'insérer dans le polymère à l'extrémité barbue.
Protéines de coiffage
Elles se lient à l'extrémité barbée d'un filament d'actine pour empêcher la polymérisation (ajout d'actine G), et donc pour arrêter la croissance du filament. Elles peuvent également se lier à l'extrémité pointue pour arrêter la dépolymérisation ou permettre la formation d'un nucléus (initiation de la polymérisation).
- Tropomoduline se fixe sur l'extrémité moins du filament d'actine et empêche la polymérisation et la dépolimérisation
- CAP (capping protein) se fixe sur l'extrémité plus du filament, et empêche la polymérisation et la dépolymérisation
Protéines de fragmentation
Ces protéines permettent de cliver les filaments d'actine :
- la gelsoline, comme son nom l'indique, permet de passer de l'actine en gel (dans un réseau de maille) à l'actine en solution (actine G) ;
- la cofiline impose une torsion supplémentaire à l'actine, entraînant sa dépolymérisation(-)
.
Protéines motrices
- Myosine de type 1 : maintient l'actine large fasciculée avec l'aide de l'alpha-actinine.
- Myosine de type 2 : contraction musculaire.
- Myosine de type 5 : protéine moteur capable de se déplacer vers l'extrémité +.
Superstructures
Les filaments d'actine s'organisent de façons très diverses suivant leurs fonctions biologiques. Voici quelques exemples de structures observées et leurs principales propriétés : faisceaux, câbles de tension, réseaux, comètes.
Rôles
- Maintien des édifices structuraux par exemple des villosités.
- Mouvements intracellulaires : contraction des cellules musculaires striées: ces cellules musculaires sont organisées en myofibrilles (= disposition particulière des filaments d'actines et de myosines et d'autres protéines). L'unité fonctionnelle de la myofibrille est le sarcomère qui va se raccourcir lors de la contraction (isotonique ou isométrique). /contraction des cellules musculaires lisses: pas d'organisation sarcomérique, arrangement particulier des filaments qui parcourent la cellule transversalement, longitudinalement et en diagonale, pour s'insérer sur les corps denses.
- Les mouvements cellulaires : déplacement de l'amibe, des leucocytes (pseudopodes).
- La cytodiérèse (en fin de division cellulaire).
- La formation des jonctions cellulaires (y compris des neurones, via le « cône de croissance »).
- Le mouvement des organites : chez les végétaux supérieur le déplacement des chloroplastes dans la cellule en fonction des conditions lumineuses fait intervenir les filaments d'actine.
Effets des toxines
Certaines toxines naturelles ont des effets sur les microfilaments d'actine.
- Phalloïdine : se lie aux filaments d'actine et s'oppose à leur dépolymérisation. Toxine fongique présente notamment dans l'ammanite phalloïde. Origine = Amanite Phalloïde
- Cytochalasine B : se lie aux extrémités (+) et empêche la polymérisation. Toxine fongique. L'addition de cytochalasine à faible concentration gèle instantanément des mouvements comme la reptation d'un fibroblaste, montrant l'implication de l'actine dans de tels mouvements. Origine = Moisissure (Helminthosporium Dermatioideum)
- Latrunculine A : se lie au monomère d'actine-G et inhibe la polymérisation en filaments. Actif à très faible concentration (nM) dans la cellule. Origine = Eponge de feu ramifiée Latrunculia Magnifica)
- Jasplakinolide : induit une polymérisation amorphe avec une nucléation tous les 3 actine-G : le filament s'en trouve alors désorganisé.
Notes et références
Lien externe
- (en) The inner life of the cell, animation réalisée par Biovision d'Harvard, de l'intérieur de la cellule. On peut y voir l'actine globulaire en rose se polymériser et se dépolymériser.