Dibromure de disoufre
Le dibromure de disoufre est un composé chimique de formule S2Br2. Il s'agit d'un liquide rouge foncé huileux qui ne mouille pas le verre et s'hydrolyse au contact de l'eau en formant du dioxyde de soufre SO2, du soufre et du bromure d'hydrogène HBr, d'où son aspect fumant à l'air libre en raison de l'humidité de l'air. Il cristallise dans le système orthorhombique[3]. C'est le plus stable des bromures de soufre, mais sa stabilité thermique reste faible, et il se décompose en soufre et en dibrome Br2 lorsqu'il est chauffé, de sorte qu'il est distillé sous vide poussé afin d'éviter sa décomposition[2].
| Dibromure de disoufre | |
| |
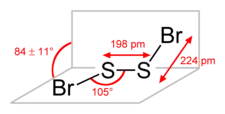
| Structure du dibromure de disoufre. | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.032.821 |
| No CE | 236-119-1 |
| PubChem | 123296 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | Br2S2 |
| Masse molaire[1] | 223,938 ± 0,012 g/mol Br 71,36 %, S 28,64 %, |
| Propriétés physiques | |
| T° fusion | −46 °C[2] |
| Masse volumique | 2,629 g cm−3[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
On peut obtenir le dibromure de disoufre en faisant réagir du soufre avec du brome ou en faisant réagir du dichlorure de disoufre S2Cl2 avec du bromure d'hydrogène HBr[2] :
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (de) Georg Brauer, Handbuch der Präparativen Anorganischen Chemie, 3e réédition, vol. 1, p. 386, Enke, Stuttgart, 1975 (ISBN 3-432-02328-6).
- (de) Jean d'Ans, Ellen Lax et Roger Blachnik, Taschenbuch für Chemiker und Physiker, p. 702, Springer DE, 1998 (ISBN 3-642-58842-5).