Bioisostère
En chimie pharmaceutique, un bioisostère est un groupe fonctionnel ou un composé chimique possédant des propriétés physiques, chimiques ou biochimiques semblables à celles d'un résidu ou d'une biomolécule, ce qui lui confère une action biologique ou physiologique comparables. On utilise les bioisostères en conception de médicament[1] afin d'accroître l'effet biologique ou physiologique recherché ou de réduire la toxicité du composé parent sans altérer significativement sa structure chimique.
Par exemple, la substitution d'un atome d'hydrogène par un atome de fluor sur un site d'oxydation métabolique d'une molécule peut empêcher cette oxydation de se produire : l'atome de fluor ayant un volume du même ordre que celui d'un atome d'hydrogène, il n'altère pas significativement la géométrie de l'ensemble de la molécule, dont l'activité biologique demeure conservée, mais avec une demi-vie plus longue puisque la molécule ne peut plus être dégradée facilement ; un effet semblable peut être obtenu avec divers autres groupes fonctionnels. Ainsi :
- La demi-vie de la procaïne, un anesthésique local aujourd'hui dépassé, peut être augmentée en remplaçant le groupe ester –COO– par un groupe amide –CONH– pour donner du procaïnamide[2], utilisé comme anesthésique local en odontologie ainsi que comme antiarythmique.
- Un bioisostère de la xanthine, l'oxypurinol, est un inhibiteur de la xanthine oxydase, enzyme qui normalement dégrade la xanthine.
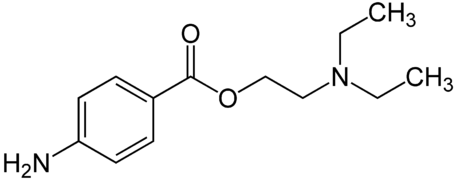 Procaïne, un anesthésique local aujourd'hui obsolète
Procaïne, un anesthésique local aujourd'hui obsolète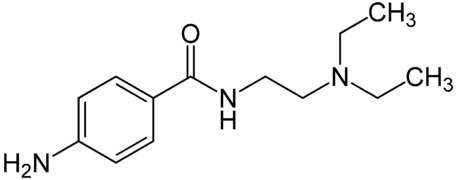 Procaïnamide, ayant une demi-vie augmentée
Procaïnamide, ayant une demi-vie augmentée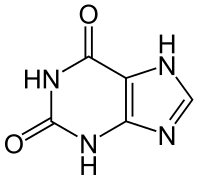
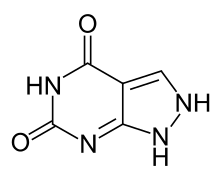 Oxypurinol, inhibiteur de la xanthine oxydase
Oxypurinol, inhibiteur de la xanthine oxydase
Notes et références
- (en) Nathan Brown, « Bioisosteres in Medicinal Chemistry », Wiley-VCH, 2012, p. 237. (ISBN 978-3-527-33015-7)
- (en) Leon Shargel, Alan H. Mutnick, Comprehensive Pharmacy Review, 6e édition, p. 264.