Conception de médicament
La conception de médicament, plus précisément conception de substance pharmacologiquement active[1] plus connue sous sa dénomination anglaise Drug design est l'ensemble des processus nécessaires à l'élaboration d'un médicament.
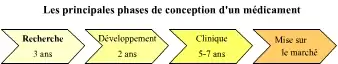
Dans l'industrie pharmaceutique, ces processus peuvent-être subdivisés et répartis en quatre phases ou étapes :
- La phase de recherche
- La phase de développement
- La phase clinique
- La phase de mise sur le marché
Remarque : Les phases de recherche et développement sont communément dénommées R&D.
Pour concevoir un médicament, il faut au préalable le chercher, l'identifier. Cette recherche, qui porte le nom de découverte de médicament ou drug discovery en anglais, s'est fondée sur différentes approches ou stratégies, au cours de ces derniers millénaires.
Historique
Depuis les débuts de la pharmacologie, les approches et les processus de recherche d'un médicament ont évolué pour devenir de plus en plus rationnelles.
Différentes approches usitées au cours du temps
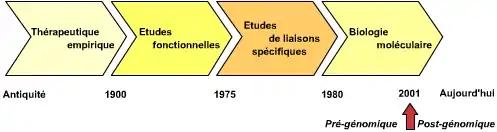
De l'Antiquité à nos jours les approches furent successivement :
- Les approches empiriques
- Les approches fonctionnelles
- Les approches moléculaires
- Les approches actuelles
Approches empiriques
De l'Antiquité à la fin du XVIIIe siècle, les médicaments ou les remèdes provenaient principalement de l'expérience accumulée des médecins au cours des millénaires. Ils ne reposaient pas sur des approches systématiques de découverte et de conception, même si de grands scientifiques de l'époque prônaient déjà l'importance de l'expérimentation, tels que Claudius Galenus (Galien, 129-200), ou encore Ibn Sina (Avicenne, 930-1037), qui avait rédigé de nombreux ouvrages sur les remèdes. Pour qu'un composé soit considéré comme un remède, il suffisait que son activité soit démontrée. La connaissance de son mécanisme d'action était inutile. Cette ère était celle de la thérapeutique empirique.
Approches fonctionnelles
Néanmoins, au début du XIXe siècle, en Europe, l'augmentation des connaissances en anatomie, en physiologie, en chimie, associée aux développement technologiques de l'époque ont permis l'émergence au sein de la médecine d'une nouvelle discipline, dénommée la pharmacologie.
Celle-ci, qui est la science du médicament, était fondée sur une approche expérimentale. À partir de ce moment-là, des stratégies diverses et variées ont vu le jour pour aboutir à l'aube du XXe siècle avec les approches dites fonctionnelles, ainsi qualifiées car elles se devaient de démontrer l'effet d'un composé sur une fonction de l'organisme tel que la respiration, la digestion, etc. Les composés étudiés et testés étaient principalement des produits d'origine naturelle et la découverte d'une nouvelle substance bio-active était plus ou moins le fruit de la chance.
Approches moléculaires
Par la suite, vers le milieu des années 1970, de nouvelles méthodologies, nommées approches moléculaires, dues à la généralisation de l'utilisation des techniques de liaisons spécifiques ont vu le jour. Ces approches furent qualifiées de moléculaires car l'observation et la démonstration ne se font plus ni au niveau de l'organisme, ni au niveau de la fonction, mais à une échelle encore plus petite celle de la molécule. La molécule exogène (le médicament) étant le ligand et la molécule endogène ciblée étant le récepteur qui initiera une réponse de l'organisme.
Approches actuelles
À partir du début des années 1970, une panoplie de stratégies se sont développées en parallèle. Celles-ci présentent chacune leurs avantages et leurs inconvénients. De nos jours, la problématique posée et les contraintes de départ orienteront le choix de l'approche, voire vers une combinaison de celles-ci.
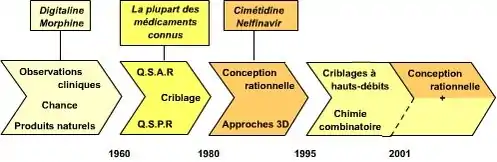
On peut distinguer trois grands types d'approches :
- Les approches par criblages à haut débit
- Les approches par chimie combinatoire
- Les approches rationnelles
Approches rationnelles
Les approches rationnelles sont basées sur l'obtention de données détaillées sur le mécanisme pathologique et sur les étapes biochimiques qui sont impliquées. Ceci suppose d'avoir identifié et validé la ou les étapes et les molécules biologiques impliquées : le récepteur à la surface de la cellule, l'enzyme... Cette validation suppose d'établir un lien direct entre la pathologie et la cible permettant d'espérer un effet thérapeutique. Cette validation peut s'appuyer sur les données des études génétiques et génomiques (mutation associée à la pathologie), sur des données biochimiques (altérations métaboliques, dosages enzymatiques) et sur des études chez l'animal.
Lorsque la cible est validée, deux approches sont envisageables : celles qui sont basées sur la structure des ligands connus et celles qui sont basées sur la structure de la cibles.
- Lorsque des ligands naturels de la cible sont connus, comme des agonistes ou des antagonistes d'un récepteur, on peut en synthétiser des analogues par des approches de chimie médicinale, afin de tester leur activité. En corrélant leur activité biologique avec leur structure, on peut alors établir des règles pour améliorer les molécules testées et obtenir des médicaments.
- Les approches les plus récentes sont basées sur la détermination de la structure tridimensionnelle de la cible, par des techniques de biologie structurale. À partir de cette structure, on effectue alors la conception rationnelle de molécules chimiques capables de se fixer à la cible et de former des interactions avec elle.
Aujourd'hui, la conception rationnelle d'un médicament s'appuie sur de nombreuses disciplines intimement interconnectées telles que la Chimie, Biochimie, Biologie structurale, Génomique, Bio et Chemoinformatique, Modélisation moléculaire, etc.
Approches par criblage à haut débit
L'automatisation des tâches via l'utilisation de robots et de logiciels de traitement de données permet de tester et d'analyser une importante quantité de composés chimiques sur une ou plusieurs cibles d'intérêt.
Approches par chimie combinatoire
Les approches présentées jusqu'ici consistaient à tester des composés chimiques préalablement purifiés et identifiés. En revanche, cette approche procède comme suit. Avec, tout d'abord, la synthèse d'un très grand nombre de composés chimiques. Par la suite, on mesure l'effet de ce mélange sur l'activité biologique. Et s'il s'avère qu'un effet est observé, un processus de déconvolution permettra alors de remonter au composé responsable de cette activité.
Notes et références
- Journal officiel de la république française, avis et communications, avis divers, commission d’enrichissement de la langue française, Vocabulaire de la chimie et des matériaux, (liste de termes, expressions et définitions adoptés) 28 janvier 2020
- (en) D.A. Matthews, R.A. Alden, J.T. Bolin, S.T. Freer, R. Hamlin, N. Xuong, J. Kraut, M. Poe, M. Williams et K. Hoogsteen, « Dihydrofolate reductase: x-ray structure of the binary complex with methotrexate. », Science, vol. 197, , p. 452-455 (PMID 17920, DOI doi:10.1126/science.17920)
Liens externes
- (fr) Le médicament : de la recherche à la commercialisation
- VLS3D Liste de logiciels pour la conception rationnelle de molécules thérapeutiques (Villoutreix et al., Drug Discovery Today, 18:1081-9, 2013)
Bibliographie
- Principes fondamentaux de chimie thérapeutique, médicaments, propriétés physico-chimiques, prodrogues, pharmacophore Roland Barret, (ISBN 978-1-78406-481-5)
- Graham L. Patrick, Chimie Pharmaceutique, éditions de Boeck Supérieur, (ISBN 9782744501548)
- Un livre pratique de chimie médicinale avancée - I: La chimie médicinale avancée concerne la chimie, la synthèse, le SAR, le MOA, les propriétés et les utilisations des médicaments, Awadh Kishor éditions Sciencia Scripts (ISBN 978-6200893529)