Acide zolédronique
L'acide zolédronique (DCI) ou zolédronate est un bisphosphonate. Il s'agit d'un médicament utilisé dans le traitement de l'ostéoporose.
| Acide zolédronique | ||
| ||
 | ||
| Identification | ||
|---|---|---|
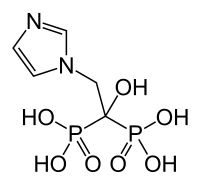
| Nom UICPA | acide 1-hydroxy-2-(1H-imidazol-1-yl)éthane-1,1-diyl]bis(phosphonique | |
| No CAS | ||
| Code ATC | M05 | |
| DrugBank | APRD01294 | |
| PubChem | 68740 | |
| Propriétés chimiques | ||
| Formule | C5H10N2O7P2 [Isomères] |
|
| Masse molaire[1] | 272,089 6 ± 0,007 2 g/mol C 22,07 %, H 3,7 %, N 10,3 %, O 41,16 %, P 22,77 %, |
|
| Données pharmacocinétiques | ||
| Biodisponibilité | 22 % | |
| Métabolisme | nul | |
| Demi-vie d’élim. | 146 heures | |
| Excrétion |
rénale (partielle) |
|
| Considérations thérapeutiques | ||
| Voie d’administration | I.V | |
| Unités du SI et CNTP, sauf indication contraire. | ||
Histoire
Introduit dans le commerce le , l'acide zolédronique est préconisé pour les complications osseuses chez des patients atteints de pathologies malignes, le traitement et la prévention de l'ostéoporose, le traitement du cancer de la prostate, le traitement de l'hypercalcémie maligne, le traitement de la douleur induite par des métastases osseuses, certaines fractures chez la femme ménopausée et la maladie de Paget.
La mise en commerce de ce principe actif a un réel impact sur la médecine d'aujourd'hui. Il a permis de réduire le risque de fracture de 35 %, et le risque de mortalité de 28 %.
L'acide zolédronique est le seul bisphosphonate qui a été développé exclusivement pour l'injection intraveineuse (IV), qui a conduit à une administration seulement une fois par an dans le traitement de l'ostéoporose.
Mode de production
La synthèse de l'acide zolédronique est très complexe et ne peut être réalisée que grâce à deux autres synthèses, réalisée préalablement de celle-ci : celle de l'hydrochlorure de l'acide imidazole-1-yl-acétique et celle de l'imidazole-1-yl-acétate tertiobutylique[2].
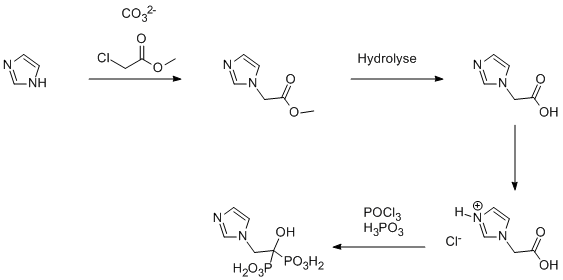
Synthèse de l'imidazole-1-yl-acétate tertiobutylique
Dans une solution d'imidazole (C3H4N2) dans de l'acétate d'éthyle , du carbonate de potassium (K2CO3) suivi par du chloroacétate de tertiobutyle (C6H12O2) sont ajoutés et le mélange est porté à reflux pendant 10 heures environ. Après son séchage, le solide est agité puis lavé, ce qui donne de l'imidazole-1-yl acétate tertiobutylique, un solide blanc.
Synthèse de l'hydrochlorure de l'acide imidazole-1-yl-acétique
À une solution d'imidazole-1-yl-acétate tertiobutylique dans du dichlorométhane, du tétrachlorure de titane (TICl4) est ajouté goutte à goutte pendant une heure. Ensuite, de l'acide isopropylique (C3H8O) est ajouté doucement pendant 3 heures. Le dichlorométhane est éliminé par distillation et cela donne un solide blanc cassé, l'hydrochlorure de l'acide imidazole-1-yl-acétique.
Synthèse de l'acide zolédronique
Dans une suspension contenant de l'hydrochlorure de l'acide imidazole-1-yl-acétique, ainsi que de l'acide phosphoreux (H3PO3) dans du chlorobenzène (C6H5Cl) de l'oxychlorure de phosphore (POCl3) est ajouté pendant environ 5 heures. La masse obtenue est refroidie avec de l'eau, ensuite la couche aqueuse est portée à reflux pendant 18 heures, et enfin refroidie et diluée avec du méthanol. Le solide obtenue est l'acide zolédronique, après être filtré, lavé à l'eau froide puis au méthanol et enfin séché sous vide pendant 12 heures.
Cette synthèse présente plusieurs avantages : Elle permet une production de l'acide zolédronique avec un meilleur rendement (80 % au lieu de 14 % par d'autres voies de synthèse), il y a àgalement une facilité de l'industrialisation du processus à des fins commerciales. On note aussi une constance du rendement en acide zolédronique constant et de sa pureté de plus de 99,8 % et une absence de réaction exothermique dans le processus et donc une simplicité et sureté de celui-ci.
Mécanismes d'action
Ostéoporose
L’os est un tissu qui se forme et se résorbe continuellement. Ce phénomène est appelé : remodelage osseux.
Il existe deux types de cellules intervenant dans ce remodelage : les ostéoblastes et les ostéoclastes. La résorption osseuse est assurée par les ostéoclastes tandis que les ostéoblastes interviennent dans la reconstruction osseuse.
Un déséquilibre de ces phases provoque l'ostéoporose. L'os ainsi fragilisé devient beaucoup moins résistant et se fracture plus facilement. Les fractures peuvent se produire spontanément comme pour les vertèbres ou à la suite d’un choc. L'inhibition de la résorption osseuse de l'acide zolédronique est très prolongée puisqu'elle peut persister au delà de cinq ans après une unique injection[3].
Les cellules tumorales et la résorption
L’ostéolyse tumorale résulte de la stimulation excessive de l’activité des ostéoclastes et de l’inhibition des ostéoblastes par les cellules tumorales. Certaines molécules peuvent être utiles pour le traitement de cette ostéolyse, il faut alors employer des molécules avec des propriétés anti-résorptives tels que les bisphosphonates ou les anticorps anti-RANKL (denosumab)[4].
La destruction de l’os est liée à une infiltration tumorale métastatique qui, par l’intermédiaire de produits d’origine tumorale comme le Parathyroid Hormone-related peptide (Ph-rp), agit en stimulant la production d’ostéoclates et favorise ainsi la destruction de l’os. Cette résorption est aussi due à d’autres facteurs libérés par les cellules tumorales qui entrainent une augmentation de l’expression de RANKL par les ostéoblastes. De plus lors de la destruction de l’os il y a libération de calcium et des facteurs augmentant aussi la production de PTH-rp et la croissance tumorale. Il s’agit d’un cercle continu dans lequel l’activité des ostéoblastes ne peut plus compenser l’activité des ostéoclastes entrainant petit à petit la destruction osseuse et augmentant également la croissance tumorale.
On utilise alors les bisphosphonates ou des inhibiteurs de RANKL afin de diminuer cette résorption osseuse et les facteurs favorisant la croissance tumorale
L’acide zolédronique possède également plusieurs propriétés anti-tumorales qui contribuent à son efficacité dans le traitement des métastases osseuses. Bien que l'utilisation de l'acide zolédronique ne peut ni supprimer ni arrêter la propagation du cancer, il peut être utilisé pour traiter la maladie osseuse chez les patients qui souffrent du cancer. Il agit en ralentissant la dégradation osseuse et en diminuant la quantité de calcium libérée par les os, dans le sang.
Indications
Ce médicament est indiqué dans la prévention des fractures au cours de l'ostéoporose, sous forme d'une perfusion annuelle. Il permet une diminution significative du risque de survenue de fractures[5]. Ce bénéfice est conservé même si l'intervalle entre chaque perfusion est prolongée à 18 mois[6]. Utilisé à distance d'une fracture de hanche, il est même constaté une diminution de la mortalité[7], possiblement en raison d'effets autres qu'osseux[8].
Il est également utilisé dans les hypercalcémies secondaires à l'atteinte osseuse certains cancers.
Aclasta & Zometa
Les deux principaux médicaments contenant de l'acide zolédronique sont commercialisés sous les noms d'Aclasta et le Zometa par le même laboratoire, Novartis. La différenciation des deux produits est sur son dosage (5 mg pour le premier et 4 mg pour le second) avec un positionnement commercial également différent. Le médicament est également disponible sous forme générique.
Aclasta
L'Aclasta est indiqué dans le traitement de la maladie osseuse de Paget, de l'ostéoporose postménopausique, de l'ostéoporose masculine et de le l'ostéoporose cortisonique[9]. Il a été mis sur le marché en par les laboratoires NOVARTIS. La dose recommandée est une perfusion intraveineuse de 5 mg d'acide zolédronique (anhydre) dans une solution aqueuse de 100 mL, administrée par l'intermédiaire d'un dispositif de perfusion, avec prise d'air, à vitesse de perfusion constante. La durée de la perfusion ne doit pas être inférieure à 15 minutes.
Zometa
Le Zometa est utilisé pour prévenir les fractures squelettiques chez les patients atteints de cancers tels que myélome multiple ou le cancer de la prostate,ainsi que dans le traitement de l'ostéoporose[10] - [11]. Il peut aussi être utilisé dans le traitement de l'hypercalcémie maligne et peut être utile dans le traitement de la douleur induite par des métastases osseuses.
Lorsqu'il s'agit d'une hypercalcémie provoquée par une tumeur, la dose initiale recommandée est de 4 mg donnée 1 seule fois sous la forme d'une injection intraveineuse
Lorsqu'il s'agit de métastases osseuses et d'un myélome multiple, la dose recommandée est de 4 mg donnée 1 seule fois sous la forme d'une injection intraveineuse toutes les 3 ou 4 semaines. Dans ce cas la, l'acide zolédronique peut être donné avant ou après un traitement par chimiothérapie.
Contre-indication
Atteintes rénales : Le médicament Zometa, en particulier, peut causer une altération de la fonction rénale. L'acide zolédronique n'est donc pas recommandé aux personnes atteintes d'une grave maladie du rein.
Somnolence ou vigilance réduite : l'acide zolédronique peut causer de la somnolence et des étourdissements.
Grossesse : L'utilisation de l'acide zolédronique à travers le médicament Zometa ne doit pas être ingéré pendant une grossesse.
Allaitement : Aucune indication est présente pour déterminer si l'acide zolédronique peut passer dans le lait maternel pendant que la mère allaite. Il est donc déconseillé de l'utiliser pendant l'allaitement du nouveau-né.
Effets secondaires
Les effets indésirables et secondaires sont répertoriés en fonction de leur localisation dans le corps humain. Ci-dessous, certains effets secondaires classés en 3 catégories :
Très fréquent : >1/1000
Fréquence basse : <1/1000
Pas de fréquence
Les effets secondaires les plus fréquents classés par thème[12]
| Symptômes | |
|---|---|
| Dermatologie | |
| Divers | Frisson, Fièvre, Fatigue, Douleur |
| Hématologie | Anémie |
| Immuno-allergologie | Œdème de Quincke |
| Infectiologie | Grippe |
| Nutrition | Augmentation du poids |
| Instrumentation | Douleur au point d'injection |
| Ophtalmologie | Conjonctivite, Douleur oculaire, Vision floue |
| Psychiatrie | Léthargie |
| ORL, stromatologie | Rhino-pharyngite, Sensation de vertige |
| Système cardiovasculaire | Hypertension artérielle |
| Système digestif | Anorexie, Crampe |
| Système nerveux | Trouble du sommeil |
| Système respiratoire | Toux, Dyspnée |
| Urologie | Néphropatie |
La survenue d'une fibrillation auriculaire est décrite[5]
Comparaison entre l'acide zolédronique, le placébo et le dénosumab
La voie RANKL
Elle joue un rôle essentiel dans l’ostéolyse tumorale. On utilise donc le dénosumab, anticorps monoclonal, qui présente une haute spécificitée pour le RANKL afin d’inhiber la formation et les fonctions des ostéoclastes ainsi que leur survie. Le Dénosumab et les bisphosphonates possèdent donc d’un mécanisme d’action différent puisque les bisphosphonates se lient à l’os sur les sites de résorption et entrainent la perte de fonction des cellules tandis que le dénosumab permet la diminution du nombre d’ostéoclastes.
Le cancer du sein avec métastases osseuses : les inhibiteurs de la résorption
Les cellules tumorales stimulent l'activité des ostéoclastes mais inhibent également l'activité des ostéoblastes, notamment au cours du cancer du sein.
L’efficacité de l’acide zolédronique chez des patientes atteintes du cancer du sein avec métastases osseuse a été étudié afin de diminuer le taux de complication osseuses et/ou augmenter le délai du premier événement osseux.
Cette étude compare l’efficacité de ce bisphosphonate à un placébo ou un groupe sans bisphosphonates et montre qu’ils diminuent réellement le risque d’événement osseux mais ne modifient pas la survie.
La principale étude a été publiée par Stopeck en 2010. Elle a été réalisée en double aveugle afin de comparer l’efficacité de l’acide zolédronique (4mg en intraveineuse) à celle du dénosumab (120mg en sous cutané) toutes les 4 semaines et en incluant 2046 patientes. Cette étude a ainsi montré une supériorité du dénosumab par rapport à l’acide zolédronique pour retarder la survenue de la première complication osseuse. En effet, le temps moyen de l’apparition du premier événement squelettique était de 26,4 mois pour l’acide zolédronique et à ce moment-là les patients ayant pris du dénosumab ne présentaient aucune complication. Le dénosumab a permis de diminuer le risque de 23 % par rapport à l’acide zolédronique cependant la survie globale et la progression de la maladie étaient similaires avec les deux traitements.
Le cancer de la prostate avec métastases osseuses
Dans ce cas là il existe une augmentation de la prolifération et de l’activité ostéoblastique, mais également une ostéolyse ce qui explique l’intérêt des inhibiteurs de la résorption osseuse.
Là encore, il existe une étude comparant l’efficacité de l’acide zolédronique par rapport au placébo qui a été réalisée chez 643 patients ayant un cancer de la prostate. On a alors observé une diminution significative de l’incidence des événements osseux avec l’acide zolédronique et, au bout de deux ans, 49 % des patients ayant pris du placébo ont connu leur premier événement osseux contre 38 % des patients recevant de l’acide zolédronique. De plus la douleur a largement diminué avec la prise d’acide zolédronique.
Une autre étude a été réalisé afin de comparer l’efficacité de l’acide zolédronique à celle du dénosumab dans cette pathologie. Il s’agit là encore d’une étude en double aveugle chez 1901 patients. On observe que le premier événement osseux apparait au bout de 20,7 mois avec le dénosumab et au bout de 17,1 mois avec l’acide zolédronique et que la survie globale n’est pas différente.
Les métastases osseuses des autres tumeurs solides
L'efficacité de l'acide zolédronique a été également étudiée au cours d'autres cancers avec métastases osseuses, notamment en cas de cancer pulmonaire et de cancer du rein. Une étude a été effectuée chez 773 patients présentant une tumeur solide avec métastases osseuse. Les patients recevaient de l’acide zolédronique ou du placébo et il a été démontré que l’acide zolédronique a retardé de manière significative l’apparition de la première complication osseuse et diminué l’incidence annuelle de ces événements.
L’acide zolédronique a aussi été comparé au dénosumab chez 1776 patients et a démontré une non infériorité du dénosumab mais pas de supériorité par rapport à l’effet de l’acide zolédronique pour retarder l'apparition du premier événement osseux.
Selon des experts internationaux du « national compréhensive cancer network » (NCCN), l’acide zolédronique représente un bisphosphonate de choix chez les patients atteints des cancers énoncés précédemment ainsi que le Dénosumab.
La durée optimale d'un traitement inhibiteur de la résorption
La question du ratio bénéfice/ risque se pose au-delà d'un traitement de 24 mois.
Certains essais cliniques en cours évaluent la possibilité d'autres schémas d'administration avec notamment un espacement de l'intervalle d'administration après un an de traitement mensuel par acide zolédronique.
L'acide pamidronique et l'acide zolédronique ont l'avantage d'une action plus rapide et plus durable que les bisphosphonates oraux, mais nécessitent une administration par voie intraveineuse et induisent de fréquents effets indésirables.
Liens externes
- Compendium suisse des médicaments : spécialités contenant Acide zolédronique
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Process of making zoledronic acid », sur google, (consulté le )
- Grey A, Bolland MJ, Horne A et al. Five years of anti-resorptive activity after a single dose of zoledronate — results from a randomized double-blind placebo-controlled trial, Bone, 2012;50:1389-1393
- Françoise DEBIAIS, Traitements de l'ostéolyse au cours des métastases osseuses: Biphosphonates, anticorps anti-RANKL, perspectives, Poitiers, 2014-2015, 11 p.
- (en) Black DM et al. « Once-yearly zoledronic acid for treatment of postmenopausal osteoporosis » N Engl J Med. 2007;356(18):1809-22.
- Reid IR, Horne AM, Mihov B et al. Fracture prevention with zoledronate in older women with osteopenia, N Engl J Med, 2018;379:2407-2416
- Lyles KW, Colón-Emeric CS, Magaziner JS et al. Zoledronic acid and clinical fractures and mortality after hip fracture, N Engl J Med, 2007;357:1799-1809
- Colón-Emeric CS, Mesenbrink P, Lyles KW et al. Potential mediators of the mortality reduction with zoledronic acid after hip fracture, J Bone Miner Res, 2010;25:91-97
- Aclasta, Haute Autorité de Santé, , 9 p.
- « Zometa », sur Novartis
- (en) National Prescribing Service (2009). "Zoledronic Acid for Osteoporosis". Medicines Update, consultable en ligne à http://www.nps.org.au/consumers/publications/medicine_update/issues/Zoledronic_acid
- « Acide zolédronique », sur vidal, (consulté le )