Titanocène
Le titanocène est un composé organométallique du titane appartenant à la famille des métallocènes et de formule chimique (η5-C5H5)2Ti. L'existence du titanocène sous la forme de monomère à l'état solide n'a pas été démontrée à ce jour, mais des dérivés substitués, tel que le décaméthyltitanocène (Ti(Cp*)2) existent. Comme pour tous les autres métallocène, l'atome central métallique, ici le titane, est à l'état d'oxydation +II. De ce fait, le complexe titanocène possède seulement 14 électrons de valence, et est donc un puissant oxydant.
| Titanocène | |

| |
| Identification | |
|---|---|
| Nom UICPA | cyclopenta-1,3-diène;titane(2+) |
| Synonymes |
titanocène, |
| No CAS | |
| PubChem | 92881 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C10H10Ti [Isomères] |
| Masse molaire[1] | 178,053 ± 0,01 g/mol C 67,46 %, H 5,66 %, Ti 26,88 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Structure
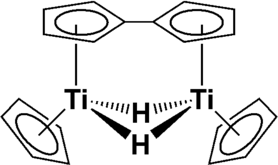
Avec seulement 14 électrons de valence, le titanocène manque de quatre électrons pour avoir une configuration stable, et a donc tendance à se stabiliser en formant des complexes dimériques, incluant des liaisons avec des atomes d'hydrogène. Les deux liaisons hydrogène avec les deux atomes de titane forment ainsi un système à trois centres et deux électrons, tandis que deux ligands cyclopentadiényle forment un fulvalènediényle, formant ainsi un complexe à 16 électrons de valence.
Synthèse
Le titanocène peut être synthétisé par réaction entre le sodium et le dichlorure de titanocène.
- Cp2TiCl2 + 2 Na → Cp2Ti + 2 NaCl
Parmi d'autres synthèses possibles, on peut citer la thermolyse du dicyclopentadiényldiphényltitane (Cp2Ti(C6H6)2) ou du dicyclopentadiényldiméthyltitane (Cp2Ti(CH3)2) (Cp=Cyclopentadiényle).
Bibliographie
- (de) Holleman, Wiberg: Lehrbuch der Anorganischen Chemie, 101e édition, 1995, p. 1700.
- (en) Hans Brintzinger, John E. Bercaw: Nature of so-called titanocene, (C10H10Ti)2, in: J. Am. Chem. Soc., 1970, 92, p. 6182-6185 DOI 10.1021/ja00724a013.
Notes et références
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Titanocen » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.